Что такое послеоперационное воспаление глаза
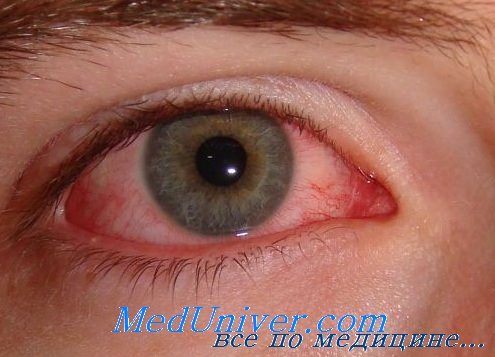
Причины воспаления глаза после операции, травмыСреди возбудителей послеоперационного эндофтальмита также преобладают грамположитсльные бактерии. Грамотрицательную флору и микробные ассоциации при послеоперационном эндофтальмите можно встретить значительно реже, чем при раневой инфекции. В последние годы отмечено ослабление вирулентности микроорганизмов при послеоперационных зндофтальмитах и сохранение высокой вирулентности при посттравматическом эндофтальмите (Воhigian, Olk, Picker et al., Speaker, Drady et el., Owens et al., Treumer). Установлена причина позднего хронического вялотекущего эндофтальмита. Это слабовирулентная грамположительная микрофлора: Propionihacterium acnes, Candida parapsilosis, diphtheroids, которые пребывают в глазу несколько месяцев и даже лет. Возбудители, как правило, находятся между листками капсулы хрусталика на гаптических элементах ИОЛ и, постоянно стимулируя иммунную систему глаза, вызывают хроническое персистирующее воспаление с помутнением задней капсулы хрусталика. Взгляды авторов по вопросу о возможности по бактериальной флоре конъюнктивы судить о непосредственном возбудителе внутриглазной раневой инфекции противоречивы. В этой связи нами произведен анализ бактериологических исследований, проведенных у больных с внутриглазной инфекцией, находившихся на стационарном лечении в отделе травматологии Московского научно-исследовательского института глазных болезней им. Гельмгольца в период с 1968 по 2007 гг. (Южаков А. М.). В связи с известной длительностью микробиологического исследования, а также быстротой прогрессирования внутриглазного инфекционного процесса следует придавать большое значение взятию соответствующего материала на посев у пострадавших с прободными травмами глаза, когда клинические признаки инфицирования раны еще отсутствуют. Однако чаще всего эти исследования, особенно 15-20 лет назад (а во многих областных и районных больницах даже и в настоящее время), не проводятся. У остальных 43 больных со свежей прободной травмой глазного яблока при их поступлении в стационар материал на посев не брали. Анализ историй болезни показал, что эти пострадавшие поступили в институт в вечернее и ночное время или в выходные и праздничные дни. Как показал анализ историй болезни и сопроводительных документов пострадавших с инфицированными проникающими ранениями глаза, направленных в институт из других офтальмологических учреждений, ранние бактериологические исследования были проведены в 12 из 195 случаев.
Было выяснено, что посевы осуществлялись чаще всего с одного и реже с двух объектов — с конъюнктивы или с извлеченного из глаза инородного тела. По результатам проведенного бактериологического исследования, микрофлора обнаружена только у 8 из 47 пострадавших со свежими проникающими ранениями глазного яблока. У 5 пострадавших бактерии обнаружены в посевах с конъюнктивы и у 3 — с извлеченного из глаза инородного тела. Из общего числа положительных находок в 4 случаях был выделен стафилококк с отрицательной реакцией плазмокоагуляции, в 1 — плазмокоагулирующий стафилококк, в 2 — палочка ксероза и в 1 — диплококк. Выделенные микроорганизмы оказались резистентны к пенициллину, ампициллину, стрептомицину, тетрациклину и левомицетину, но чувствительны к канамицину, неомицину, мономицину. Из 8 пострадавших, у которых при раннем бактериологическом исследовании была обнаружена в глазу та или иная микрофлора, у 3 больных при уже развитой клинической картине внутриглазной инфекции в повторных посевах, взятых с конъюнктивы или внутриглазных экссудатов, роста бактерий не обнаружено. В остальных 5 случаях инфекции глаза повторные бактериологические исследования не проводились. При развившемся внутриглазном инфекционном процессе бактериологическое исследование проведено у 273 больных. Помимо посевов с конъюнктивы или с извлеченного из глаза инородного тела, брали на посев влагу передней камеры или экссудат измененного стекловидного тела. Внутриглазные жидкости нужны были для бактериологического исследования в тех случаях, когда с лечебной целью производился парацентез роговицы с промыванием передней камеры глазного яблока раствором антибиотика или удалялся внутриглазной осколок диасклерально. У некоторых больных экссудат из полости глаза был взят на посев во время операции замещения стекловидного тела, а также при интравитреальном введении антибиотика. В ряде случаев исследовались извлеченные хрусталиковые массы, отсеченные инфильтрированные участки радужной оболочки, которые были ущемлены в ране роговицы и при осмотре определялись как нежизнеспособные. У некоторых пострадавших с инфицированными проникающими ранениями глазного яблока брали на посев содержимое из области раны. Возбудители инфекции выявлены только у 41 (14,9%) больного. Обнаруженная микрофлора у 32 больных была представлена монокультурой бактерий и у 9 имела смешанный характер. Из общего числа обнаруженных видов микроорганизмов в 24 случаях выявлен стафилококк, не обладавший, по данным бактериологического исследования, патогенными свойствами, в 3 — патогенный стафилококк, в 7 — палочка ксероза, в 4 — сенная палочка, в единичных случаях — пневмококк, стрептококк, диплококк. Из 32 штаммов микроорганизмов, исследованных на чувствительность к антибиотикам, 30 были резистентны к пенициллину, 19 — к стрептомицину, 15 — к тетрациклину, 14 — к левомицетину. В 17 случаях микроорганизмы проявляли резистентность одновременно к пенициллину, стрептомицину, левомицетину. Исследованные штаммы были чувствительны к гентамицину, канамицину, мономицину, неомицину. Таким образом, при бактериологическом исследовании ограниченного числа объектов (1-2) в случаях развившегося внутриглазного воспалительного процесса после прободных ранений глазного яблока складывается впечатление, что их инфицированность невелика — 14,9% случаев. – Также рекомендуем “Причины эндофтальмита при проникающих ранениях. Воспаление глаза от инородного тела” Оглавление темы “Микрофлора глаза и причины его воспаления”:
|
Источник
 Современная методика удаления катаракты путем факоэмульсификации применяется во всем мире и является максимально безопасной и надежной. Риски послеоперационных осложнений сведены к минимуму, но все же присутствуют. Воспаление роговицы после операции катаракты относится к раннему послеоперационному осложнению, которое при своевременном лечении быстро устраняется. Именно по этой причине важно не пропускать контрольные осмотры после проведения операции.
Современная методика удаления катаракты путем факоэмульсификации применяется во всем мире и является максимально безопасной и надежной. Риски послеоперационных осложнений сведены к минимуму, но все же присутствуют. Воспаление роговицы после операции катаракты относится к раннему послеоперационному осложнению, которое при своевременном лечении быстро устраняется. Именно по этой причине важно не пропускать контрольные осмотры после проведения операции.
Причины возникновения воспаления
Воспаление после операции катаракты могут возникнуть из-за чрезмерного воздействия ультразвука во время факоэмульсификации. Длительное воздействие ультразвуковых волн на помутневший хрусталик требуется в случаях удаления созревшей катаракты. Плотность помутнения в таком случае высокая, поэтому хрусталик тяжело поддается дроблению. Длительность воздействия ультразвука увеличивается, что в свою очередь негативно влияет на весь глаз в целом. Для защиты расположенных вблизи элементов зрительного органа применяется вискоэластик, но в редких случаях этого оказывается недостаточно.
Воспаление может возникнуть также в результате проведения имплантации ИОЛ через большой разрез. При увеличении разреза риски воспаления значительно возрастают. Для исключения такого риска применяются мягкие интраокулярные линзы, которые вводятся в переднюю камеру через минимальный разрез в свернутом виде. Высокая квалификация и опыт хирурга, выполняющего операцию, гарантирует точное и аккуратное введение ИОЛ. При формировании микроразреза фемтосекундным лазером достигается более точный профиль разреза, а также быстрейшее его заживление и снижение отечности роговицы после проведения операции.
В очень редких случаях в течение первых суток после проведения операции может возникнуть неинфекционное воспаление, признаком которого является отек роговицы и резкое ухудшение зрения. Причиной такой реакции может быть токсическая реакция на ирригационный раствор, применяемый во время факоэмульсификации. Также реакция может возникнуть на остатки вискоэластика, который не был удален полностью после процедуры.
Какие еще могут быть осложнения
К ранним осложнениям также можно отнести кровоизлияния после удаления катаракты, которые могут быть следствием травматического воздействия фиксирующих элементов конструкции интраокулярной линзы. Такое повреждение может возникнуть в результате травматического воздействия на глаз, давления, трения руками и неосторожного поведения в первые дни после операции. Как правило такое осложнение устраняется при помощи капель, которые помогают рассасыванию кровоизлияния. Также стоит отметить, что моноблочная конструкция интраокулярной линзы из мягкого материала позволяет исключить такой риск травмирования глаза.
Повышение внутриглазного давления может быть вызвано проблемами с дренажной системой глаза, которая возникает в результате недостаточно тщательного вымывания вискоэластика. Для устранения осложнения назначается медикаментозная терапия.
Смещение искусственного хрусталика может возникнуть в случае травматического воздействия на глаз в ранний послеоперационный период. Также в исключительно редких случаях может быть неправильно подобран размер интраокулярной линзы, которая из-за этого недостаточно надежно фиксируется внутри капсулы.
Предотвращение и устранение осложнений
В послеоперационный период нужно придерживаться несложных правил:
- применять все назначенные врачом препараты;
- следить за самочувствием и в случае обнаружения неприятных симптомов обращаться к офтальмологу;
- ограничить физические нагрузки;
- исключить употребление алкоголя, чтобы исключить риск травматизма повышения внутриглазного давления;
- не тереть глаза и избегать попадания в них воды и мыла во время гигиенических процедур;
- отказаться от косметики;
- ограничить зрительные нагрузки, следя за усталостью глаз и обеспечивая им своевременный отдых;
- отказаться от посещения бассейна, сауны и открытых водоемов;
- использовать солнцезащитные очки во время длительного пребывания на улице.
Для предотвращения развития воспаления в послеоперационный период в обязательном порядке назначаются препараты искусственной слезы. Также применяются лекарственный препараты, обеспечивающие стимуляцию процессов регенерации и уменьшения отечности роговицы в первые дни после операции. Зрительная реабилитация в случае регулярного приема назначенных офтальмологом препаратов протекает быстро и без осложнений. Также важно в этот период соблюдать график контрольных осмотров и придерживаться ограничений физической активности.
Источник
Сергушев С.Г.
Что мы понимаем под термином «воспаление»? Воспаление – это типический патологический процесс, развивающийся при повреждении тканей и проявляющийся нарушением кровообращения, изменением крови и соединительной ткани в виде альтерации, экссудации и пролиферации. Само понятие «воспаление» гораздо старше, чем само человечество, поскольку воспалительная реакция уже существовала, когда на Земле появились первые многоклеточные организмы. Признаки воспаления описаны еще в древности Цельсом и Галеном. Они дали основные признаки, которые хорошо известны, и их учат еще студенты:
• tumor (припухлость, отек),
• rubor (жар, температура),
• calor (покрасненние),
• dolor (боль),
• functio laesa.
Этиологические причины воспаления. Любая причина, по силе и длительности превосходящая адаптационные возможности ткани, вызывает воспаление. Причины воспаления (флогогенные факторы) могут быть двух видов: внешние и внутренние.
Флогогенные факторы: экзогенные (внешние) – ‘микроорганизмы (бактерии, вирусы, грибы), животные организмы (простейшие, черви, насекомые), химические вещества (кислоты, щелочи), механические (инородные тела, травма) и термические воздействия (холод, тепло), лучевая энергия (рентгеновские, ультрафиолетовые лучи). Эндогенные (внутренние) факторы – это факторы, возникающие в самом глазу в результате иного заболевания (опухоль, отслойка сетчатки, глаукома, диабет, аутоиммунные заболевания).
Каковы же механизмы начала, развития и исхода процесса воспаления? Прежде всего это повреждение от действия флогогенного агента (первичная альтерация), которая вызывает выброс из клеток и образование биологически активных веществ – медиаторов воспаления, освобождение и активацию лизосомальных ферментов, действие их на биологические макромолекулы (вторичная альтерация), которые в свою очередь вызывают нарушения микроциркуляции, повышение проницаемости стенок сосудов, экссудацию. Все это приводит к размножению клеток (пролиферация) и ликвидации дефекта.
Итак, стадии воспаления:
• альтерации (повреждения): первичная, вторичная;
• экссудации и эмиграции;
• пролиферации и репарации: пролиферация, завершение воспаления.
Хотелось бы остановиться на общих принципах терапии, которые применяются в разработке практически любой схемы лечения. Лечение должно быть, прежде всего, этиотропным, направленным на устранение причины или этиологического фактора; патогенетическим, направленным на прерывании самих процессов воспаления; саногенетическим, т.е. обращать внимание нужно не только на тот орган, который мы лечим и непосредственно на который жалуется пациент, а лечить весь организм в целом; и симптоматическим, направленным на подавление патологических симптомов (жар, боль и т.д.).
Какие противовоспалительные средства сейчас существуют? Прежде всего, это нестероидные противовоспалительные средства (НПВС); стероидные противовоспалительные средства (СПВС) и противовоспалительные средства медленного действия, или средства так называемой «базисной» терапии. В патогенезе некоторых воспалительных (как правило, системных) заболеваний существенную роль играет гиперчувствительность замедленного типа. В ее осуществлении участвуют цитотоксические Т-лимфациты, разрушающие клетки, имеющие на своей поверхности антигены.
При лечении этих заболеваний и применяются базисные средства, для которых характерно развитие медленного эффекта – через несколько месяцев после начала лечения (делагил, пенициллинамин, препараты золота), цитостатики, а также циклоспорины.
Хотелось бы коротко сказать о стероидах. Плюсами стероидной терапии являются очень мощный противовоспалительный эффект, антипролиферативный эффект и иммуносупрессия. Правда, минусов больше. Прежде всего, это повышение внутриглазного давления (ВГД) при длительном их использовании, замедление регенерации и как следствие, возникновение трофических язв роговицы, ухудшение течения вирусных заболеваний, поскольку возникает иммуносупрессия, помутнение хрусталика, так называемая «стероидная» катаракта, как правило, при пероральном применении стероидных препаратов, также возможно помутнение стекловидного тела и нарушение аккомодации.
На рис. 1 как пример показаны формулы стероидов, которые вырабатываются собственно в организме, и какой процесс происходит, пока они достигают конечной точки. Это сложные биохимические реакции, занимающие достаточно долгое время и требующие больших энергетических затрат.
Нестероидные противовоспалительные препараты. НПВС ингибируют циклооксигеназный (ЦОГ) путь, препятствуя образованию простагландинов, которые являются основным фактором развития воспалительного процесса после хирургического вмешательства, в основном по поводу катаракты и развития кистозного макулярного отека (КМО).
Сочетанное применение кортикостероидов и НПВС показало синергическое взаимодействие, поскольку места приложения у этих групп препаратов разные.
Стойкий миоз способен существенно осложнить работу хирурга в ходе операции по удалению катаракты, затрудняя ход хирургической процедуры.
Всем хирургам хорошо известна ситуация, представленная на рис. 2.
Несмотря на применение мидриатиков, проведение хирургом всех возможных технических приемов, зрачок остается узким, и это осложняет всю дальнейшую работу. Применяются различные устройства, которые помогают справиться с мидриазом, но механическое воздействие достаточно травматично для радужки и осложняет течение послеоперационного процесса. Применение до операции НПВС способно существенно помочь в уменьшении интраоперационного миоза.
Вторая точка приложения – это лечение воспаления. НПВС часто назначаются совместно со стероидами для лечения воспалительного процесса, спровоцированного оперативным лечением глаз. Стероиды регулируют экспрессию клеточных белков, что ведет к снижению метаболизма арахидоновой кислоты и, как следствие, к снижению синтеза простагландинов, которые являются основными в этом процессе.
Третья точка приложения – это предупреждение КМО. КМО является самой частой причиной снижения зрения после рутинных операций по удалению неосложненной катаракты. По оценкам ряда авторов, возникает у 12% пациентов из группы низкого риска, перенесших хирургию катаракты.
Развитие КМО обуславливается нарушением внутреннего гематоретинального барьера из-за воздействия простагландинов.
Факторы риска возникновения КМО:
• предшествующее воспаление глаза;
• проблемы с эпиретинальной или витреоретинальной мембраной;
• диабетическая ретинопатия;
• сосудистые болезни глаз или сердечно-сосудистые заболевания;
• наличие в анамнезе пигментного ретинита.
У пациентов, подверженных повышенному риску возникновения КМО, профилактическое лечение необходимо начать раньше и продолжать на протяжении более длительного периода времени.
На рис. 3 показаны тракции витреомакулярной зоны, которые очень часто трудно диагностировать при осмотре глазного дна, тем более, если у пациента имеется серьезное помутнение хрусталика.
Все это приводит к развитию патологии в центральном отделе. Сами по себе нестероидные средства, конечно, такие тракции не убирают, и требуется последующая витреоретинальная хирургия.
«Терапевтическое» решение этой проблемы представила компания Алкон, впервые продемонстрировав препарат JETREA (OCRIPLASMIN).
Первое именно фармакологическое лечение витреомакулярных тракций у взрослых, включая пациентов с макулярными отверстиями менее 400m. Вводится он интравитреально и как фермент позволяет убрать тракции из витреомакулярной зоны.
Как правильно применять НПВС?
Адекватное применение НПВС максимизирует эффективность лечения и минимизирует осложнения (рис. 4-5). Адекватное применение подразумевает применение в течение 4-х недель после операции по удалению катаракты для профилактики КМО с ограничением применения у пациентов с поврежденной роговицей. Это особенно актуально для пациентов, перенесших ФРК.
Также их нужно с осторожностью применять у пациентов с выраженным синдромом «сухого глаза». НПВС после рефракционных операций используются в первую очередь для обеспечения анальгезирующего эффекта, использование после операции должно быть немедленным и не должно применяться в течение всего процесса заживления эпителиальных ран.
Хотелось бы остановиться на том, что нового в этом направлении мы сегодня получили для клинической практики. Офтальмологическая суспензия непафенака 0.1%, коммерческое название НЕВАНАК®. Показанием является лечение боли и воспаления после хирургии катаракты. Режим дозирования: одна капля 3 раза в день за день до операции, в день хирургического вмешательства и в течение 14 дней после него. Это первое и единственное нестероидное пролекарство для применения в офтальмологии.
В состав входит консервант: 0.005% бензалкония хлорид. К сожалению, без консерванта обойтись нельзя, но тем не менее компании удалось поддержать физиологическое значение pH: 7.4, поэтому неприятных ощущений от применения данного препарата у пациента нет.
Что такое пролекарство? Это такое «модное» понятие, которое на самом деле известно в медицине с давних пор. Начало было положено Буссом в 1875 г., когда был применен салицилат Na в лечении ревматических синдромов. Сам по себе салицилат Na был достаточно агрессивен, вызывая язвенные поражения ЖКТ. Чтобы избежать таких осложнений, Дрессером в 1899 г., т.е. почти 20 лет спустя, было получено пролекарство – ацетилсалициловая кислота, которую мы до сих пор успешно применяем. Еще один пример пролекарства. Paul Ehrlich в 1909 г. предлагает сольварсан – это суспензия, которая применялась при лечении сифилиса. Препарат содержал мышьяк. От этого препарата были тяжелые токсические последствия. Carl Voegtlin в 1925 г. предложил препарат мафарсен, который также являлся пролекарством и не имел таких тяжелых патологических последствий на организм и успешно применялся вплоть до наступления эры антибиотиков.
На рис. 6 показана пролекарственная структура и ее метаболическая трансформация. Непафенак преобразуется в мощный ингибитор фермента циклооксигеназы амфенак гидролазами глазной ткани .
Сам по себе непафенак достаточно мягкий препарат, но с помощью гидролазы глазной ткани превращается в мощный блокатор циклооксигеназной системы. Поскольку препарат работает вместе с гидролазами глазной ткани, он самостоятельно оптимизирует свое действие: при введении в глаз непафенак метаболизируется внутриглазными тканями, т.е. он проходит роговицу, попадает в радужку и цилиарное тело, затем также беспрепятственно проникает в задний отрезок глаза.
Итак, пролекарственная формула нового поколения минимизирует возникновение токсичности, и главное, на что бы я хотел обратить внимание, это минимальная системная абсорбция, в 1700 раз меньше разовой пероральной дозы, когда наступает клинический эффект.
На рис. 7 показана скорость проникновения непафенака в роговицу по сравнению с другими известными препаратами, например, с часто встречающимся на рынке диклофенаком. По шкале см/с видно, что он проникает быстрее почти в 3 раза, сильно опережая по проницаемости все остальные препараты.
Эффективность в передней камере глаза. В 2000 г. было проведено Gamache D.A. исследование по оценке противовоспалительного эффекта непафенака 0.1% в сравнении с диклофенаком 0.1%. Результаты представлены на рис. 8. Это продукция простагландинов в радужке и цилиарном теле новозеландских кроликов-альбиносов после разовой местной дозы. Видно, как непафенаком подавляется продукция простагландинов в отличие от диклофенака.
Также была проведена оценка противовоспалительной эффективности среди пациентов, проходящих хирургию катаракты. На рис. 9 показан процент клинического выздоровления при осмотре на 1, 3, 7, 14-й дни после операции. Оранжевые столбики – это группа плацебо, желтые – пациенты, получавшие суспензию Неванак®. Практически все (90% случаев) имели клиническое выздоровление уже на 14-е сутки в отличие от групп плацебо (около 30%).
На рис. 10 показан процент пациентов без жалоб на боль в послеоперационном периоде. Уже на первый день после операции группа пациентов, получавших непафенак, в 2 раза превышала результаты группы плацебо. На 3-й день боль исчезла у 90% пациентов, получавших непафенак в отличие от контрольной группы.
На заднем отрезке глаза также было проведено исследование, было показано мощное ингибирующее действие. Препарат направленно воздействует на циклооксигеназу внутриглазной ткани (COX-1: конституционный синтез тромбоцитами; COX-2: индуцированный цитокином (ИЛ-1(3)), воздействуя на все зоны гематоофтальмического барьера.
Метаболический путь этого препарата схож с метаболизмом арахидоновой кислоты. Он одинаково ингибирует все простагландины (PGE2, PG12) радужки и цилиарного тела ( PGF2g, PGA1, PGD2), подавляет синтез простагландина E2 (PGE2) в сетчатке и ингибирует нарушение гематоретинального барьера.
Оценивалась эффективность этого препарата и в профилактике отека сетчатки, способность местных форм непафенака, кеторолака и диклофенака предотвращать развитие индуцированного отека сетчатки.
На рис. 11 показано сокращение количества протеинов в стекловидном теле в сравнении с группой контроля. Нельзя сказать, что диклофенак или кеторолак в данном случае не работают. Работают, но гораздо менее эффективней по сравнению с группой, получающей непафенак. И уменьшение количества PGE2 в стекловидном теле также показывает, что это средство почти в 200 раз эффективней диклофенака (рис. 12).
Хочу рассказать о некоторых особенностях Неванака, которые мы получили, начав его применение в клинической практике. Прежде всего его необходимо хорошо встряхивать, поскольку это эмульсия. К сожалению, это чудо-лекарство применяется только у взрослых, т.е. с 18 лет. Не рекомендуется его применение во время беременности и лактации, поскольку таких исследований не проводилось. Также нужно обратить внимание на пациентов, принимающих ТРОМБО АСС. Это достаточно большая группа, особенно пожилых пациентов с сердечно-сосудистыми заболеваниями, поскольку может быть некий синергизм воздействия этих препаратов. Также с Рис. 9. Процент клинического выздоровления при каждом осмотре Рис. 10. Процент пациентов без жалоб на боль осторожностью надо применять этот препарат пациентам с синдромом «сухого глаза». Но для таких пациентов у компании Алкон есть неплохая линейка препаратов, которая позволяет бороться и с этим недугом. Также среди некоторых особенностей неванака хотелось бы отметить противодействие между хорошо известными противоглаукомными средствами простагландинового ряда и нашим противовоспалительным препаратом. Кто кого победит, сказать трудно, но в своей практике мы стараемся некоторое время избегать применения таких препаратов у пациентов, которые готовятся к катарактальной хирургии, но потом назначаем снова, как правило, повышения давления за это время не возникает.
Выводы:
• В клиническую практику вошел новый препарат в виде пролекарственной формы;
• На до– и постмаркетинговом этапе проведены многочисленные плацебоконтролируемые исследования, доказавшие его высокую проницаемость, прицельность действия, эффективность и безопасность;
• Высокоэффективен в противовоспалительной терапии, купировании болевого синдрома, поддержании мидриаза во время ФЭК, профилактике и купировании КМО;
• Хорошо сочетается со стероидными противовоспалительными средствами;
• Доступен для поликлинической и стационарной практики.
Источник
