Делать при воспалении кишечника
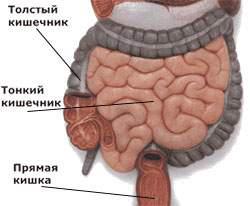
Кишечник является частью желудочно-кишечного тракта человека. Он состоит из двенадцатиперстной кишки, тонкого и толстого кишечника. Основная его функция – это переваривание пищи с помощью пищеварительных ферментов до более простых соединений и их всасывание в кровь. Различные факторы могут приводить к нарушению функции слизистой оболочки кишечника и ее воспалению.

Воспаление кишечника представляет собой собирательный термин, который характеризует наличие воспалительного процесса в слизистой оболочке одного или нескольких отделов кишечника. По частоте это состояние занимает 2-е место от всех болезней желудочно-кишечного тракта, с одинаковой частотой встречается у людей обоих полов и всех возрастных категорий
Причины возникновения
Воспаление в кишечнике может развиваться в результате воздействия множества различных причин, для удобства все они разделены на несколько основных групп:
• инфекции – воспаление вызывают бактерии (кишечная палочка, сальмонеллы, шигеллы), вирусы (ротавирус) или простейшие (амебная дизентерия);
• паразитирование гельминтов (глистов);
• аутоиммунные процессы – состояние, при котором иммунная система воспринимает клетки слизистой оболочки кишечника как чужеродные и вырабатывает антитела к ним, которые и вызывают воспаление (неспецифический язвенный колит, болезнь Крона);
• генетическая предрасположенность – некоторые воспалительные заболевания кишечника и врожденная недостаточность пищеварительных ферментов передаются наследственно от родителей детям;
• погрешности в диете – переедание, злоупотребление жирной, копченой, жареной, острой пищей может приводить к воспалению любого участка желудочно-кишечного тракта, особенно его верхних отделов – двенадцатиперстной кишки и тонкого кишечника;
• недостаточное кровообращение в сосудах стенок кишечника в результате атеросклеротических изменений и сужения артериального русла;
• нарушение нормальной микрофлоры кишечника – преобладание условно-патогенной флоры приводит к воспалительным процессам в слизистой оболочке.
Механизм развития воспаления связан с тем, что в результате воздействия повреждающего фактора, происходит гибель клеток слизистой оболочки, усиливается кровоснабжение участка (гиперемия), возникает боль и нарушение функции (клетки воспаленного участка не секретируют ферменты, прекращается всасывание питательных веществ).
Классификация
Воспаление кишечника разделяется на несколько видов, в зависимости от локализации воспаления, длительности процесса и причин возникновения.
По локализации процесса воспаление кишечника разделяется на такие виды:
1. воспаление 12-перстной кишки (дуоденит) – процесс развивается в начальном отделе тонкого кишечника, отдельно выделяют воспаление луковицы двенадцатиперстной кишки (место перехода желудка в тонкий кишечник);
2. воспаление тонкого кишечника (энтерит) – может быть воспаление на ограниченном участке, но чаще бывает на протяжении всего тонкого кишечника;
3. воспаление толстого кишечника (колит) – бывает как при инфекциях, так и при аутоиммунных процессах, воспаление обычно возникает на протяжении всего толстого кишечника.
По длительности процесса выделяют:
• острое воспаление – период времени, при котором развивается воспаление, не превышает 1-го месяца;
• хроническое воспаление – процесс длится от полугода и дольше.
По причинному фактору все воспалительные процессы в кишечнике разделяются на 2 группы:
• инфекционные – причиной является любой инфекционный возбудитель (чаще всего бактерии), эти воспалительные процессы еще называются острыми кишечными инфекциями;
• неинфекционные – все остальные причинные факторы (аутоиммунные процессы, наследственные генетические факторы, погрешности в диете, и пр.).
Симптомы воспаления кишечника
Для воспалительных заболеваний кишечника характерны ряд общих симптомов, которые не зависят от локализации процесса и причин возникновения:
• боль в животе – характер давящий или распирающий, без четкой локализации, возникновение боли связано со спазмом гладких мышц стенок кишечника;
• тошнота – указывает на воспаление тонкого кишечника или двенадцатиперстной кишки, возникает после употребления пищи;
• рвота – бывает при воспалении в верхних отделах кишечника после приема пищи, обычно ровота приносит облегчение;
• вздутие живота – обусловлено повышенным образованием газов вследствие недостаточности пищеварительных ферментов при воспалении в тонком кишечнике;
• неустойчивый стул – может быть послабление стула, вплоть до развития диареи (острая кишечная инфекция), воспаление толстого кишечника чаще сопровождается склонностью к запорам;
• похудание – результат недостаточного всасывания питательных веществ из тонкого кишечника;
• анемия (малокровие) – снижение содержания гемоглобина в крови вследствие недостаточного поступления железа в организм из воспаленного кишечника.
Диагностика заболеваний
Диагностика проводится для уточнения диагноза, причины и локализации воспаления. Для этого используются такие дополнительные методы лабораторного и инструментального обследования:
• клинический анализ крови – повышение скорости оседания эритроцитов (СОЭ) и количества лейкоцитов позволяет заподозрить наличие воспалительного процесса в организме;
• копрограмма – лабораторное исследование кала дает возможность оценить функцию кишечника, выявить недостаточность пищеварительных ферментов (по непереваренным остаткам пищевых волокон);
• бактериологическое исследование кала – исследование кала на наличие бактерий, их идентификации и определения чувствительности к антибиотикам для выбора адекватного лечения;
• фиброэзофагогастродуоденоскопия (ФЭГДС) – эндоскопическое обследование слизистой оболочки желудка и двенадцатиперстной кишки с помощью оптоволоконной трубки с камерой и освещением, при необходимости есть возможность взять кусочек слизистой оболочки для гистологического исследования (биопсия);
• колоноскопия – принцип тот же, что и ФЭГДС, только датчик вводится не через рот, а через задний проход, обследуется толстый кишечник, оценивается состояние слизистой оболочки, локализация воспаления;
• видеокапсульная эндоскопия – современный метод обследования кишечника, при котором пациент проглатывает капсулу с освещением и камерой, капсула проходит через все отделы кишечника в течении суток, информация передается посредством радиоволн на компьютер, позволяет оценить состояние слизистой оболочки всего кишечника.
Чем и как лечить воспаление кишечника?
Лечение воспаления кишечника является комплексным и включает несколько направлений в терапии:
• Этиотропная терапия направлена на исключение причины воспаления. Для уничтожения бактерий используются антибиотики. Иммунодепрессанты (препараты, снижающие активность иммунной системы) необходимы при аутоиммунном воспалении. Для уничтожения гельминтов принимаются противоглистные средства – пиперазин, альбендазол.
• Диета при воспалении кишечника является основополагающим фактором в успешном лечении, используется меню, которое максимально снижает нагрузку на воспаленную слизистую оболочку. Рекомендуются такие продукты – нежирные сорта мяса, курица, овощи и фрукты, черный хлеб, нежирные молочные продукты. Все блюда готовятся на пару или варятся, их нельзя жарить, коптить или готовить на открытом огне.
• Патогенетическая терапия используется для того, чтобы снять воспаление, применяются противовоспалительные средства и сорбенты, которые связывают токсины, находящиеся в просвете кишечника. Для уменьшения нагрузки на кишечник и создания функционального покоя, используются ферментные препараты, которые содержат пищеварительные ферменты – панкреатин, мезим.
• Симптоматическая терапия помогает облегчить состояние больного, снять болевые ощущения с помощью спазмолитиков (препараты, снимающие спазм кишечника – но-шпа), обезболивающие. Для уменьшения вздутия принимают пеногасители – эспумизан.
Следует помнить, что в большинстве случаев хроническое воспаление тонкого кишечника может быть вызвано погрешностями в диете, поэтому рекомендации в отношении питания полезны не только для лечения, но и для профилактики воспаления кишечника.
Источник
Лечение воспалительных заболеваний кишечника
Несколько классов медицинских препаратов эффективны при лечении воспалительных заболеваний кишечника. Детали их выбора и использования обсуждаются в отношении каждого заболевания.
5-аминосалициловая кислота
(5-АСК, месаламин). 5-АСК блокирует продукцию простагландинов и лейкотриенов и оказывает другие благоприятные эффекты на воспалительный каскад. Поскольку 5-АСК активна только внутри просвета кишечника и быстро абсорбируется в проксимальных отделах тонкой кишки, это должно быть учтено для создания условий замедленной абсорбции при пероральном приеме. Сульфасалазин, оригинальный препарат в этом классе, задерживает абсорбцию комплекса 5-АСК с сульфагруппой сульфапиридина. Комплекс расщепляется бактериальной флорой в терминальных отделах подвздошной и толстой кишки, освобождая 5-АСК. Сульфагруппа, однако, вызывает многочисленные нежелательные эффекты (напр., тошноту, диспепсию, головную боль), нарушает абсорбцию фолиевой кислоты и, иногда, вызывает тяжелые неблагоприятные реакции (напр., гемолитическую анемию и агранулоцитоз и, редко, гепатит или пневмонит).
Обратимое снижение в сперме количества сперматозоидов и их подвижности наблюдается у 80 % мужчин. При использовании сульфасалазина его необходимо принимать с пищей, первоначально в низкой дозировке (напр., 0,5 г перорально 2 раза в день) и постепенно увеличивать дозу в течение нескольких дней до 1-2 г 2-3 раза в день. Пациенты должны дополнительно ежедневно принимать перорально 1 мг фолата и контролировать общий анализ крови и печеночные тесты каждые 6-12 месяцев.
Более современные препараты, состоящие из комплекса 5-АСК с другими транспортными средствами, также эффективны, но обладают меньшими неблагоприятными эффектами. Олсалазин (димер 5-АСК) и балсалазин (5-АСК, конъюгированная с неактивным компонентом) расщепляются бактериальной азоредуктазой (как и сульфасалазин). Эти препараты активируются главным образом в толстой кишке и менее эффективны при поражениях проксимальных отделов тонкой кишки. Дозировка олсалазина составляет 500-1500 мг 2 раза в день и балсалазина – 2,25 г 3 раза в день. Олсалазин иногда вызывает диарею, особенно у пациентов с панколитом. Эта проблема минимизируется постепенным увеличением дозы и приемом препарата с пищей.
Другие формы 5-АСК предусматривают покрытия для задержки выхода препарата. Асакол (обычная доза 800-1200 мг 3 раза в день) представляет собой 5-АСК, покрытую акриловым полимером, рН растворимость которого задерживает выход препарата до дистального отдела подвздошной и толстой кишки. Пентаза (1 г 4 раза в день) представляет собой 5-АСК, заключенную в капсулу из микрогранул этилцеллюлозы, и в тонкой кишке освобождается только 35% препарата. Вторичный острый интерстициальный нефрит из-за применения месаламина развивается редко; желателен периодический контроль функции почек, так как в большинстве случаев нарушения обратимы при своевременном выявлении осложнения.
При проктитах и поражении левой половины толстой кишки возможно применение 5-АСК в форме суппозиториев (500 мг 2-3 раза в день) или в виде клизм (4 г перед сном или 2 раза в день). Ректальное применение препарата эффективно при остром течении заболевания и длительном использовании и может быть целесообразным в комбинации с пероральным приемом 5-АСК.
[27], [28], [29], [30], [31], [32], [33], [34], [35], [36], [37], [38], [39], [40]
Глюкокортикоиды
Глюкокортикоиды показаны в острых случаях большинства форм воспалительных заболеваний кишечника, если препаратов 5-АСК недостаточно, но они не предназначены для поддерживающего лечения. В тяжелых случаях используется внутривенно гидрокортизон 300 мг/день или метилпреднизолон 60-80 мг/день непрерывно капельно или разделенными дозами; при средней степени тяжести можно применять перорально преднизолон или преднизолон 40-60 мг 1 раз в день. Лечение воспалительных заболеваний кишечника продолжается до исчезновения симптомов (обычно 7-28 дней) и доза снижается постепенно с 5 до 10 мг еженедельно до 20 мг 1 раз в день с последующим снижением с 2,5 до 5 мг еженедельно с назначением поддерживающей терапии 5-АСК или иммуномодуляторами. Неблагоприятные эффекты кратковременной терапии глюкокортикоидами в высоких дозах включают гипергликемию, гипертонию, бессонницу, повышенную активность и острые эпизоды психотических расстройств.
Клизмы с гидрокортизоном или орошения могут использоваться при проктитах и поражении левого фланга толстой кишки; в виде клизмы вводится 100 мг препарата в 60 мл изотонического раствора 1-2 раза в день. Этот состав следует задержать в кишке как можно дольше; инстилляции перед сном при положении пациента на левом боку с приведенными к животу бедрами позволяют пролонгировать время задержки раствора и увеличить зону воздействия. В случае эффективности ежедневное лечение должно быть продлено приблизительно на 2-4 недели, затем через день в течение 1-2 недель с последующей постепенной отменой в течение более чем 1-2 недель.
Будезонид – глюкокортикоид с высоким (> 90%) метаболизмом в печени в течение первого цикла; таким образом, пероральное применение может иметь существенный эффект на заболевание ЖКТ, но минимальный супрессивный эффект на надпочечники. Пероральное применение будезонида имеет меньше неблагоприятных эффектов, чем преднизолон, но он не столь эффективен и обычно используется в менее тяжелых случаях заболевания. Его дозировка – 9 мг 1 раз в день. Его применение также доступно за пределами США, как и клизма. Как и другие глюкокортикоиды, будезонид не рекомендован при длительном применении.
Иммуномодулирующие препараты
Азатиоприн и его метаболит 6-меркаптопурин ингибируют функцию Т-клеток. Они эффективны при длительном применении и могут уменьшать потребность в глюкокортикоидах и поддерживать ремиссию в течение многих лет. Для достижения клинического эффекта часто необходимо применение этих препаратов в течение 1-3 месяцев, поэтому глюкокортикоиды не могут быть исключены из лечения, по крайней мере, 2 месяца. Обычная дозировка азатиоприна 2,5-3,0 мг/кг перорально 1 раз в день и 6-меркаптопурина 1,5-2,5 мг/кг перорально 1 раз в день, но дозировка индивидуально может варьировать в зависмости от метаболизма. Признаки супрессии костного мозга должны регулярно контролироваться подсчетом лейкоцитов (каждые две недели в 1-м месяце, затем каждые 1-2 месяца). Панкреатит или высокая лихорадка наблюдаются приблизительно у 3-5% пациентов; любое из них является абсолютным противопоказанием к повторному применению. Гепатотоксичность развивается более редко и может контролироваться биохимическими анализами крови каждые 6-12 месяцев.
У ряда пациентов, нечувствительных к глюкокортикоидам, может быть успешным применение метотрексата перорально, внутримышечно или подкожно в дозе 15-25 мг, и даже у тех пациентов, которые были нечувствительны к азатиоприну или 6-меркаптопурину. Характерны тошнота, рвота и бессимптомные изменения функциональных печеночных тестов. Пероральное применение фолата 1 мг 1 раз в день может уменьшить некоторые из неблагоприятных эффектов. Употребление алкоголя, тучность и диабет являются факторами риска развития гепатотоксичности. Пациентам с этими факторами риска необходимо выполнить биопсию печени после полной дозы 1,5 г.
Циклоспорин, который блокирует активацию лимфоцитов, может быть эффективным у пациентов с тяжелым течением язвенного колита, нечувствительного к глюкокортикоидам и требующего колэктомии. Его применение абсолютно показано у пациентов с болезнью Крона и неподдающимися лечению свищами или пиодермией.
Начальная доза – 4 мг/кг внутривенно 1 раз в день; при эффективности пациентов переводят на пероральный прием 6-8 мг/кг 1 раз в день и затем быстро переводят на азатиоприн или 6-меркаптопурин. Многочисленные неблагоприятные эффекты (напр., почечная токсичность, приступы эпилепсии, оппортунистические инфекции) являются противопоказанием к длительному применению препарата (> 6 месяцев). В целом пациентам не предлагают лечение циклоспорином, если нет причины избежать более безопасного метода лечения, чем колэктомия. При применении препарата его уровни в крови должны сохраняться между 200-400 нг/мл и при этом рассматриваться как профилактика Pneumocystis jiroveci (ранее именовалась P. carinii). Такролимус – иммунодепрессант, используемый в трансплантологии, так же эффективен, как и циклоспорин.
Антицитокиновые препараты
Инфликсимаб, CDP571, CDP870 и адалимумаб являются антителами против TNF. Натализумаб является антителом против молекулы адгезии лейкоцита. Эти вещества могут быть эффективными при болезни Крона, но их эффективность при ЯК неизвестна.
Инфликсимаб применяется в режиме отдельной внутривенной инфузии в дозе 5 мг/кг в течение 2 часов. Некоторые клиницисты начинают лечение с параллельного назначения 6-меркаптопурина, используя инфликсимаб в качестве поддерживающего препарата, пока эффективность основного медикамента не достигнет наибольшей активности. Плавное снижение дозы глюкокортикоида можно начать через 2 недели. При необходимости повторные введения инфликсимаба можно повторять каждые 8 недель. Неблагоприятные эффекты включают отсроченные реакции гиперчувствительности, головную боль и тошноту. Несколько пациентов погибли от сепсиса после использования инфликсимаба, поэтому генерализованная бактериальная инфекция является противопоказанием к применению препарата. Кроме того, на фоне применения этого препарата зарегистрирована реактивация туберкулеза; поэтому перед назначением препарата необходимо выполнение туберкулиновой пробы с PPD и рентгенографии органов грудной клетки.
Талидомид снижает продукцию aTNF и интерлейкина 12 и в некоторой степени подавляет ангиогенез. Препарат может быть эффективным при болезни Крона, но тератогенность и другие неблагоприятные эффекты (напр., сыпь, гипертония, нейротоксичность) ограничивают его применение пока только научными исследованиями. Изучается эффективность других антицитокинов.антиинтегриновых антител и факторов роста.
[41], [42], [43], [44], [45], [46], [47], [48], [49], [50], [51]
Антибиотики и пробиотики
Антибиотики эффективны при болезни Крона, но их применение ограничено при язвенном колите. Метронидазол в дозе 500-750 мг перорально 3 раза в день в течение 4-8 недель купирует проявления заболевания при средней степени тяжести и достаточно эффективен при развитии свищей. Однако неблагоприятные эффекты (особенно нейротоксичность) могут препятствовать полному курсу лечения. Ципрофлоксацин в дозе 500-750 мг перорально 2 раза в день оказывается менее токсичным. Некоторые эксперты рекомендуют комбинированное применение метронидазола и ципрофлоксацина.
Различные непатогенные микроорганизмы (напр., комменсал Escherichia coli, Lactobacillus species, Saccharomyces) каждодневно используются как пробиотики и могут быть эффективными в профилактике синдрома воспаления илео-анального резервуара (pouchitis syndrom), но все же должна быть ясно определена и другая их роль в лечении.
[52], [53], [54], [55], [56], [57], [58], [59], [60], [61], [62], [63], [64], [65], [66]
Заместительная терапия
Большинство пациентов и их семьи волнует режим питания и влияние стресса. Хотя имеются единичные сообщения о клиническом эффекте определенных диет, включая одну с жестким ограничением углеводов, контрольные исследования не доказали какой-либо эффективности. Исключение стрессовых перегрузок может быть эффективным.
Источник
