Для изменения углеводного обмена в очаге воспаления характерно
На начальном этапе воспаления в ткани (не только зоны первичной, но и вторичной альтерации) преобладают реакции катаболизма, затем – при развитии артериальной гиперемии и активации процессов пролиферации, как правило, начинают доминировать анаболические реакции.
Углеводный обмен: в очаге воспаления метаболизм углеводов претерпевает характерные изменения, выражающиеся в преобладании гликолиза и развитии ацидоза.
Проявления
увеличение поглощения тканью кислорода при одновременном снижении эффективности окисления глюкозы в процессе тканевого дыхания;
активация гликогенолиза и гликолиза;
уменьшение уровня АТФ в ткани;
накопление избытка лактата и пирувата.
Липидный обмен: обмен липидов в очаге воспаления характеризуется доминированием липолиза над реакциями их синтеза.
Проявления
активация процессов липолиза и накопление продуктов липолиза
торможение реакций синтеза липидов
активация перекисного окисления липидов и накопление перекисей и гидроперекисей липидов
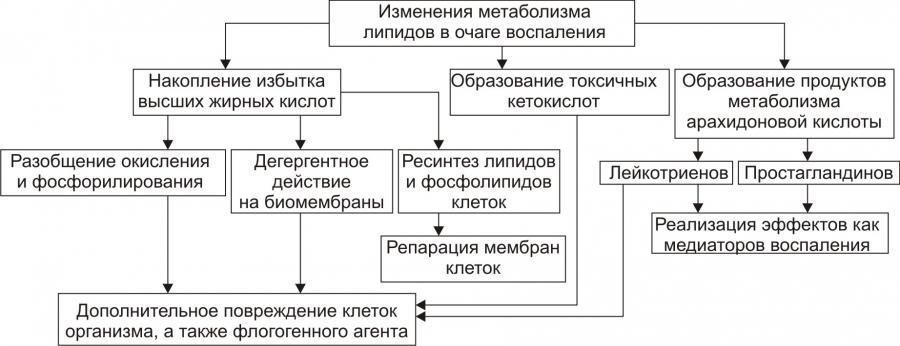
Рис. 7. – Изменения метаболизма липидов в очаге воспаления
(по П.Ф. Литвицкому, 2002)
Белковый обменхарактеризуется преобладанием протеолиза над процессами протеосинтеза.
Проявления
активация процессов протеолиза и накопление продуктов протеолиза.
торможение реакций протеосинтеза.
денатурация молекул белка (образование аутоантигенов).
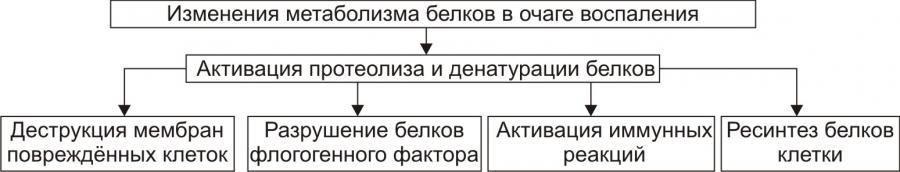
Рис. 8. – Изменения метаболизма белков в очаге воспаления (по П.Ф. Литвицкому, 2002)
Обмен ионов и воды
Для ионов и воды характерен трансмембранный дисбаланс ионов, увеличение внутриклеточного содержания Na+иCa2+и внеклеточного содержанияK+и Mg2+, гипергидратация клеток и отёк ткани в очаге воспаления.
Проявления
нарушения распределения ионов по обе стороны плазмолеммы; происходит потеря клеткой K+,Mg2+, микроэлементов и накопление их в межклеточной жидкости. В клетку же поступаютNa+,Ca2+и некоторые другие ионы.
нарушения соотношения между отдельными ионами как в клетке, так и вне клетки в результате расстройства механизмов трансмембранного переноса ионов.
гипергидратация ткани в очаге воспаления в связи с высокой гидрофильностью накапливающихся в нём Na+иCa2+, а также продуктов гидролиза органических соединений.
высвобождение дополнительного количества катионов (K+,Na+,Ca2+, железа, цинка) при гидролизе солей, распаде гликогена, белков и др. органических соединений, а также клеточных мембран.
выход большого количества Ca2+из повреждённых внутриклеточных депо (митохондрий и цистерн эндоплазматической сети и митохондрий).
Медиаторы воспаления
В ходе первичной и вторичной альтерации высвобождаются большие количества разнообразных медиаторов и модуляторов воспаления.
Медиаторы воспаления – БАВ, образующиеся при воспалении, обеспечивающие закономерный характер его развития и исходов, формирование местных и общих признаков. По происхождению делятся на гуморальные (образующиеся в жидких средах – плазме крови и тканевой жидкости) иклеточные. Всегуморальные медиаторы являются предсуществующими, т.е. имеются в виде предшественников до активации последних (производные комплемента, кинины и факторы свертывающей системы крови).Среди клеточных медиаторов выделяют предсуществующие (депонированные в клетках в неактивном состоянии) – вазоактивные амины, лизосомальные ферменты, нейропептиды, ивновь образующиеся (т.е. продуцируемые клетками при стимуляции) – эйкозаноиды, цитокины, лимфокины, активные метаболиты кислорода (таб. 2-4).
Таблица 2. Клеточные предшествующие медиаторы воспаления
Основные группы | Основные медиаторы | Основные источники | Основные эффекты |
Вазоактивные амины | Гистамин | Базофилы Тучные клетки Тромбоциты | Вазодилятация Повышение проницаемости сосудов Спазм гладкой мускулатуры |
Серотонин | Тромбоциты | Зуд Угнетение гранулоцитов Стимуляция моноцитов-макрофагов и фибробластов | |
Лизосомальные факторы | Протеиназы | Гранулоциты Моноциты-макрофаги | Тканевая деструкция Усиление эмиграции и фагоцитоза Стимуляция моноцитов-макрофагов и фибробластов Пролиферация и активация лимфоцитов |
Неферментные катионные белки | Гранулоциты | Микробицидность Повышение проницаемости сосуда Дегрануляция тучных клеток Адгезия и эмиграция лейкоцитов | |
Нейропептиды | Вещество Р Кальцитонин-генродственный пептид Нейрокинин А | С-волокна афферентных нейронов | Вазодилятация Повышение проницаемости сосудов Дегрануляция тучных клеток Спазм гладкой мускулатуры |
Нейромедиаторы | Ацетилхолин | Холинергические нейроны | Вазодилятация Спазм гладкой мускулатуры Стимуляция лейкоцитов |
Таблица 3. Клеточные, вновь образующиеся, медиаторы воспаления
Основные группы | Основные медиаторы | Основные источники | Основные эффекты |
Производные арахидоновой кислоты (эйкозаноиды) | Простагландины | Моноциты-макрофаги Гранулоциты Тромбоциты | Активация лейкоцитов Вазодилятация Боль |
Тромбоксаны | Моноциты -макрофаги Гранулоциты Тромбоциты | Агрегация тромбоцитов Спазм гладкой мускулатуры Активация гранулоцитов | |
Лейкотриены Гидроокси- и гидропер-оксиэйкозатетраеновые кислоты Липоксины | Моноциты-макрофаги Гранулоциты Тромбоциты | Активация лейкоцитов Повышение проницаемости сосудов (ЛTC4, D4, E4) Вазодилятация Спазм гладкой мускулатуры (ЛTC4, D4, E4, липоксины) | |
Фосфолипиды | Фактор, активирующий тромбоциты | Гранулоциты Тучные клетки Моноциты-макрофаги | Спазм гладкой мускулатуры Вазодилятация Повышение проницаемости сосудов Активация лейкоцитов Агрегация тромбоцитов |
Монокины | Интерлейкин-1 Фактор некроза опухоли | Моноциты-макрофаги | Активация лейкоцитов и других клеток Пролиферация и активация лимфоцитов Усиление фагоцитоз Стимуляция пролиферации и активации фибробластов Стимуляция тканевой деструкции |
Лимфокины | Фактор, активирующий макрофаги. Фактор, угнетающий макрофаги. Интерлейкин-2 | Т-лимфоциты | Активация и угнетение макрофагов Стимуляция гранулоцитов и лимфоцитов Активация естественных киллеров |
Активные формы кислорода | Супероксид-анион Гидроксил-анион Пергидроксил-анион Синглетный кислород Перекись водорода Гипохлорид | Гранулоциты Моноциты-макрофаги | Тканевая деструкция Активация гранулоцитов Стимуляция фагоцитоза Угнетение моноцитов |
Другие малые молекулы | Окись азота | Моноциты-макрофаги Гранулоциты | Тканевая деструкция Активация гранулоцитов |
Таблица 4. Гуморальные медиаторы воспаления
Основные группы | Основные медиаторы | Основные источники | Основные эффекты |
Производные комплемента | С5b-С9 С5а des Arg С5аС3а | Плазма Тканевая жидкость | Тканевая деструкция (С5b-С9) Активация лейкоцитов Повышение проницаемости сосудов (С5а, С3а) Дегрануляция тучных клеток (С5а, С3а) Спазм гладкой мускулатуры (С3а) |
Кинины | Брадикинин Каллидин | Плазма Тканевая жидкость | Вазодилятация Повышение проницаемости сосудов Спазм гладкой мускулатуры Угнетение гранулоцитов Стимуляция лимфоцитов и фибробластов Боль |
Факторы свертывающей системы крови | Фибринопеп-тиды Продукты деградации фибрина | Плазма | Активация лейкоцитов Усиление фагоцитоза |
Источник
Альтерационные процессы, нарушение обмена веществ и кровообращения в очагах воспаления вызывают ряд физико-химических изменений – ацидоз, гипертонию, дистонию, гиперосмию, гиперонкию и гипертермию.
Ацидоз
Ацидоз (H hiperjonija) очаг воспаления, возникающий в результате увеличения количества молочной и кетоновых кислот, плохо насыщенных кислородом промежуточных продуктов цикла Кребса (яблочная, янтарная и т. д.) и аминокислот. Первоначально буферная система ткани и воспалительный экссудат нейтрализуют кислотные соединения, образующиеся в тканевом метаболизме, и pH ткани не снижается – ацидоз компенсируется. Декомпенсированный ацидоз возникает при истощении буферной системы. PH экссудата снижается.
![]() Ацидоз и алкалоз
Ацидоз и алкалоз
Чем острее воспаление, тем сильнее выражен ацидоз. Особенно тяжелый ацидоз возникает при гнойном воспалении. В условиях хронического воспаления pH ткани обычно не опускается ниже 6,5 единиц, в то время как pH при остром гнойном абсцессе может упасть до 5,3. Наиболее выражен ацидоз в центре воспалительного очага, где он усиливает повреждение (альтерацию).
![]() Альтерация
Альтерация
До выделения биологически активных веществ изменения связаны только с ацидозом. Слабый ацидоз на периферии очага воспаления стимулирует пролиферацию. Следовательно, разрастание ткани происходит в направлении от периферии очага воспаления к центру. Этот пример показывает, что один и тот же фактор может работать двумя способами.
Гипериония и дизиония
Наряду с разрастанием ионов водорода в воспалительных очагах увеличивается количество ионов натрия, кальция и хлора, а в результате повреждения клеток – количество ионов калия и анионов фосфорной кислоты. В нормальных тканях концентрация ионов К не превышает 20 мг%, но в гнойном экссудате может достигать 100-200 мг%. Отношение K:Na к K:Ca увеличивается. Дизион в основном проявляется увеличением количества ионов К в воспалительной жидкости и крови, оттекающей от места воспаления.
Гиперосмия (осмотическая гипертензия)
Концентрация ионов в очаге воспаления увеличивается, в том числе при усилении диссоциации солей. Кроме того, в результате активных ферментативных процессов большие молекулы распадаются на более мелкие и концентрация молекул увеличивается. В процессе интенсивного гликолиза, липолиза и главным образом протеолиза выделяется:
- много аминокислот;
- органических кислот цикла Кребса;
- жирных кислот;
- молочной кислоты.
Концентрация молекул увеличивается в основном за счет аминокислот – когда одна молекула белка (аминокислотного полимера) разрушается, высвобождается много молекул аминокислот. В результате осмотическое давление в очагах воспаления резко повышается – в нормальных тканях оно составляет 7-8 атмосфер, но очаги воспаления могут увеличиваться вдвое и более.
Кроме того, наибольшее осмотическое давление находится в центре воспалительного процесса. Гиперосмии тканей играют важную роль в развитии экссудации и боли.
Гиперонкия
Повышение коллоидосмотического давления вызывается увеличением количества мелкодисперсных белков в тканях. В то же время белки плазмы, в основном альбумины, попадают в ткани из сосудов с повышенной проницаемостью стенки.
Онкотическое давление низкое (всего около 1% от осмотического), но оно играет важную роль в обмене жидкости между кровеносными сосудами и тканями – обычно белки плазмы не проходят через стенку сосудов и удерживают жидкость в крови.
При ацидозе гидрофильность белков тканей увеличивается, и они набухают. Экссудация вызывает местный воспалительный отек. Развивается один из основных местных признаков воспаления – опухоль. Отек опухших тканей вызывает боль.
![]() Отек и боль
Отек и боль
Гипертермия
Вызывает один из характерных признаков воспаления – жар. Если воспаление развивается на поверхности тела, например на коже, повышение температуры происходит главным образом из-за артериальной гиперемии. Гораздо более теплая артериальная кровь поступает в относительно низкотемпературную область тела. Однако температура тканей также повышается, когда воспаление локализуется на большой глубине, например, во внутренних органах.
Причиной локальной гипертермии считается разделение процессов биологического окисления и окислительного фосфорилирования. В результате энергия не накапливается в АТФ, а выделяется в виде тепла.
Роль нервной и эндокринной систем в развитии воспаления
Регуляторная роль нервной системы проявляется на всех стадиях воспаления. Например, воспалительная гиперемия и экссудация могут быть вызваны у человека, при убеждении, что монета, помещенная на кожу, горячая, хотя на самом деле монета холодная.
Анестезия тормозит развитие воспаления, но местная анестезия способствует созреванию очагов гноя. Состояние вегетативной нервной системы считается важным в развитии воспаления, однако воспаление также возникает в полностью денервированных тканях. Нарушения микроциркуляции в очаге воспаления возникают в результате локальных нервных процессов (аксональный рефлекс) и гуморальных влияний.
На развитие воспаления значительное влияние оказывают гормоны коры надпочечников. Поэтому кортикоиды дезоксикортикостерон и альдостерон также называют воспалительными гормонами. В фазе воспалительной гипергидратации они увеличивают проницаемость сосудистой стенки и более позднюю пролиферацию. Во время фазы гипогидратации обычно увеличивается выработка адренокортикотропного гормона и глюкокортикоидов.
Глюкокортикоиды (кортизон, гидрокортизон) – это так называемые противовоспалительные гормоны. Кортизон снижает активность гистидиндекарбоксилазы и увеличивает активность гистамина, тем самым снижая уровень гистамина. Одновременно снижается активность 5-окситриптаминдекарбоксилазы и, как следствие, продукция серотонина. В результате снижается проницаемость сосудистой стенки, подавляется гиперемия и экссудация.
![]() Глюкокортикоиды
Глюкокортикоиды
Из-за ингибирующего действия глюкокортикоидов на ферментные системы снижается энергетический потенциал клеток, деление и подвижность клеток (эмиграция лейкоцитов и фагоцитоз). Глюкокортикоиды стабилизируют лизосомные мембраны и инактивируют кислую фосфатазу, рибонуклеазу и другие ферменты. Глюкокортикоиды подавляют не только воспаление, но и защитные реакции организма – экссудацию, эмиграцию лейкоцитов, фагоцитоз, пролиферацию и образование антител.
Другие гормоны также влияют на течение воспаления. Давно известно, что воспаление активно у пациентов с гипертиреозом и инертно у пациентов с микседемой.
Инсулин регулирует не только углеводный обмен, но и метаболизм белков. При отсутствии инсулина сопротивляемость организма инфекционным агентам снижается, и воспаление протекает гораздо тяжелее. Фурункулез часто встречается у диабетиков.
Эстрогенные половые гормоны подавляют активность гиалуронидазы и течение воспаления.
Продолжение статьи
- Часть 1. Этиология и патогенез воспаления. Классификация.
- Часть 2. Особенности обмена веществ при воспалении.
- Часть 3. Физико – химические изменения. Роль нервной и эндокринной систем в развитии воспаления.
- Часть 4. Изменения в периферическом кровообращении при воспалении.
- Часть 5. Экссудация. Экссудат и транссудат.
- Часть 6. Эмиграция лейкоцитов. Хемотаксис.
- Часть 7. Фагоцитоз. Асептическое и острое воспаление.
- Часть 8. Распространение. Последствия. Принципы лечения воспаления.
Источник
Альтерация – это главное звено, по сути – пусковой механизм. Альтерация может быть первичная или вторичная. Первичная альтерация развивается сразу после воздействия повреждающего фактора и формируется на уровне функционального элемента органа. Первичная альтерация может проявляться специфическими изменениями, а также неспецифическими изменениями, которые развиваются стереотипно независимо от свойств и особенностей действия патогенного фактора. Эти изменения связаны:
1) с повреждением мембранных структур,
2) с повреждением мембраны митохондрий,
3) с повреждением лизосом.
Нарушения структуры мембраны клеток ведет к нарушению клеточных насосов. Отсюда теряется способность клетки адекватно реагировать изменением собственного метаболизма на изменения гомеостаза окружающей среды, изменяются ферментативные системы и митохондрии. В клетке накапливаются недоокисленные продукты обмена: пировиноградная, молочная и янтарная кислоты. Первоначально эти изменения являются обратимыми и могут исчезнуть, если этиологический фактор прекратил свое действие. Клетка полностью восстанавливает свои функции. Если же повреждение продолжается и в процесс вовлекаются лизосомы, то изменения носят необратимый характер. Поэтому лизосомы называют “стартовыми площадками воспаления” и именно с них начинается формирование вторичной альтерации.
Вторичная альтерация обусловлена повреждающим действием лизосомальных ферментов. Усиливаются процессы гликолиза, липолиза и протеолиза. В результате распада белков в тканях увеличивается количество полипептидов и аминокислот; при распаде жиров возрастают жирные кислоты; нарушения углеводного обмена ведет к накоплению молочной кислоты. Все это вызывает физико-химические нарушения в тканях и развиваются гиперосмия с повышением концентрации ионов K+, Na+, Ca2+, Cl-; гиперонкия – повышение количества белковых молекул из-за распада крупных на более мелкие; гипериония H+ – в связи с диссоциацией большого количества кислот с высвобождением ионов водорода. И как следствие всего этого – развивается метаболический ацидоз в связи с повышением кислых продуктов обмена. В процесс вовлекаются все компоненты ткани и альтерация носит необратимый характер, итогом которого будет аутолиз клеток. Образуются вещества, которые могут не только усиливать, но и ослаблять альтерацию, оказывая влияние на различные компоненты воспаления, т.е. регулируя микроциркуляцию, экссудацию, эмиграцию лейкоцитов и пролиферацию клеток соединительной ткани.
10. Нарушения микроциркуляции в очаге воспаления
Нарушение микроциркуляции в очаге воспаления характеризуется изменением тонуса микроциркуляторных сосудов, усиленным током жидкой части крови за пределы сосуда (т.е. экссудацией) и выходом форменных элементов крови (т.е. эмиграцией).
Для сосудистой реакции характерны 4 стадии:
1) кратковременный спазм сосудов,
2) артериальная гиперемия,
3) венозная гиперемия,
4) стаз.
Спазм сосудов возникает при действии повреждающего агента на ткани и связан с тем, что вазоконстрикторы возбуждаются первыми, поскольку они чувствительнее вазодилятаторов. Спазм длится до 40 секунд и быстро сменяется артериальной гиперемией. Артериальная гиперемия формируется следующими тремя путями: а) как результат паралича вазоконстрикторов; б) как результат воздействия медиаторов с сосудорасширяющей активностью; в) как результат реализации аксон-рефлекса.
Расслабляются прекапиллярные сфинктеры, увеличивается число функционирующих капилляров и кровоток через сосуды поврежденного участка может в десятки раз превышать таковой неповрежденной ткани.
Расширение микроциркуляторных сосудов, увеличение количества функционирующих капилляров и повышенное кровенаполнение органа определяет первый макроскопический признак воспаления – покраснение. Если воспаление развивается в коже, температура которой ниже температуры притекающей крови, то температура воспаленного участка повышается – возникает жар. Поскольку в первое время после повреждения линейная и объемная скорость кровотока в участке воспаления достаточно велики, то оттекающая из очага воспаления кровь содержит большее количество кислорода и меньшее количество восстановленного гемоглобина и поэтому имеет яркокрасную окраску. Артериальная гиперемия при воспалении сохраняется недолго (от 15 минут до часа) и всегда переходит в венозную гиперемию, при которой увеличенное кровенаполнение органа сочетается с замедлением и даже полным прекращением капиллярного кровотока.
Венозная гиперемия начинается с максимального расширения прекапиллярных сфинктеров, которые становятся нечувствительными к вазоконстрикторным стимулам и венозный отток затрудняется. После этого замедляется ток крови в капиллярах и приносящих артериолах. Главной причиной развития венозной гиперемии является экссудация – выход жидкой части крови из микроциркуляторного русла в окружающую ткань. Экссудация сопровождается повышением вязкости крови, периферическое сопротивление кровотоку возрастает, скорость тока крови падает. Кроме того, экссудат сдавливает венозные сосуды, что затрудняет венозный отток и также усиливает венозную гиперемию. Развитию венозной гиперемии способствует набухание в кислой среде форменных элементов крови, сгущение крови, нарушение десмосом, краевое стояние лейкоцитов, образование микротромбов. Кровоток постепенно замедляется и приобретает новые качественные особенности из-за повышения гидростатического давления в сосудах: кровь начинает двигаться толчкообразно, когда в момент систолы сердца кровь продвигается вперед, а в момент диастолы кровь останавливается. При дальнейшем повышении гидростатического давления кровь в систолу продвигается вперед, а в момент диастолы возвращается обратно – т.е.возникает маятникообразное движение. Толчкообразное и маятникообразное движение крови определяет возникновение пульсирующей боли. Постепенно экссудация вызывает развитие стаза – обычное явление при воспалении. Как правило, стаз возникает в отдельных сосудах венозной части микроциркуляторного русла из-за резкого повышения ее проницаемости. При этом жидкая часть крови быстро переходит во внесосудистое пространство и сосуд остается заполненным массой плотноприлежащих друг к другу форменных элементов крови. Высокая вязкость такой массы делает невозможным продвижение ее по сосудам и возникает стаз. Эритроциты образуют “монетные столбики”, границы между ними постепенно стираются и образуется сплошная масса в просвете сосуда – сладж (от англ. sludge – тина, грязь).
Соседние файлы в папке К экзамену
- #
- #
- #
- #
- #
- #
Источник
