Фактор хагемана в остром воспалении
Фактор Хагемана (XII фактор свертывания крови) представляет собой белок, который участвует в двух важнейших биологических процессах — гемокоагуляции и образовании кининов. Кинины можно рассматривать как относительно низкомолекулярные активные медиаторы воспаления, обладающие одновременно и другими биологическими свойствами (например, способностью вызывать бронхоспазм). Фактор Хагемана оказывается связующим звеном между процессами воспаления и свертывания крови; до его открытия связь этих процессов была гипотетической.
В крови фактор Хагемана циркулирует в неактивной форме. Он активируется при контакте с отрицательно заряженными поверхностями, к которым, в частности, относятся стекло, эластин, почечная основная мембрана и, что особенно важно для ревматологии, суставной хрящ, урат натрия, пирофосфат кальция.
Активированный фактор превращает циркулирующий в крови малоактивный прекалликреин в активный фермент калликреин, который взаимодействует с находящимися в плазме неактивными предшественниками кининов — низкомолекулярным и высокомолекулярным кининогенами. Из последних в результате такого химического взаимодействия образуются кинины, наиболее известным представителем которых является брадикинин.
Кроме того, активированный фактор Хагемана взаимодействует с добавочным количеством его неактивированных молекул, и за счет этого происходит активирование плазменного предшественника тромбопластина (ППТ), который переводит определенное количество протромбина в тромбин и в конечном итоге превращает фибриноген в фибрин, т. е. таким образом осуществляется процесс свертывания крови. Система фактора Хагемана эффективнее активирует калликреин, чем ППТ.
Существуют многообразные пути взаимодействия как между системами кининобразования и свертывания крови, так и внутри каждой из этих систем. Так, калликреин не только участвует в генерации кининов, но и способствует превращению плазминогена в протеолитический фермент плазмин (фибринолизин), расщепляющий, в частности, молекулы недавно образовавшегося фибрина. Считается, что в организме плазмин не образуется без активации фактора Хагемана.
Последний, таким образом, участвует не только в процессе свертывания крови, но и в продукции одного из активных противосвертывающих факторов. Плазмин в свою очередь способен активировать фактор Хагемана. Таким же свойством обладают калликреин (причем эта реакция ускоряется высокомолекулярным кининогеном) и комплекс прекалликреина с высокомолекулярным кининогеном. Примечательно, что активированный плазменный предшественник тромбопластина (ППТа), усиливая процессы свертывания, в то же время превращает плазминоген в плазмин, т. е. уменьшает коагуляционные свойства крови. Этим, по-видимому, объясняются большие возможности для саморегулирования процесса гемокоагуляции.
Система фактора Хагемана генерирует ряд продуктов, имеющих непосредственное отношение к развитию воспалительного процесса. Основным кинином считается брадикинин, который повышает проницаемость капилляров, расширяет артериолы, способствует освобождению гистамина из тучных клеток и повышает синтез простагландинов, рассматриваемых в настоящее время как важные медиаторы воспаления. Калликреин и фибринопептиды, возникающие в результате ферментативного расщепления фибриногена плазмином, усиливают хемотаксис лейкоцитов. Плазмин, кроме того, активирует первый компонент комплемента, расщепляет его третий компонент, превращает проколлагеназу синовиальных клеток в коллагеназу, обладающую деструктивным влиянием на ткани.
Известны физиологические антагонисты ряда биологически активных веществ, участвующих в рассматриваемой системе. Комплекс антитромбина III с гепарином угнетает фактор Хагемана и ППТа. Циркулирующий в крови a2-макроглобулин ингибирует плазмин и калликреин, а a1-антитрипсин—плазмин и ППТа. Активность брадикинина тормозится ферментом кининазой I (она угнетает также активность таких компонентов комплемента, как СЗа и С5а).
Изложенные факты демонстрируют предпосылки для возможных сочетаний воспалительного процесса с расстройствами гемокоагуляции. Последние в виде тромбирования микроциркуляторного русла часто наблюдаются в очагах воспаления. В норме деятельность систем кининообразования и гемокоагуляции протекает сбалансированно, но при качественных или даже чисто количественных изменениях их компонентов равновесие нарушается.
Опубликовал Константин Моканов
Источник
Здравствуйте! Сегодня мы поговорим о 12-ом факторе свертываемости крови, или о факторе Хагемана.
История
В 1950-е годы анализ крови перед операцией выявил удлинение внутреннего пути свертывания у железнодорожника Джона Хагемана. Знаменитый ученый Оскар Ратноф (Oscar Ratnoff) начал исследовать эту кровь и обнаружил у Хагемана дефицит неизвестного фактора свертываемости, который был назван фактором Хагемана, а потом – фактором XII.
У железнодорожника было резкое удлинение АЧТВ, и при этом не было никаких признаков кровоточивости. Интересно,что при этом умер Джон Хагеман не от кровотечения, а от тромбоза – в результате тромбоэмболии легочной артерии в молодом возрасте.
Фактор XII
Фактор XII – это профермент, синтезируемый печенью и циркулирующий в крови. Активация FXII происходит при контакте с различными поверхностями, даже со стеклом, в организме чаще с поврежденными поверхностями.
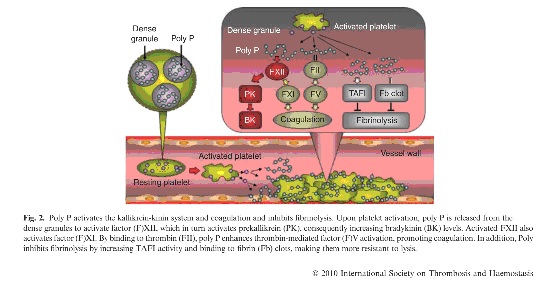
Это очень хорошая картинка, взятая из статьи, посвященной Оскару Ратнофу, обнаружившему неизвестный доселе фактор свертывания крови у сцепщика Джона Хагемана. Она иллюстрирует запуск “контактного” (“внутреннего”) пути.
-Активация тромбоцита приводит к выбросу из него гранул с полифосфатами.
-Полифосфаты запускают активацию фактора Хагемана на поверхности образующегося агрегата тромбоцитов, с последующим запуском всей цепочки.
-Потом полифосфаты вымываются и фактор Хагемана становится одним из основных факторов фибринолиза.
Дефицит уровня FXII
Дефицит уровня FXII – самая частая причина удлинения АЧТВ. И если причиной является такой дефицит, добавление в систему нормальной плазмы, содержащей нормальные количества фактора XII, укорачивает и приближает к норме АЧТВ.
Напомним, что в АЧТВ для активации свертывания используется “частичный тромбопластин”, то есть это тромбопластин без тканевого фактора, фактически мы говорим о фосфолипидах.
Фосфолипиды в системе активации АЧТВ играют роль поверхности тромбоцитов. Если в системе есть антитела против фосфолипидов, то, соответственно, и в этом случае АЧТВ будет замедляться – это и есть то, что получило название Волчаночного Антикоагулянта (ВА).
Таким образом, ВА является второй причиной удлинения АЧТВ. В присутствии ВА АЧТВ плохо корригируется добавлением плазмы, богатой фактором XII, потому что его и так много в системе.
А если мы бездумно блокируем тромбин гепарином, то будут удлиняться показатели как внешнего, так и внутреннего пути. Поэтому на фоне активной терапии гепаринами АЧТВ тоже будет удлиняться, в данном случае, фармакологически.
Главное и ключевое то, что при дефиците FXII повышается риск не кровотечений, а тромбозов! Почему? Потому что фактор XII в гораздо большей степени активирует фибринолиз, чем тромбоз.
Один из главных рисков венозного тромбоза.- недостаточный фибринолиз. Поэтому, Джон Хаггеман умер не от кровотечения, а от тромбоза.
По своей химической структуре FXII очень похож и эволюционно связан с tPA (тканевым активатором плазминогена). При этом следует помнить, что концентрация FXII значительно превышает концентрацию tPA в крови.
Для коагуляции снижение концентрации FXII не критично, а вот для фибринолиза — может быть катастрофично.
Мы видим парадокс: удлинение АЧТВ очень часто указывает на дефицит фактора Хагемана, и в пробирке мы видим гипокоагуляцию. А в организме беременной женщины мы видим гипофибринолиз – резкое торможение фибринолиза. Фибриноид начинает накапливаться, плацента быстро стареет, тромбируются мелкие вены, резко ухудшается плацентарное кровообращение с материнской стороны, и плод страдает.
Диагностика дефицита фактора 12
Определяемый нами полиморфизм rs1801020 (C46T) ассоциирован с резким снижением продукции печенью FXII (сам фактор совершенно нормальный).
В мировой научной среде проводилось очень много исследований по поводу дефицита фактора XII на течение беременности. Немцы из Геттингентского университета установили жесткую связь между наличием этого полиморфизма у женщин с привычным невынашиванием беременности (3 остановки подряд и более). А японские коллеги из Токийского университета, выявили связь этого полиморфизма с многократными неудачными попытками ЭКО.
Сейчас абсолютно доказанными вещами является то, что дефицит фактора 12 – гипофибринолиз – связан с нарушением плацентарной функции, невынашиванием на ранних сроках, ранней преэклампсией, неоднократными неудачными попытками ЭКО
Самое резкое снижение фактора XII мы наблюдаем у гомозигот T/T. У гетерозигот (около 34 %) имеется промежуточное значение концентрации FXII.
“Хороший вариант” гомозигот встречается примерно в 60%.
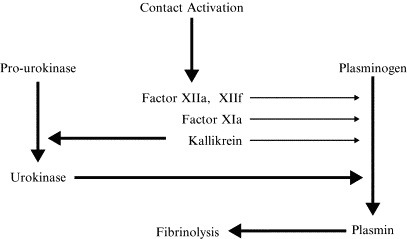
Посмотрите, пожалуйста, вот очень важная схема:

Что мы наблюдаем?
-Фактор XII активирует калликреин, который мощно активирует урокиназу.
-Урокиназа запускает образование плазмина из плазминогена. Это главный путь стимуляции фибринолиза фактором XII.
-Параллельно работают другие механизмы, не главные, но активно вносящие свой вклад в активацию плазмина.
-Сам активированный FXII катализирует переход плазминогена в плазмин.
-Активированный фактор XII активирует фактор XI (основной механизм запуска “внутреннего пути свертывания”). Но активированный таким образом FXI не только запускает генерацию тромбина, но и генерацию плазмина.
-И, наконец, активированный калликреин не только активирует урокиназу, но и сам, напрямую – плазмин.
Фактор 12 при АФС
При АФС (антифосфолипидный синдром) могут быть и АТ, направленные против FXII. Это важный анализ, но к сожалению, в нашей стране он не проводится (реактивы не серцифицированы).
При наличии антифосфолипидных АТ как правило наблюдается резкое снижение FXII , поэтому ,всегда внимательно оцениваем АЧТВ, которое часто начинает удлиняться именно при снижении концентрации FXII.
FXII может быть мишенью аутоиммунной атаки при АФС. Это частично объясняет механизм действия волчаночного антикоагулянта, удлиняющего АЧТВ.
Всё это указывает на то, что нарушение фибринолиза, одним из важных маркеров которого является снижение уровня FXII и связанное с этим удлинение АЧТВ, играет очень важную роль в нарушении плацентарной функции при АФС.
Дефицит 12 фактора у беременных
Дефицит фактора ХII может приводить к очень серьезным проблемам во время беременности, начиная от невынашиваемости на ранних сроках, и заканчивая задержкой развития плода и антенатальной гибелью.
Часто большое значение имеют не изолированные факторы, а связки полиморфизмов. В частности, при связке с таким полиморфизмом, как PAI-1, особенно если речь идет о гомозиготе 4G/4G, мы будем наблюдать достаточно серьезные проблемы с плацентацией. Потому что очистка от фибрина зоны инвазии экстравиллезного трофобласта с стенках спиральных артерий имеет очень большое значение, практически решающее для того, чтобы плацентация прошла хорошо.
Ассоциации с нарушениями фибринолиза
1) Если говорить об опасных связках, это такие полиморфизмы, как PAI-1, FXI, FXIII, FXII, PLAT и ген фибриногена. Если говорить о полиморфизмах сосудистого тонуса, это ангиотензинпревращающий фермент.
2) Группы крови (все плохие, кроме первой); Частота аллелей для европейской популяции:
3) Если говорить об антителах к фосфолипидам, то АТ против бета2GP1 и аннексина V, двух факторов, которые играют важную роль в нормальном фибринолизе.
4) Нерастворимые комплексы фибрин-мономеров (РКФМ). То есть это уже фибрин, только не успевший дальше полимеризироваться и пока еще растворимый. Этот показатель напрямую связан с активностью тромбина, и значительное повышение – плохо. Если первая цифра 4 (4,0-4,9) — нормально для беременности, они всегда более высокие с конца первых недель беременности, но если больше 5 — значит высокая активность тромбина, значит его лучше аккуратно притушить назначением гепаринов.
Для того, чтобы не пропустить серьёзные осложнения беременности, необходимо комплексное обследование комбинации гемостаза , диагностики аутоиммунных проблем иполного спектра полиморфизмов гемостаза.
Источник
Анестезиолог-реаниматолог Юлия Егорова о синдроме нарушения свертывания крови, который повышает риск тромбозов и спонтанных выкидышей
Дефицит фактора Хагемана (XII фактор свертывания крови) — это редкое (около 1:1 000 000 населения) и наследственно обусловленное нарушение коагуляционного гемостаза. Наследуется этот дефект преимущественно аутосомно-рецессивно, но в единичных случаях — более тяжелых — выявляется аутосомно-доминантное наследование. В иммунологических исследованиях было показано, что синдром Хагемана характеризуется сниженным синтезом фактора Хагемана, а не образованием его аномальных молекул.
В 1954 году в Кливленде (США) гематолог Оскар Ратнов наблюдал пациента Джона Хагемана 37 лет со значительно увеличенным временем кровотечения. Обратив внимание на то, что, несмотря на изменения в коагуляции, пациент перенес хирургическую операцию без значительного кровотечения, Ратнов совместно с биохимиком Эрлом Дэйви установил, какого именно белка не хватало в плазме у этого пациента, заподозрив в этом причину нарушения свертываемости крови. Этот сложный белок и был назван фактором Хагемана, а после того как английский гематолог Роберт Макфарлан в 1964 г. сформулировал каскадную теорию гемостаза, занял в ней место как 12‑й фактор свертывания.
Кровотечение — одно из самых опасных для организма состояний, защита организма от него должна быть как надежной, так и саморегулирующейся, чтобы остановка кровотечения не переходила в распространенный тромбоз. Эту роль выполняют сразу несколько систем — клеточная (тромбоцитарный гемостаз) и сложная система белков плазмы, состоящая из многих взаимосвязанных факторов свертывания:
- I — Фибриноген
- II — Протромбин
- III — Тканевой тромбопластин
- IV — Ионы кальция
- V — Проакцелерин
- VI — Акцелерин — изъят из классификации, так как является
активированным V фактором - VII — Проконвертин
- VIII — Антигемофильный фактор
- IX — Фактор Кристмаса
- X — Фактор Стюарта—Прауэра
- XI — Плазменный предшественник тромбопластина
- XII — Фактор Хагемана
- XIII — Фибринстабилизирующий фактор
- Фактор Флетчера — плазменный прекалликреин
- Фактор Фитцжеральда — высокомолекулярный кининоген
- Фактор Виллебранда — опосредует связывание тромбоцитов с субэндотелием
Фактор Хагемана — сиалогликопротеин — сложное органическое соединение, помимо белковой части включающее в себя олигосахарид и сиаловые кислоты. Сиалогликопротеин синтезируется в печени, далее свободно и «без дела» циркулирует в плазме крови, пока не соприкоснется с отрицательно заряженными поверхностями, например, коллагеном поврежденной ткани или с калликреином, о котором стоит рассказать подробнее.
Калликреин — один из основных функциональных элементов сложной калликреин-кининовой системы, регулирующей процессы воспаления, свертывания крови, микроциркуляции и функции сосудистой стенки.
Фактор Хагемана, активированный повреждением ткани, участвует в запуске калликреин-кининовой системы, превращая прекалликреин в калликреин, а калликреин в свою очередь активирует все новые молекулы фактора Хагемана.
Получается петля для каскадного нарастания процесса. За счет этого небольшое количество поврежденных тканей вызывает реакцию в значительной части плазмы крови.
Кроме того, на 12 фактор (Хагемана) в активной форме действует 13 фактор (фибринстабилизирующий фактор), что запускает каскад биохимических реакций среди молекул, исходно присутствовавших в крови, — внутренний путь коагуляции. В отличие от внутреннего пути, внешний запускается попаданием в кровь тканевого тромбопластина из поврежденных тканей.
Таким образом, фактор Хагемана оказывается связующим звеном между процессами воспаления и свертывания крови; до его открытия связь этих процессов была гипотетической.
Клиническая картина
Клинически дефицит 12 фактора свертывания крови проявляется удлинением времени кровотечения без каких‑либо других симптомов нарушения гемостаза. Выраженность удлинения времени кровотечения зависит от типа наследования генетического дефекта. При доминантном типе дефицит выражен сильнее, при рецессивном — частично компенсируется другими факторами свертывания. Время кровотечения увеличено из‑за замедленной инициации каскадной системы свертывания крови. Склонности к патологическим кровотечениям пациенты не проявляют, поэтому заболевание часто не обнаруживают или обнаруживают случайно при лабораторном обследовании или предоперационном скрининге.
Немного парадоксальным кажется то, что при дефиците фактора свертывания проявляют себя не кровотечения, а тромбозы. Например, Джон Хагеман, по имени которого назван фактор свертывания, впоследствии погиб от тромбоэмболии, которой осложнился перелом костей таза. Современные опубликованные клинические случаи оперативных вмешательств у пациентов с синдромом Хагемана, к счастью, заканчивались благополучно. Тромбофилические нарушения связаны с тем, что XII фактор участвует в разрушении тромбов путем активации калликреин-кининовой системы. Активный калликреин не только запускает генерацию кининов, регулирующих воспаление, сосудистый тонус и болевые реакции, но и превращает неактивный белок плазминоген в активный фермент плазмин (фибринолизин), который и растворяет фибриновую часть тромба. Поэтому с дефицитом фактора Хагемана ассоциированы:
- тромбозы
- мигрирующие тромбофлебиты
- тромбоэмболии
- инфаркты
- спонтанные аборты
Диагноз и прогноз
Кроме лабораторных исследований установить диагноз помогут анамнестические данные: склонность к длительным кровотечениям и тромботическим осложнениям у пациента и его родственников, а также положительный симптом Румпеля — Лееде (появление мелкоточечных кровоизлияний дистально от наложенного на плечо жгута). Прогноз при дефиците фактора Хагемана в большинстве случаев благоприятный, лечение не требуется. Коррекции это состояние требует только в связи с хирургическими вмешательствами. В качестве подготовки к операции может быть назначено переливание небольших доз свежезамороженной плазмы.
Период выведения донорского XII фактора — 48–56 ч. Также при наличии этой коагулопатии следует уделять большее внимание профилактике тромботических осложнений: профилактическая компрессия нижних конечностей, УЗИ-контроль состояния вен нижних конечностей и малого таза, особенно при длительном постельном режиме. В послеоперационном периоде для профилактики тромбозов необходимо назначение низкомолекулярных гепаринов, а для терапии кровотечений — отказ от применения ингибиторов фибринолиза, таких как аминокапроновая и транексамовая кислота.
Источник
