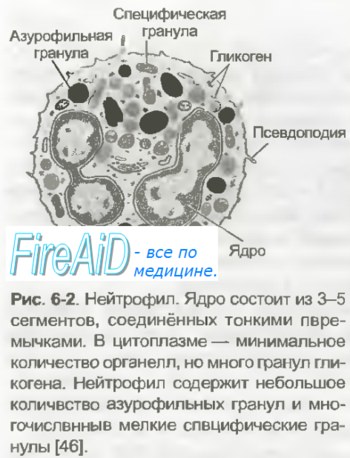
Функции нейтрофилов в очаге воспаления
Одним из подвидов гранулоцитарных лейкоцитов являются нейтрофилы. Созревают они в красном костном мозге. Как связаны между собой нейтрофилы и воспаление, какую роль они играют в защите организма?
Коротко о нейтрофильных гранулоцитах
Эти клетки белой крови достаточно крупные, имеют диаметр около 10 мкм. Свое название они получили из-за наличия в цитоплазме клетки зернистых гранул. Гранулы содержат особые антибактериальные ферменты, способные разрушать оболочку бактерий, внедрившихся при воспалении. При лабораторных исследованиях для определения количества клеток, мелкие зерна в виде пыли обрабатывают красителями, они окрашиваются в фиолетово-розовый цвет.
Зрелые нейтрофилы – большая группа, составляющая 2/3 от количества всех клеток лейкоцитов. При этом большее их количество находится в костном мозге, остальные распределяются по другим органам. И только небольшая часть (1%), достигая периферической крови, через несколько часов проникает в ткани. Продолжительность их жизни зависит от количества микроорганизмов в очаге воспаления.
Процесс образования нейтрофильных клеток лейкоцитов в костном мозге составляет примерно 5 суток. Затем они перемещаются по сосудистому руслу в течение 8–10 часов. За это время клетки, при столкновении с чужеродным агентом, уничтожают вредоносные частицы в очаге поражения.
Функции нейтрофилов при заболевании
Основная функция – защита организма при инфицировании. Нейтрофильные гранулоциты крови очень подвижны. В очаге поражения они выделяют особые ферменты, которые способствуют рассасыванию отмирающих тканей. Передвигаясь по сосудам, они находят инфицированное место, проникают сквозь стенки капилляров, поглощают и растворяют патогенные бактерии.
Для работы нейтрофилы, используют энергию, а получать ее могут даже без участия кислорода. Это дает Клетки крови возможность выполнять функции в очаге, где нарушено кровообращение. Нейтрофильные клетки лейкоцитов выделяют фермент лизосом, который способствует размягчению тканей в инфицированном очаге. Клетки захватывают вредоносные частицы и «переваривают» их.
Кроме того, они способны оказывать влияние на иммунитет. Гранулы выделяют в кровь регуляторное вещество, которое другие клетки воспринимают как сигнал для защиты организма. А также нейтрофилы содержат особые вещества, которые влияют на процесс свертывания крови.
Работа нейтрофильных лейкоцитов более всего распространяется на бактерии и грибки, на вирусы они реагируют слабо. Один нейтрофил способен уничтожить около семи микробов. Жизнь клеток продолжается от нескольких часов до нескольких суток, затем они нейтрализуются печенью и селезенкой.
Классификация нейтрофильных гранулоцитов
Исходя из формы ядра, нейтрофилы состоят из трех видов гранулоцитарных клеток: сегментоядерные, палочкоядерные и юные. В костном мозге всегда есть некоторое количество нейтрофилов. При патологических изменениях и по требованию организма происходит их выброс в кровь.
Начиная с зарождения и до полного созревания, нейтрофилы проходят шесть стадий развития. Одновременно организм может иметь клетки разных стадий созревания. Для постановки диагноза важным показателем есть соотношение четырех видов друг с другом в результатах анализов крови. По степени зрелости можно назвать следующие группы: миелоциты → метамиелоциты → палочкоядерные → сегментоядерные.
При наличии воспаления первыми начинают борьбу самые старшие клетки. Обычно их количества достаточно для нейтрализации бактерий в очаге. При серьезном воспалении функцию могут выполнять палочкоядерные, и даже совсем несозревшие клетки.
Образование полностью созревших клеток происходит только в костном мозге. Юные клетки у человека здорового в крови не присутствуют. Если болезнь приобретает осложненную форму, прежде всего, гибнут сегментоядерные клетки. При этом новые формы не успевают созревать, кровь наполняют незрелые нейтрофилы, изменяется формула лейкоцитов. Учитывая соотношение старших и молодых клеток, происходит сдвиг формулы в ту или другую сторону.
Нормы и аномалии нейтрофилов
Допустимый уровень нейтрофильных клеток у взрослых варьируют от 45 до 70% от уровня лейкоцитов. Для женщин и мужчин значения нормы практически одинаковы. Показатели отличаются у разных возрастных групп. В процессе роста у детей содержание нейтрофильных клеток изменяется. После шести лет лейкоцитарная формула у детей сравнивается с данными анализов у взрослых.
Состояние, когда нейтрофилы повышены, именуют нейтрофилией или нейтрофилез. Показатели умеренны, если литр крови содержит не более 10 миллиардов клеток, повышены, если их от 10 миллиардов до 20. Цифры от 20 до 60 свидетельствуют о тяжелой нейтрофилии. Нарушения формулы крови могут быть вызваны некоторыми патологиями:
- образование гнойного воспаления – ангина, перитонит, аппендицит, пиелонефрит, сепсис;
- отравление алкоголем или другими токсинами, действующими на костный мозг;
- разложение тканей в очаге новообразований;
- некрозы при ожоге, а также патология тканей во время инсульта или инфаркта.
Количество нейтрофилов держится выше нормы, какое-то время после патологического процесса. Чуть повышены нейтрофилы могут быть у беременных, после тяжелой физической нагрузки, а также после сытной трапезы.
Нейтропения свидетельствует о сниженном уровне нейтрофилов. Численность их колеблется от 1,5 до 0,5 миллиарда в зависимости от степени нейтропении. Такое положение наблюдается при недостаточной выработке клеток костным мозгом, гибели клеток при наличии тяжелого воспаления. Понижение нейтрофилов может быть связано с лучевой и химиотерапией, анемией или недостатком витаминов.
Некоторые рекомендации
Нейтрофилия и нейтропения не рассматриваются как заболевание. Но сдвиг формулы в одну или другую сторону, важный показатель для постановки диагноза. Лекарства для нормализации уровня нейтрофилов в крови нет. Врач должен установить причину нарушений, принять меры и назначить лечение для устранения обнаруженной патологии.
После лечения воспаления показатели сами приходят к нормальным цифрам. Если причина кроется в приеме лекарств, врач должен пересмотреть назначения, отменить неэффективные препараты или заменить другими. При недостаточном поступлении или усваивании питательных веществ, витаминов, минералов следует сбалансировать питание, начать прием витаминных и минеральных комплексов.
Источник
Оглавление темы “Функции клеток крови. Эритроциты. Нейтрофилы. Базофилы.”: Функции нейтрофильных гранулоцитов ( лейкоцитов ). Дефенсины. Кателицидины. Белки острой фазы. Хемотаксические факторы.Функцией зрелых нейтрофильных лейкоцитов является уничтожение проникших в организм инфекционных агентов. Осуществляют ее они, тесно взаимодействуя с макрофагами, Т- и В-лимфоцитами. На важность функционального вклада нейтрофилов в защиту организма от инфекции указывает, например, тяжесть течения инфекционных заболеваний у больных, страдающих сниженной продукцией или качественными нарушениями этих клеток. Нейтрофилы фагоцитируют поврежденные клетки собственного организма, секретируют бактерицидные вещества и способствуют регенерации тканей, удаляя из них поврежденные клетки, а также секретируя стимулирующие регенерацию тканей вещества (нейтрофилокины).
Зрелый нейтрофил содержит сегментированное на 2—5 долей ядро, уплотненный хроматин, а в цитоплазме — многочисленные мелкие секреторные гранулы трех типов. Часть гранул, дающих положительную окраску на фермент миелопероксидазу, представлена лизосомами, которые содержат лизоцим (повреждает стенку бактерий), низкомолекулярные катионные белки — дефенсины и кателицидины (нарушают дыхание и рост микроорганизмов и грибков; дефенсины повышают проницаемость сосудов микроциркуляторного русла), протеазы и кислые гидролазы — позволяют ней-трофилам легко переваривать фагоцитированные объекты. Гранулы 2-го типа содержат лактоферрин, обладающий бактериостатическим действием, транскобаламины I и III — переносчики витамина В12 в крови и лизоцим. Вещества гранул 3-го типа содержат кислые гликозаминогликаны, участвующие в процессах размножения, роста и регенерации тканей, благодаря их способности концентрировать факторы роста в тканях костного мозга. Гранулы 2-го и 3-го типов, содержащиеся в цитоплазме нейтрофилов, постоянно секретируют биологически активные вещества даже вне фагоцитоза. К ним относятся опухольнекротизирующий фактор а, интерлейкин-1, интерлейкин-6, интерлейкин-11. Вместе с такими же цитокинами, секре-тируемыми макрофагами в острой фазе заболевания, вызванного инфекцией, травмой (например, ожоговой), они стимулируют синтез и секрецию в кровь из печени так называемых белков острой фазы (с-реактивный белок, сц-антитрипсин, а,-кислый гликопротеин, церулоплазмин), повышающих устойчивость организма к инфекции, токсичным соединениям, образуемым микроорганизмами. Нейтрофилы осуществляют свои функции благодаря способности быстро мигрировать и накапливаться в инфицированном или поврежденном участках организма, фагоцитировать, т. е. захватывать и разрушать в фагоцитарных вакуолях внутри клетки поглощенные бактерии и поврежденные клетки. Их способность к миграции связана с хорошо развитым аппаратом движения, выбор направления их движения к воспаленным или инфицированным тканям обусловлен появлением в этих тканях вазоактивных и хемотаксических факторов. Вазоактивные факторы (дефенсины, гистамин, секретируемый под влиянием дефенсинов тучными клетками тканей) повышают проницаемость капилляров, что способствует миграции нейтрофилов в ткань. Хемотаксические факторы взаимодействуют с рецепторами на поверхности гранулоцитов, образуя лиганд-рецепторный комплекс, определяющий движение нейтрофилов к воспаленному участку. Мощным хе-мотаксическим эффектом обладают N-формилпепетиды бактериального происхождения и лейкотриены, производные метаболизма арахидоновой кислоты в мембране клеток. Лейкотриены секретируются активированными Т-лимфоцитами и макрофагами после воздействия на них бактериальных веществ. Помимо лейкотриенов эти клетки секретируют другие хемо-аттрактанты — эндотоксины. Важными хемотакическими факторами являются продукты активации комплемента — фрагменты его молекул С3в и С5а. Некоторые из этих факторов, особенно С3в, функционируют как опсонины, т. е. вещества, облегчающие фагоцитоз бактерий (от греческого орsonein — делать съедобным). Недостаточность хемотаксической активности нейтрофилов препятствует накоплению этих лейкоцитов в очаге воспаления, что способствует распространению инфекции в организме. К таким последствиям приводит, например, нарушение хемотаксиса нейтрофилов у больных при ожоговой болезни, диабете, при низком содержании белка в рационе человека. – Также рекомендуем “Бактерицидный эффект нейтрофилов. Гранулопоэз. Нейтрофильный гранулопоэз. Гранулоцитоз. Нейтропения.” |
Источник
Нейтрофилия. Защитные механизмы воспаления
а) Резкое увеличение количества нейтрофилов в крови – нейтрофилия. В течение нескольких часов после начала острого, тяжелого воспаления количество нейтрофилов в крови возрастает иногда в 4-5 раз, т.е. от нормального количества 4000-5000 до 15000-25000 нейтрофилов в 1 мкл. Это состояние называют нейтрофилией, что означает увеличение количества нейтрофилов в крови.
Нейтрофилия вызывается продуктами воспаления, которые входят в кровоток, транспортируются к костному мозгу и там действуют на резервные нейтрофилы костного мозга, заставляя их выходить в циркулирующую кровь. Это обеспечивает возможность доставки еще большего числа нейтрофилов в воспаленную тканевую область.
б) Вторичная инвазия макрофагов в воспаленную ткань является третьей «линией обороны». Вместе с инвазией нейтрофилов моноциты поступают из крови в воспаленную ткань и увеличиваются, становясь макрофагами. Однако количество моноцитов в циркулирующей крови низкое; запас моноцитов в костном мозге также гораздо меньший, чем запас нейтрофилов. Следовательно, увеличение количества макрофагов в воспаленной ткани происходит значительно медленнее, чем нейтрофилов, и требует нескольких дней, чтобы стать эффективным.
Более того, даже после внедрения в воспаленную ткань моноциты являются еще незрелыми клетками, и нужно 8 ч или более для разбухания их до значительных размеров и развития громадного количества лизосом; только тогда они приобретают характерную для тканевых макрофагов высокую способность к фагоцитозу. Однако на протяжении периода от нескольких дней до нескольких недель макрофаги становятся преобладающими фагоцитарными клетками воспаленной области из-за значительного увеличения продукции новых моноцитов костным мозгом, что будет объяснено далее.
Как уже подчеркивалось, в сравнении с нейтрофилами макрофаги могут фагоцитировать гораздо больше бактерий (примерно в 5 раз) и значительно более крупные частицы, включая даже сами нейтрофилы и большое количество некротизированной ткани. Кроме того, макрофаги играют важную роль в инициации развития антител.
в) Увеличение продукции гранулоцитов и моноцитов костным мозгом является четвертой «линией обороны». Это происходит в связи со стимуляцией гранулоцитарных и моноцитарных клеток-предшественников костного мозга. Однако требуются 3-4 сут, прежде чем вновь сформированные гранулоциты и моноциты достигнут стадии, когда они покидают костный мозг. Если стимул из воспаленной ткани продолжает действовать, костный мозг может непрерывно производить эти клетки в огромных количествах в течение нескольких месяцев и даже лет, иногда со скоростью, в 20—50 раз превышающей норму.

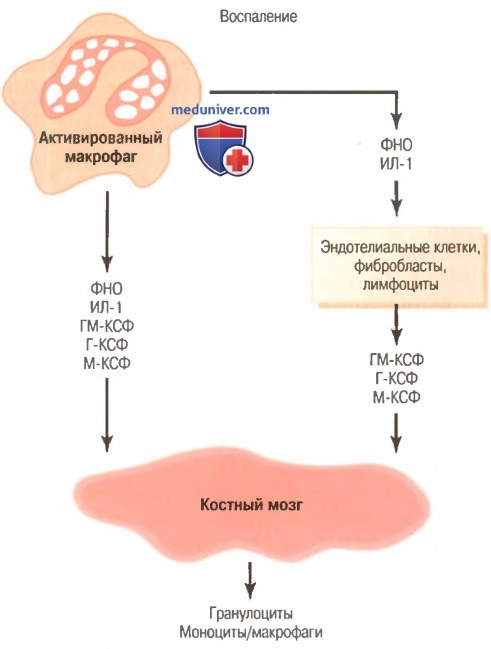
Регуляция формирования гранулоцитов и моноцитов-макрофагов костным мозгом с помощью множества факторов роста, выделяемых из активированных макрофагов в воспаленной ткани.
Г-КСФ – гранулоцитарный колониестимулирующий фактор, ГМ-КСФ – гранулоцитарно-моноцитарный колониестимулирующий фактор,
ИЛ-1 – интерлейкин-1, М-КСФ — моноритарный колониестимулирующий фактор,
ФНО – фактор некроза опухоли
г) Регуляция реакций макрофагов и нейтрофилов по принципу обратной связи. В настоящее время известно более двух дюжин факторов, участвующих в регуляции реакции макрофагов на воспаление, пять из них, как полагают, играют доминирующую роль. Они представлены на рисунке выше и включают:
(1) фактор некроза опухоли (ФНО);
(2) интерлейкин-1 (ИЛ-1);
(3) гранулоцитарно-моноцитарный колониестимулирующий фактор (ГМ-КСФ);
(4) гранулоцитарный колониестимулирующий фактор (Г-КСФ);
(5) моноцитарный колониестимулирующий фактор (М-КСФ).
Эти факторы формируются активированными макрофагальными клетками и в меньших количествах — другими клетками воспаленной ткани.
Основными стимуляторами увеличения продукции гранулоцитов и моноцитов костным мозгом являются три колониестимулирующих фактора, один из которых (ГМ-КСФ) повышает продукцию и гранулоцитов, и моноцитов; два других (Г-КСФ и М-КСФ) усиливают продукцию гранулоцитов и моноцитов, соответственно. Эта совокупность ФНО, ИЛ-1 и колониестимулирующих факторов обеспечивает мощный механизм обратной связи, который начинается с воспаления ткани и развивается до формирования большого количества защитных белых клеток крови, которые помогают удалять причину воспаления.
– Также рекомендуем “Образование гноя. Эозинофилы и базофилы”
Оглавление темы “Клетки иммунитета. Виды иммунитета”:
1. Ретикулоэндотелиальная система. Макрофаги в лимфатических узлах
2. Альвеолярные макрофаги в легких. Клетки Купфера печени
3. Эффекты воспаления. Макрофаги и нейтрофилы при воспалении
4. Нейтрофилия. Защитные механизмы воспаления
5. Образование гноя. Эозинофилы и базофилы
6. Лейкопения. Лейкемии и его типы
7. Врожденный иммунитет. Приобретенный или адаптивный иммунитет
8. Типы приобретенного иммунитета. Лимфоциты в приобретенном иммунитете
9. Длительность жизни белых клеток крови. Нейтрофилы и макрофаги
10. Роль лимфоцитарных клонов. Происхождение клонов лимфоцитов
Источник
Значение нейтрофилов. Механизмы фагоцитоза
Воспалительная реакция нейтрофилов возникает, когда в крови посткапиллярных венул эти клетки «обнаруживают» небольшое количество хемокинов и других хемотаксических веществ, выделяющихся из очага инфекции. Эти растворимые эффекторы воспаления вызывают изменения состава и активности поверхностных молекул эндотелиальных клеток и нейтрофилов. Начальные взаимодействия между этими клетками (главным образом, между селектинами нейтрофилов и углеводными компонентами поверхности эндотелия) отличаются низким сродством и обратимостью.
В результате происходит так называемое перекатывание лейкоцитов по эндотелию; слабые связи образуются и распадаются, приводя к колебательному движению нейтрофилов по поверхности эндотелия. Перекатывание обеспечивает более тесный контакт нейтрофилов с такими активирующими факторами, как ФНО) или ИЛ-1, вследствие чего возникают качественные и количественные изменения Р2-интегриновых рецепторов нейтрофилов (поверхностные молекулы группы CD11/CD18).
Активированные интегриновые рецепторы прочно связывают нейтрофилы друг с другом и с эндотелиальными клетками. Окончательный результат всех этих межклеточных взаимодействий сводится к тому, что нейтрофилы распластываются на эндотелиальных клетках и образуют агрегаты друг с другом и с тромбоцитами, приводя к сужению просвета венул и снижению кровотока.
На следующем этапе интегриновые рецепторы нейтрофилов концентрируются на поверхности псевдоподий. Нейтрофилы способны перемещать свои интегриновые рецепторы по поверхности и изменять свою конфигурацию, что позволяет им проходить через контакты между эндотелиальными клетками и проникать в ткани. Затем они мигрируют в очаг инфекции по градиенту концентраций хемокинов или других хемоаттрактантов. Миграция нейтрофилов — сложный процесс, включающий циклы перемещения рецепторов, проведение сигналов в клетки и перестройку актиновых нитей цитоскелета.
Проникновению нейтрофилов сквозь базальную мембрану сосудов и соединительную ткань способствует секреция этими клетками специфических гранул или везикулярных элементов, содержащих желатиназу, гепариназу и другие ферменты. Достигнув очага инфекции, нейтрофил с помощью Fc-участка иммуноглобулина и рецепторов комплемента, фи-бронектина и других молекул адгезии распознает патогенный агент.
Поглощаемые нейтрофилами микробы предварительно подвергаются опсонизации (подготовке к поглощению) сывороточными термостабильными и термолабильными факторами, соответственно IgG и СЗ. Опсонины облегчают фагоцитоз, при котором микроб втягивается в закрытую вакуолю, называемую фагосомой.
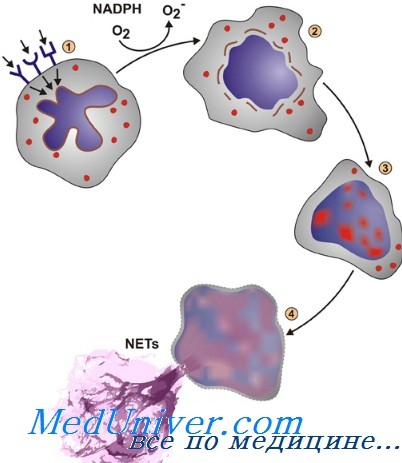
Образование фагосомы сопровождается двумя реакциями, необходимыми для проявления бактерицидной активности нейтрофилов, — дегрануляцией и активацией НАДФ-зависимой оксидазы. Слияние мембран гранул с мембраной фагосомы приводит к появлению в фагосоме белков, обладающих мощной антимикробной активностью. Содержимое специфических, а затем и азурофильных гранул попадает в фагосому. Одновременно в ее мембране происходит сборка и активация НАДФ-зависимой оксидазы.
Под действием этого фермента из молекулярного кислорода образуется большое количество супероксид-аниона (O2), который, в свою очередь, превращается в перекись водорода (Н2O2) и синглетный кислород. Н2O2 реагирует с O2, образуя гидроксильные радикалы. В присутствии миелопероксидазы (основного компонента азурофильных гранул) и хлоридного иона в фагосоме образуется хлорноватистая кислота (НОС1). Н2O2 и НОС1 не только обладают бактерицидной активностью, но и модулируют иммунные реакции. Эти оксиданты денатурируют белки, повышая их чувствительность к протеолизу, и, кроме того, активируют некоторые протеазы нейтрофилов.
Все это способствует разрушению патогенного агента и удалению его из очага инфекции. Оксиданты также инактивируют хемотаксические факторы, прекращая приток нейтрофилов в очаг инфекции и тем самым ослабляя процесс воспаления.
– Также рекомендуем “Мононуклеары: моноциты и макрофаги”
Оглавление темы “Клетки иммунной системы”:
- Механизмы созревания нейтрофилов. Дифференцировка нейтрофилов
- Значение нейтрофилов. Механизмы фагоцитоза
- Мононуклеары: моноциты и макрофаги
- Активация макрофагов. Механизмы
- Функции и значение макрофагов
- Нарушения функции моноцитов и макрофагов иммунитета
- Функции и значение эозинофилов
- Причины эозинофилии. Гиперэозинофильный синдром
- Нарушения функции фагоцитов. Генетические причины недостаточности адгезии лейкоцитов
- Клиника и лечение недостаточности адгезии лейкоцитов – НАЛ
Источник