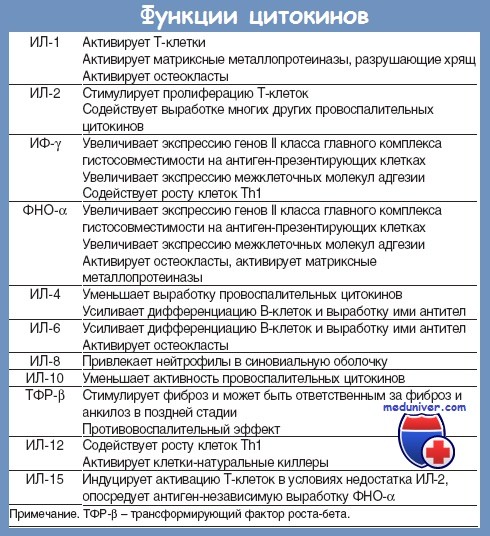
Иммунное воспаление и интерлейкины
Энциклопедия / Анализы / Интерлейкины 1, 6, 8, 10
Синонимы: Интерлейкины, ИЛ, Interleukin, IL.
Научный редактор: М. Меркушева, ПСПбГМУ им. акад. Павлова, лечебное дело.
Август, 2018г.
Интерлейкины (цитокины) являются частью иммунной системы организма человека и представляют собой гормоноподобные белки, которые вырабатываются лейкоцитами, фагоцитами и другими тканевыми клетками с целью обеспечения иммунного ответа на проникновение провоцирующего агента (вируса, бактерии, микроба, паразита и пр.).
Всего существует более 20 видов интерлейкинов, отличающихся между собой по своим свойствам и функциям. Каждый из них отвечает за определенную иммунную реакцию организма (аллергия, боль, гипертермия, воспаление и т.д.), контролирует ее течение и интенсивность.
Диагностическое обследование на ИЛ позволяет установить наличие воспалительных, вирусных, бактериальных, инфекционных и паразитарных заболеваний, а также определить иммунный статус организма и скорость иммунного отклика
Интерлейкины образуют сигнальную клеточную структуру, которая передает информацию белым кровяным тельцам (лейкоциты), «оповещая» их о возникшей угрозе. После этого нужный вид лейкоцитов активируется и направляется к патологическому очагу.
Организм производит очень малое количество ИЛ, поэтому ученые научились получать их лабораторным путем. Введение извне высоких доз интерлейкинов стимулирует иммунную систему и способствует повышению ее функциональности практически в 2 раза. Поэтому заместительная терапия ИЛ активно применяется в борьбе с раковыми и аутоиммунными заболеваниями.
Иммунологический тест на интерлейкины позволяет не только определить наличие, стадию и форму заболевания, но также и решить вопрос о целесообразности назначения больному заместительной терапии ИЛ. Кроме того, обследование на ИЛ проводится и с целью оценки эффективности текущего курса лечения.
Наибольшее диагностическое значение имеют 4 вида интерлейкинов: ИЛ-1, ИЛ-6, ИЛ-8 и ИЛ-10.
Интерлейкин-1 – цитокин, отвечающий за реакцию воспаления. Выделяют 2 подтипа:
- интерлейкин-1бета
- интерлейкин-1-альфа.
В организме человека преобладает подтип 1-b.
Через 5 часов после контакта с антигеном начинается его интенсивное производство, которое может продолжаться до 2 суток. В этот период ИЛ-1 выполняет следующие функции:
- иммунологическую (передает сигнал лейкоцитам);
- кроветворную (усиливает выработку красных кровяных телец);
- защитную (обеспечивает реакцию организма на антиген);
- межсистемную (устанавливает связь между внутренними системами организма).
Интерлейкин-11 участвует в первичной стадии иммунного ответа:
- Активизирует лимфоциты (Т-хелперы) и способствует трансформации В-лимфоцитов в плазматические клетки, которые, в свою очередь, участвуют в образовании антител.
- Защищает кровяные клетки от воздействия радиоактивных веществ.
- Обеспечивает передачу сигналов между нервной, нейроэндокринной и иммунной системами и участвует в синтезе важнейших гормонов гипоталамуса и гипофиза, подавляет секрецию пролактина, что важно для наступления беременности.
- Регулирует поведенческие реакции человека и его сон.
- Участвует в регуляции температуры тела, его повышенная продукция приводит к развитию лихорадки.
- Вызывает продукцию белков острой фазы воспаления в печени.
Интерлейкин-62 является основным медиатором острых воспалительных процессов в тканях.
- Он отвечает за скорость производства и созревания антител, В-лимфоцитов и иммуноглобулинов.
- ИЛ-6 принимает активное участие в работе внутренних органов и систем организма.
- Играет важную роль при механических повреждениях тканей в результате травм, ожогов, ударов, порезов.
- Вызывает обострение хронических заболеваний и переводит острые болезни в хроническую форму.
- Сам ИЛ-6 не защищает клетки от радиации, то усиливает защитную функцию ИЛ-1.
- Регулирует эндокринную систему: подавляет выработку тиреотропного гормона и стимулирует секрецию соматотропного гормона.
Интерлейкин-8 вырабатывается в организме через 4 часа после активации других клеток иммунитета. Причиной для секреции цитокина может послужить отравление организма продуктами жизнедеятельности патогенных микроорганизмов, производство фактора некроза опухоли, а также сигнал от интерлейкина-1. ИЛ-8 также называют фактор, активирующий нейтрофилы (NAF).
ИЛ-8 выполняет следующие функции:
- участвует в регенеративных процессах (заживление ран),
- может катализировать рост и развитие опухолей,
- является маркером на аутоиммунные заболевания (ревматоидный артрит, волчанка)
На заметку: специалисты также отмечают взаимосвязь3 между ИЛ-8 и вероятностью преждевременных родов. Как правило, у половины обследованных беременных с риском преждевременных родов концентрация интерлейкинов-1, -6 и -8 в околоплодных водах повышена.
Интерлейкин-104 обладает противовоспалительным, прямо противоположным действию других цитокинов, эффектом.
- Он подавляет озноб и лихорадку (синдром воспалительной реакции иммунитета).
- Может снижать производство других интерлейкинов.
- Участвует в местной иммунной и антипаразитарной защите и повышает аллергическую реактивность организма.
- Защищает клетки головного мозга от ишемического повреждения.
- В определенной дозе содержится в грудном молоке, что обеспечивает новорожденным защиту от воспаления кишечника.
Важно! Изменения концентрации ИЛ-10 возможно у пациентов с нарушениями работы почек. После пересадки этого органа уровень ИЛ-10 может снижаться, что будет свидетельствовать о возникновении реакции отторжения трансплантата.
Увеличение концентрации ИЛ-10 у онкобольных – неблагоприятный признак, характерный для усиления опухолевого роста. Количество ИЛ-10 повышается после переливания крови.
Для ИЛ-1
- Оценка иммунного статуса;
- Диагностика тяжелых бактериальных, инфекционных и воспалительных заболеваний.
Для ИЛ-6
- Бактериальные инфекции, тяжелые воспалительные состояния;
- ВИЧ, СПИД;
- Комплексное обследование онкобольных;
- Лечение пациентов с высокой сенсибилизацией (аллергическая реакция);
- Острый панкреатит (воспаление поджелудочной железы);
- Аутоиммунные процессы;
- Подозрение на бактериальный сепсис (инфицирование крови) у новорожденных.
Для ИЛ-8
- Оценка состояния иммунной системы пациента при острых и хронических инфекциях, злокачественных новообразованиях;
- Диагностика начальной стадии инфаркта миокарда.
Для ИЛ-10
- Оценка иммунного статуса организма;
- Определение успешности приживления пересаженного трансплантата (почки);
- Прогнозирование рисков развития инсульта или ишемической болезни сердца (ИБС);
- Подбор тактики и оценки эффективности лечения гепатита С;
- Обследование онкобольных.
Дают направление на интерлейкины и проводят расшифровку результатов проводят специалисты:
- иммунолог,
- инфекционист,
- нефролог,
- кардиолог,
- онколог.
Врач может поставить достоверный диагноз только при изучении других показателей крови, в том числе уровней остальных интерлейкинов.
Референсные значения лаборатории Инвитро
| Вид интерлейкина | Концентрация, пг/мл |
| ИЛ-1 | < 5 |
| ИЛ-6 | < 7 |
| ИЛ-8 | < 62 |
| ИЛ-10 | < 9,1 |
Важно! Интерпретация результатов всегда проводится комплексно. Поставить точный диагноз на основании только одного анализа невозможно.
Для интерлейкина-1
- Бактериальные и воспалительные заболевания;
- Туберкулез, саркоидоз;
- Аутоиммунные процессы (ревматоидный артрит);
- Эндокринные заболевания (сахарный диабет 1-го типа);
- Множественные травмы в организме;
- Угроза выкидыша;
- УФ-облучение;
- Отторжение пересаженной почки;
- ВИЧ или СПИД;
- Миелолейкоз (опухолевое поражение костного мозга) в острой или хронической форме;
- Некоторые виды лейкоза.
Для интерлейкина-6
- Острый воспалительный или инфекционный процесс;
- Ревматоидный артрит или другие аутоиммунные патологии;
- Эссенциальный тромбоцитоз (повышенный уровень тромбоцитов);
- Системные поражения почек или печени;
- Псориаз (неинфекционное поражение кожи);
- Ожирение;
- Атеросклероз;
- Панкреатит в острой форме;
- Болезнь Крона (поражение органов пищеварительного тракта);
- Заболевания органов ЖКТ (язвенные поражения);
- Обширные травмы, например, в результате ДТП;
- Неспецифический язвенный колит (воспаление слизистой толстой кишки);
- Целиакия (аллергия на глютен);
- Слизисто-кожный лимфатический синдром (острое поражение артерий);
- Гепатит вирусной этиологии (воспаление печени);
- Миксомы сердца (доброкачественные опухоли предсердия);
- Саркома Капоши (злокачественные новообразования на коже);
- Карцинома почки (злокачественное новообразование);
- Лимфома (опухоль лимфатической системы);
- Первичный билиарный цирроз печени (разрушение внутрипеченочных желчных протоков аутоиммунной природы).
Для интерлейкина-8
- Тяжелые инфекционные и воспалительные процессы (особенно, происходящие в легких);
- Острая форма инфаркта миокарда;
- Ревматоидный артрит;
- Псориаз;
- Язвенный колит (воспаление слизистой оболочки кишечника);
- Септический шок (угрожающее жизни состояние, развивающееся вследствие тяжелых инфекционных заболеваний);
- Гломерулонефрит (поражение клубочков почек);
- Злокачественные и доброкачественные новообразования;
- Гепатит (алкогольная форма).
Для интерлейкина-10
- Гемотрансфузии (переливание крови);
- Почечная недостаточность (хроническая форма);
- Злокачественные процессы в организме;
- Положительный прогноз лечения гепатита С.
Низкий интерлейкин-1:
- респираторные вирусные заболевания в острой форме;
- псориаз;
- онкология легких;
- прием некоторых препаратов: циклоспорина А, глюкокортикоидов и т.д.;
- атопии (склонность организма к различным аллергическим реакциям).
Низкий интерлейкин-10:
- отторжение трансплантата после пересадки почки;
- метаболический синдром (гормональные и метаболические нарушения) у пациенток с ожирением;
- неблагоприятный прогноз лечения инсульта.
Забор крови проводится в утреннее время (до 11.00) и строго натощак. Последний прием пищи должен быть не позднее чем за 8-14 часов до венепункции.
Накануне процедуры:
- исключить из рациона жирные, острые, жареные блюда, алкоголь и кофеинсодержащие напитки;
- не париться в бане или сауне;
- избегать тяжелых физических нагрузок и эмоционального стресса.
Непосредственно перед процедурой:
- нельзя пить ничего, кроме обычной негазированной воды;
- запрещено курить, употреблять наркотические и лекарственные препараты;
- рекомендовано соблюсти режим покоя.
Обо всех текущих или недавно завершенных курсах лечения и диагностических обследованиях врача нужно предупредить заранее.
Источники:
- 1. The interleukin (IL)-1 cytokine family–Balance between agonists and antagonists in inflammatory diseases//2015 Nov;76(1):25-37. doi: 10.1016/j.cyto.2015.06.017.
- 2. IL-6 in Inflammation, Immunity, and Disease//2014 Oct; 6(10): a016295.doi: 10.1101/cshperspect.a016295
- 3. В. Н. Кузьмин, Г. А. Мурриева. Значение полиморфизма и экспрессии генов цитокинов в прогнозировании риска преждевременных родов//Медицинский научно-практический портал “Лечащий врач”
- 4. Interleukin-10 paradox: A potent immunoregulatory cytokine that has been difficult to harness for immunotherapy//2015 Jul;74(1):27-34. doi: 10.1016/j.cyto.2014.10.031.
Источник: diagnos.ru
Источник
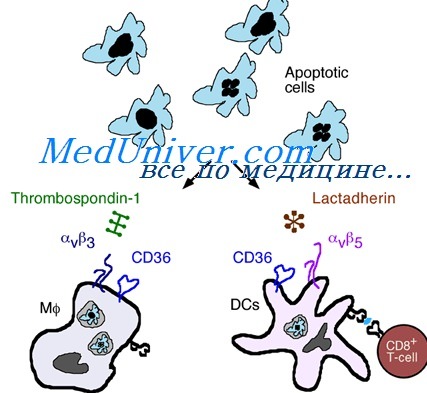
Регуляция иммунного ответа. Влияние интерлейкина-10 (IL-10) на имуннитетОбщепризнано, что иммунный ответ имеет две стороны — повреждающую и защитную. Противоинфекционный иммунный ответ нередко сопровождается сильными воспалительными реакциями. С целью ограничения повреждающего действия иммунной системой в отношении собственных клеток запускаются противовоспалительные механизмы. Как провоспалительные, так и противовоспалительные реакции являются нормальными компонентами иммунного ответа В результате скоординированного действия этих реакций осуществляется борьба против инфекций без развития иммунной патологии Важную роль в формировании противовоспалительного иммунного ответа играют антиген-стимулированные IL-10-продуцирующие регу-ляторные и натуральные супрессорные CD4 Т-клетки. Натуральные супрессорные CD4 Т-клетки начинают формироваться в позднем внутриутробном периоде, независимо от иммунного ответа. После антигенной стимуляции они не продуцируют IL-2 и не могут пролиферировать, но приобретают иммуносупрессирующие свойства по отношению к CD4- и СD8-клеткам. Наивные CD4-клетки после контакта с натуральными регуляторами сами приобретают способность к супрессии — начинают продуцировать TGF-b и IL-10. IL-10-продуцирующие CD4 Т-клетки могут быть индуцированы in vitro и in vivo при антигенной стимуляции. У мышей эти клетки имеют сходные функциональные особенности с натуральными регуляторными Т-клетками (Tregs) — CD4CD25, поскольку они могут ингибировать пролиферацию наивных CD4 Т-клеток независимо от продукции IL-10 через непосредственный клеточный контакт. IL-10-продуцирующие Tregs (IL-10-Tregs) могут быть выделены из TCR-трансгенных, RAG-дефицитных (рекомбинантно активированные гены) мышей, у которых нет натуральных Tregs (N-Tregs) и у которых не экспрессируется спиралевидный транскрипционный фактор Foxp3, необходимый для дифференцировки N-Tregs. IL-10-Tregs также называют индуцибельными Tregs; они могут происходить из CD4- и CD8-лимфоцитов в процессе иммунного ответа и не могут пролиферировать. IL-10-Tregs не могут передавать супрессивные свойства другим Т-клеткам, однако могут подавлять активацию АПК.
IL-10-Tregs ингибируют Т-клеточную экспансию in vivo у человека и у мышей при некоторых моделях заболеваний, таких как, экспериментальный аутоиммунный энцефаломиелит через активацию IL-10-зависимого механизма. Описана также способность натуральных Tregs ингибировать развитие колитов путем продукции IL-10. Адоптивный перенос донорских CD4CD25 регуляторных Т-клеток у мышей предотвращал отторжение трансплантата после аллогенной костной пересадки костного мозга. У людей IL-10-Tregs ограничивают иммунный ответ к антигенам Micobacterium tuberculosis и регулируют репликацию HIV. CD25 N-Tregs регулируют Т-клеточный ответ к HIV-1-специфическим антигенам. Оба типа иммунного ответа (ТЫ и Th2) могут регулироваться как IL-10-Tregs, так и натуральными Tregs. IFN-y-продуцирующие ТЫ клетки обладают способностью уничтожать внутриклеточный патоген, однако при этом могут провоцировать развитие воспалительных патологий. Тh2 клетки играют важную роль в регуляции ответа при гельминтозах, но продукция этими клетками IL-4, IL-5 и IL-13 может приводить к аллергическим манифестациям. К тому же, под воздействием натуральных супрессорных и IL-10-Tregs, Тh1 и Th2 клетки способны реципроктно (взаимно) регулировать дифференцировку и функцию друг друга. Установлено, что IL-10 также продуцируется В-лимфоцитами, макрофагами, ДК и другими Т-клетками, поскольку для многих типов клеток необходима регуляция иммунного ответа через продукцию этого цитокина. При коинкубации плазмоцитоидных ДК с TNF-a, IL-1 и высокими концентрациями IL-10 ДК приобретают свойства превращать CD4- и CD8-клетки в IL-10-Tregs, экспрессирующие CD152; при культивировании плазмацитоидных ДК в присутствии IL-3 + CD40L они приобретают способность дифференцировать CD8 в индуцибельные IL-10-Tregs. Учитывая разнообразие антигенных специфичностей микроорганизмов и их способность мутировать под селективным давлением иммунитета, невозможно заранее предугадать, какие из антигенов будут востребованы иммунной системой для распознавания патогенов при инфекционном процессе. Однако иммунная система имеет механизмы формирования широкого и разнообразного набора специфичностей для борьбы с различными патогенами. Следствием этого процесса является то, что иммунная система способна не только распознавать, но и отвечать на собственные антигены, в результате чего могут возникнуть как легкие, так и тяжелые аутоиммунные расстройства. Нормальный иммунный ответ, адекватно направленный против патогена, также не исключает возможность возникновения нарушений в организме. Это может произойти из-за развития провоспалительных реакций, необходимых для эффективного удаления внедрившегося патогена. Сопутствующие нарушения, наблюдающиеся при этих процессах, иногда причиняют больше вреда хозяину, чем сам патоген, так как при этом продуцируется множество цитокинов Т-клетками, макрофагами и ДК. Данные клетки активируют эффекторный ответ и удаляют патогены, участвуя в провоспалительной и аутоиммунной патологии. Удаление аутореактивных клонов при экспансии Т- и В-клеток, а также индукция анергии периферических лимфоцитов, реактивных к собственным тканям, рассматриваются как главный механизм формирования периферической толерантности. Вместе с тем, исключение сопутствующих нарушений в организме хозяина также достигается путем иммунной супрессии клеток с помощью популяции регуляторных Т-лим-фоцитов. – Вернуться в оглавление раздела “физиология человека” Оглавление темы “Стимуляция врожденного иммунитета”:
|
Источник
Интерлейкины – виды, функция
Интерлейкинами называют растворимые медиаторы, продуцируемые в основном лимфоцитами и моноцитами и оказывающие регуляторное действие на другие клетки иммунной системы или клетки, участвующие в иммунной реакции организма. Многие интерлейкины принимают участие в регуляции дифференцировки и пролиферации клеток-предшественниц гемопоэза. В настоящее время выделено и охарактеризовано более 20 интерлейкинов.
Интерлейкин-1 — это общее название для двух полипептидов — ИЛ-1а и ИЛ-1b с мол. массой 11 000—17 000 Д. Оба они, несмотря на некоторые различия в аминокислотной последовательности, связываются с одним и тем же рецептором на клеточной мембране. Эти молекулы могут синтезироваться различными клетками (Т- и В-лимфоцитами, клетками стромы, эпителиальными клетками), но основным их источником являются мононуклеарные фагоциты и эндотелиальные клетки. Молекулы ИЛ-1 оказывают широкий спектр действия и участвуют в иммунных и воспалительных реакциях. Они оказывают также прямое стимулирующее действие на клетки-предшественницы гемопоэза, а кроме этого, могут вызывать вторичную стимуляцию за счет высвобождения других гемоцитокинов макрофагами и стромальными клетками.
При клинических исследованиях I и II фаз при назначении ИЛ-1 больным после химиотерапии карбоплатином отмечалось некоторое снижение выраженности тромбоцитопении по сравнению с историческим контролем. После трансплантации костного мозга применение ИЛ-1 ускоряло начало восстановления нейтрофилов, но не тромбоцитов. В то же время токсичность данного препарата была достаточно высока. В клинических исследованиях ИЛ-1 вызывал лихорадку, гипотонию, потливость, миалгии и снижение массы тела, что ухудшает перспективы его клинического применения.
Интерлейкин-2, или, как его называют, Т-клеточный фактор роста, представляет собой гликопротеин с мол. массой около 15 000 Д. Он продуцируется активированными Т-лимфоцитами и медуллярными тимоцитами. К основным его эффектам относят запуск пролиферации антигенактивированных Т-лимфоцитов и стимуляцию NK-лимфоцитов. Препарат нашел клиническое применение при лечении рака почки и злокачественной меланомы. Кроме того, инкубирование активированных in vitro лимфоцитов с ИЛ-2 повышает противоопухолевые свойства этих клеток, используемых в клеточной иммунотерапии.
Интерлейкин-3 (мультиКСФ, или гематопоэтин) является гликопротеином с мол. массой 14 000— 20 000 Д в зависимости от степени гликозилирования. Ген, кодирующий ИЛ-3, расположен на длинном плече хромосомы 5, рядом с геном ГМ-КСФ, но, видимо, имеет отличающиеся механизмы регуляции транскрипции. Основным источником ИЛ-3 являются активированные Т-лимфоциты, хотя он может синтезироваться кератиноцитами, клетками эпителия тимуса и некоторыми другими. В исследованиях in vitro ИЛ-3 стимулирует пролиферацию ранних предшественников гемопоэза, дающих рост смешанных колоний клеток различных линий: эритроцитарных, гранулоцитарных, моноцитарных и мегакариоцитарных. Кроме того, он оказывал стимулирующее действие и на более поздние, коммитированные или дифференцированные, клетки-предшественницы. Это стимулирующее действие в гораздо большей степени проявляется в комбинации с такими цитокинами, воздействующими на поздние клетки-предшественницы, как Г-КСФ, ГМ-КСФ, эритропоэтин и др..
Клинические исследования по применению рекомбинантного ИЛ-3 после химиотерапии показали его способность несколько снижать выраженность нейтропении и тромбоцитопении. В то же время препарат оказался достаточно токсичным. У большого числа больных его применение сопровождалось лихорадкой, потливостью, головной болью, крапивницей, миалгиями и артралгиями.
В одном исследовании ИЛ-3 в монотерапии или в комбинации с ГМ-КСФ показал высокую эффективность в мобилизации клеток-прешественниц гемопоэза крови. Помимо этого, ИЛ-3 можно использовать для увеличения числа клеток-предшественниц in vitro. Предварительная инкубация костного мозга с ИЛ-3 несколько ускоряет восстановление гемопоэза после трансплантации костного мозга.
Интерлейкин-4, или В-клеточный фактор роста, — это протеин с мол. массой около 20 000 Д. Он продуцируется в основном субпопуляцией хелперных Т-лимфоцитов, а также тучными клетками, макрофагами и клетками стромы. ИЛ-4 оказывает множественные эффекты на иммунную систему. В частности, он вместе с другими цитокинами вызывает пролиферацию В-лимфоцитов, регулирует секрецию иммуноглобулинов. ИЛ-4 стимулирует пролиферацию покоящихся Т-лимфоцитов и усиливает их противоопухолевое действие.
ИЛ-4 обладает синергизмом с другими цитокинами, стимулирующими колониеобразующую активность клеток-предшественниц гемопоэза. Он является фактором роста тучных клеток.
Первые клинические исследования рекомбинантного ИЛ-4 выявили значительное побочное действие препарата: слабость, лихорадку и задержку жидкости. Отмечались также заложенность носа, поражения слизистой оболочки желудочно-кишечного тракта с язвообразованием, иногда с развитием кровотечения.

Интерлейкин-5, или фактор дифференцировки эозинофилов, представляет собой протеин с мол. массой около 18 000 Д; синтезируется в основном хелперными Т-лимфоцитами и тучными клетками. ИЛ-5 стимулирует пролиферацию В-лимфоцитов и усиливает синтез ими IgA и IgM. Кроме того, в комбинации с ИЛ-3 он может увеличивать продукцию эозинофилов костным мозгом.
Интерлейкин-6, или ИФН-b2, имеет мол. массу около 26 000 Д. Основным клеточным источником данного цитокина являются Т-лимфоциты, моноциты, макрофаги, фибробласты и эндотелиальные клетки. Он, так же как ИЛ-3, относится к мультифункциональным цитокинам: стимулирует пролиферацию многих клеточных линий. ИЛ-6 имеет частичную гомологию с ИЛ-12. Помимо клеток-предшественниц гемопоэза, ИЛ-6 действует как фактор роста и дифференцировки В-лимфоцитов, гепатоцитов, нейронов. При воздействии на Т-лимфоциты ИЛ-6 вызывает продукцию ими ИЛ-2.
Одним из наиболее важных эффектов ИЛ-6 с клинической точки зрения является его стимулирующее влияние на тромбоцитопоэз. Это действие цитокина показано на экспериментальных моделях. Назначение ИЛ-6 животным, получавшим химиотерапию, сопровождалось, помимо увеличения числа тромбоцитов, также увеличением размеров и плоидности мегакариоцитов. ИЛ-6 не является фактором роста мегакариоцитов, так как он не увеличивает общее их число и количество колониеобразующих единиц мегакариоцитов в костном мозге. Его уровень не повышается при тромбоцитопении, но растет при реактивных тромбоцитозах. Введение данного цитокина в течение 10 дней больным, не получающим химиотерапию, сопровождается увеличением числа тромбоцитов до двухкратного от исходного уровня. Содержание лейкоцитов при этом несколько увеличивается, кроме того, развивается гипохромная анемия, сопровождающаяся снижением содержания железа в сыворотке крови. Возможно, этот эффект связан с задержкой жидкости. В нескольких клинических исследованиях I фазы применение рекомбинантного ИЛ-6 ускоряло восстановление числа тромбоцитов после химиотерапии, что также отмечалось после высокодозной химиотерапии с аутологичной трансплантацией костного мозга. Показано, что миеломные клетки продуцируют ИЛ-6 и экспрессируют рецепторы к данному цитокину. У большинства пациентов с прогрессированием миеломной болезни уровень ИЛ-6 в крови повышен, что послужило основанием для попыток его блокирования у больных миеломой, резистентных к химиотерапии.
Применение ИЛ-6 сопровождается дозозависимы-ми побочными действиями, включающими лихорадку, головную боль, слабость, при более высоких дозах отмечаются анемизация и преходящая почечная и печеночная дисфункция.
Интерлейкин-7 представляет собой полипептид с мол. массой около 25 000 Д; синтезируется клетками стромы костного мозга и фетальными клетками печени. Его относят к наиболее ранним факторам роста Т- и В-лимфоцитов. Он может способствовать дифференцировке стволовой клетки в пре-Т-и пре-В-клетки. Данный интерлейкин индуцирует секрецию других цитокинов моноцитами человека.
Интерлейкин-8 (активирующий нейтрофилы протеин 1) — полипептид с мол. массой около 8000 Д. Синтезируется моноцитами, макрофагами, эндотелиальными и некоторыми другими клетками. Эффект ИЛ-8 на полиморфно-ядерные нейтрофилы включает активацию хемотаксиса вместе с повышением экспрессии молекул адгезии на поверхности этих клеток (CD11b/CD18) и увеличение выброса перекисных соединений. В то же время ИЛ-8 ингибирует адгезию нейтрофилов к эндотелиальным клеткам, активированных провоспалительными цитокинами, препятствуя повреждению эндотелия.
Влияние ИЛ-8 на гемопоэз заключается в торможении колониеобразующей активности ранних миелоидных предшественников.
Интерлейкин-9 — это гликопротеин с мол. массой 40 000 Д, который также называют Т-клеточным фактором роста III. Клеточным источником ИЛ-9 являются Т-лимфоциты. Он способен потенцировать синтез IgE В-лимфоцитами, стимулированными ИЛ-4. Кроме того, он вызывает пролиферацию активированных хелперных Т-лимфоцитов. Влияние ИЛ-9 на гемопоэз заключается в стимуляции колониеобразующей активности ранних эритроидных предшественников.
Интерлейкин-10, или фактор, ингибирующий синтез цитокинов, представляет собой полипептид с мол. массой 17 000—21 000 Д; синтезируется макрофагами, хелперными Т-лимфоцитами, В-лимфоцитами и кератиноцитами. Данный цитокин стимулирует пролиферацию и активирует В-лимфоциты. ИЛ-10 способен ингибировать синтез цитокинов хелперными Т-лимфоцитами. Он также ингибирует активность макрофагов и синтез ИФН-у-активироваными киллерными лимфоцитами. Вместе с ИЛ-3 и ИЛ-4 данный цитокин стимулирует пролиферацию предшественников тучных клеток.
Интерлейкин-11 представляет собой полипептид с мол. массой около 24 000 Д; синтезируется стромальными фибробластами. Он оказывает стимулирующее действие на клетки-предшественницы гемопоэза (но не на самые ранние стволовые клетки), В-лимфоциты и остеокласты. В комбинации с ИЛ-3 и фактором стволовых клеток вызывает пролиферацию ранних предшественников гемопоэза. ИЛ-11 обладает способностью увеличивать плоидность мегакариоцитов и ускорять созревание их предшественников. Исследования на животных показали, что данный цитокин ускоряет восстановление всех 3 ростков кроветворения после химиотерапии. Биологическое действие ИЛ-11 близко к таковому ИЛ-6, что предполагает наличие общего рецептора или частичного совпадения пути передачи сигнала к ядру клетки.
При клинических испытаниях I—II фазы у больных раком молочной железы, получавших ИЛ-11 без химиотерапии и после нескольких химиотерапевтических циклов, было выявлено стимулирующее действие цитокина на тромбоцитопоэз. Вне химиотерапии ИЛ-11 вызывал дозозависимое увеличение числа тромбоцитов крови в 2—3 раза, при этом уровень лейкоцитов не изменялся и отмечалась анемизация. Причиной анемии, возможно, являлась ге-модилюция, связанная с задержкой жидкости. Назначение рекомбинантного препарата после химиотерапии циклофосфаном и доксорубицином сокращало содержание тромбоцитов пропорционально дозе препарата. Исследование костного мозга больных, получавших ИЛ-11, показало увеличение числа мегакариоцитов при использовании препарата в дозе 50 мкг/кг в день и более.
Переносимость рекомбинантного ИЛ-11 при дозах, не превышающих 50 мкг/кг, относительно удовлетворительная. Из осложнений отмечаются слабость, миалгии и артралгии. При более высоких дозах наблюдались отеки конечностей.
Интерлейкин-12 представляет собой гетеродимерный протеин с мол. массой 75 000 Д (мономеры 35 000 и 40 000 Д). Продуцируется активированными макрофагами и В-лимфоцитами. Основным действием этого цитокина является стимулирование клеточного иммунитета путем активации Т-лимфоцитов и натуральных киллерных клеток. Уровень ИЛ-12 повышается при инфекции, а его назначение экспериментальным животным повышало устойчивость к внутриклеточным патогенам. Данный цитокин повышает цитолитическую активность лимфоцитов против клеток опухоли, он способен снижать выраженность реакции «трансплантат против хозяина» в эксперименте.
Влияние ИЛ-12 на гемопоэз заключается в его синергизме с ИЛ-3 и фактором стволовых клеток в стимулировании пролиферации ранних предшественников гемопоэза. Кроме того, он ускоряет образование мультилинейных колоний клетками-предшественницами гемопоэза в комбинации с ИЛ-11 и фактором стволовых клеток.
Интерлейкин-13 — полипептид с мол. массой около 20 000 Д. Основным клеточным источником его являются Т-лимфоциты. Он вызывает пролиферацию и дифференцировку В-лимфоцитов, активированных ИЛ-9. Кроме того, ИЛ-13 стимулирует синтез ими IgE, а также увеличивает экспрессию антигенов второго класса основного комплекса гистосовместимости на их поверхности. При воздействии на активированные макрофаги ИЛ-13 снижает их прокоагулянтную активность.

Интерлейкин-14 — белок с мол. массой около 60 000 Д; синтезируется Т-лимфоцитами. Обладает способностью стимулировать пролиферацию В-лимфоцитов и ингибировать секрецию иммуноглобулинов.
Интерлейкин-15 (интерлейкин Т) представляет собой полипептид с мол. массой около 14 000 Д, обладающий способностью вызывать пролиферацию Т-лимфоцитов и активировать их подобно ИЛ-2.
Интерлейкин-16 — это полипептид с мол. массой около 17 000 Д, синтезируется Т-лимфоцитами, клетками тимуса, селезенки и др. ИЛ-16 обладает способностью вызывать пролиферацию Т-лимфоцитов и активировать хелперные Т-лимфоциты.
Интерлейкин-17 представляет собой гомодимерный протеин с мол. массой 60 000 Д. Он продуцируется хелперными Т-лимфоцитами. Основным действием данного цитокина является стимулирование секреции ИЛ-6, ИЛ-8 и ГМ-КСФ эпителиальными клетками, эндотелием и фибробластами.
Интерлейкин-18 — это полипептид с мол. массой около 18 000 Д, синтезируется моноцитами и макрофагами. Данный цитокин способен значительно увеличивать продукцию ИФН-у и повышать активность NK-лимфоцитов.
Интерлейкины-19, -20, -22, -24 объединены структурной близостью к ИЛ-10. Кроме того, они взаимодействуют с общим рецепторным комплексом на поверхности клетки. В то же время биологические эффекты этих цитокинов отличны. ИЛ-19 активирует лимфоциты, ИЛ-20 участвует в регуляции роста эпителия, ИЛ-22 увеличивает продукцию провоспалительных цитокинов, а ИЛ-24 стимулирует апоптоз опухолевых клеток.
Интерлейкин-21 вызывает апоптоз активированных В-лимфоцитов и стимулирует гепатоциты.
Интерлейкин-23 играет критическую роль при возникновении аутоиммунных воспалительных процессов в мозге.
Интерлейкин-25 усиливает аллергическую реакцию за счет повышения экспрессии генов ИЛ-4, ИЛ-5 и ИЛ-13.
Интерлейкин-26 вырабатывается Т-клетками; его продукция значительно усиливается при вирусной инфекции.
Интерлейкин-27 структурно близок к ИЛ-12, стимулирует наивные Т4-лифоциты.
Интерлейкины-28 и -29 структурно близки к интеферонам I типа. Их продукция также усиливается при вирусной инфекции, они обладают противовирусной активностью.
– Также рекомендуем “Фактор роста и развития мегакариоцитов (ФРРМ) – строение, функции”
Оглавление темы “Клиническое применение гемопоэтических факторов роста”:
- Гемопоэтические факторы роста (гемоцитокины) – функции, участие в гемопоэзе
- Интерлейкины – виды, функция
- Фактор роста и развития мегакариоцитов (ФРРМ) – строение, функции
- Профилактика нейтропении и ее инфекционных осложнений – рекомендации
- Цитокины в химиотерапии острых нелимфобластных лейкозов – эффективность
- Цитокины в лечении нарушений образования и созревания нейтрофилов – эффективность
- Побочные эффекты Г-КСФ – токсичность филграстима
- Побочные эффекты ГМ-КСФ – токсичность молграмостима
- Дозировки и методы введения Г-КСФ – филграстима, ленограстима
- Дозировки и методы введения ГМ-КСФ – молграмостима, са