Иммунный ответ при воспалении
Оглавление темы “Селезенка. Лимфатические узлы. Стадии иммунного ответа. Формы иммунного ответа. Воспаление. Механизмы, контролирующие иммунную систему.”: Стадии иммунного ответа. Формы иммунного ответа. Воспаление. Ранний защитный воспалительный ответ.Ранний защитный воспалительный ответ призван препятствовать внедрению и распространению возбудителя, по возможности быстро удалять его из организма. Ранний защитный воспалительный ответ разыгрывается в течение первых 4 сут после внедрения возбудителя. Ранний защитный ответ против внедрившихся в организм патогенных микроорганизмов обеспечивается факторами врожденного иммунитета, к которым относятся фагоцитирующие клетки крови и тканей, естественные киллеры, циркулирующие в крови белковые молекулы, обладающие защитными свойствами (компоненты системы комплемента и др.), а также межклеточные медиаторы — цитокины. Ранний воспалительный ответ стимулирует последующий специфический иммунный ответ, влияет на его форму, способствуя развитию наиболее эффективного против конкретного микроорганизма специфического иммунного ответа.
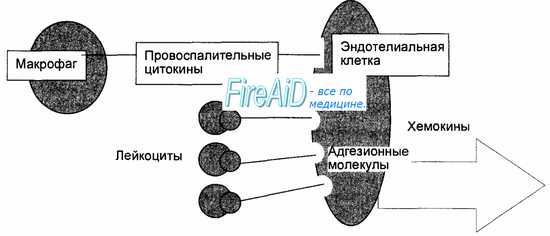
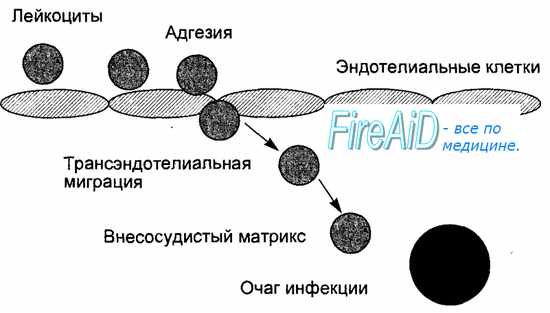
Ранний воспалительный ответ начинается с привлечения лейкоцитов из кровяного русла в очаг инфекции с последующей их активацией для удаления возбудителя (рис. 8.6). Мобилизация лейкоцитов в очаг инфекции стимулируется провоспалительными цитокинами, а опосредуется адгезионными молекулами на поверхности лейкоцитов и эндотелиальных клеток, а также молекулами хемокинов и их рецепторами. Провоспалительные цитокины (туморнекротизирующий фактор—ТНФ, интерлейкин-1 — ИЛ-1) продуцируются и секретируются макрофагами при фагоцитозе возбудителя. Под действием этих цитокинов на поверхности эндотелиальных клеток, появляются адгезионные молекулы вначале для нейтрофилов, а затем для моноцитов и лимфоцитов, ответственные за прилипание лейкоцитов к эндотелию сосудов. Кроме того, активированные цитокинами эндотелиальные клетки продуцируют хемокины, достигающие высокой концентрации на уровне очага инфекции (рис. 8.7). Этим обеспечивается прочная адгезия лейкоцитов к эндотелиальным клеткам с последующей их трансэндотелиальной миграцией и выходом в ткани в направлении очага инфекции (см. рис. 8.6). Таким образом, ранний воспалительный ответ проявляется инфильтрацией очага инфекции фагоцитирующими клетками, где эти клетки получают дополнительные сигналы активации от микробных продуктов и компонентов (липополисахарид клеточной стенки бактерий), от компонентов активированной системы комплемента и от провоспалительных цитокинов, в том числе, от гамма-интерферона, продуцируемого и секретируемого активированными естественными киллерами. Активированные фагоцитирующие клетки приобретают повышенную способность убивать захваченных микробов, что способствует удалению возбудителя. Активированные под влиянием провоспалительных цитокинов эндотелиальные клетки продуцируют молекулы вазодилататоров, под действием которых усиливается местный кровоток, повышается проницаемость сосудов для макромолекул фибриногена, который, покидая сосуды, превращается в фибрин, что способствует ограничению очага инфекции. В случае попадания в организм небольшого количества низковирулентных возбудителей ранний воспалительный ответ подавляет очаг инфекции.
Удаление из кровяного русла попавших в кровь единичных бактериальных клеток является функцией системы комплемента. Большая часть компонентов комплемента синтезируются гепатоцитами и мононуклеарными фагоцитами. Компоненты комплемента (С1, С2, СЗ, С4, С5, С6, С7, С8, С9, факторы В и D) содержатся в крови в неактивной форме. При попадании в кровяное русло бактерий на их поверхности каскад ферментативных реакций ведет к последовательной активации компонентов системы комплемента («альтернативный путь активации») с формированием мембран-атакующего комплекса (С5—С9), вызывающего лизис бактерий. В процессе активации системы комплемента накапливаются фрагменты, которые опосредуют разные биологические эффекты: привлечение лейкоцитов в очаг инфекции или воспаления (хемотаксис) — фрагмент С5а, усиление фагоцитоза (опсонизацию) — СЗb, индукцию синтеза и секреции медиаторов воспаления — С3а, С5а. (При развитии специфического иммунного ответа и появлении в кровяном русле комплексов антиген—антитело другой каскад ферментативных реакций ведет к активации системы комплемента — «классический путь активации») – Также рекомендуем “Представление антигена. Распознавание антигена. Взаимодействие Т-хелперов ( Тh1 ) с антигенпредставляющими клетками.” |
Источник
Иммунная система. ВоспалениеИммунная система и процесс воспаления участвуют в защите организма от проникающих в него микроорганизмов, отвечая на повреждение. Однако неадекватная активация этих систем приводит к широкому спектру воспалительных нарушений. Воспаление характеризуется следующими признаками: • расширением сосудов, ведущим к покраснению тканей; Физиология воспалительного процесса обладает некоторыми сходными характеристиками с физиологией повреждения. Реакции, которые они опосредуют, имеют цель обеспечить ответ организма на вторжение микроорганизмов, стресс или увеличение местного кровотока в области повреждения, обеспечивая тем самым миграцию в эту область лейкоцитов и других форменных элементов крови. Реакции обеспечивают выполнение большого количества важных процессов: возникновение боли в попытке уменьшить степень повреждения, изменение местной среды для уменьшения концентрации повреждающих веществ и миграцию лейкоцитов для уничтожения микроорганизмов.
Кроме того, многие аутакоиды, выделяемые в ответ на повреждение или инфекцию, вызывают увеличение сосудистой проницаемости, приводящее к отеку, и обеспечивают процесс регенерации и защиты ткани, который в случае неадекватности может приводить к изменению функции ткани. Ключевой дополнительной характеристикой иммунного ответа является способность лимфоцитов распознавать чужеродные белки (антигены), которые могут быть поверхностными белками на патогенах или, у некоторых людей, совершенно безвредными белками (такими как пыльца растений или чешуйки кожи животных), вызывающими аллергические реакции. Лимфоциты образуются из стволовых клеток костного мозга, затем в тимусе развиваются Т-лимфоциты, а в костном мозге — В-лимфоциты. Т-лимфоциты имеют на своей поверхности антигенные Т-клеточные рецепторы. Т-лимфоциты специфически распознают антигены, ассоциированные с главным комплексом гистосовместимости (HLA-антигены), на антигенпрезентирующих клетках — макрофагах и дендритных клетках. В случае активации Т-лимфоцитов посредством антигена через Т-клеточные рецепторы продуцируются растворимые белки, называемые цитокинами, которые передают сигнал Т-лимфоцитам, В-лимфоцитам, моноцитам/макрофагам и другим клеткам. Т-лимфоциты классифицируют на два подвида: – Также рекомендуем “В-лимфоциты. Причины начала воспаления” Оглавление темы “Препараты влияющие на иммунную систему”: |
Источник
4.1. Иммунный ответ при воспалении.
Воспаление – это первая линия иммунной защиты и реализуется клетками и гуморальными факторами, для которых стимулом их функциональной активности является само повреждение. Однако не только повреждение инициирует воспаление. Нельзя исключить участие в этом процессе бактериальных липополисахаридов и пептидогликанов, которые несвойственны нормальным клеткам. Однако нам представляется, что наиболее универсальной мишенью для ориентации иммунокомпетентных клеток и гуморальных факторов на реализацию воспалительной реакции являются концевые сахара (манноза) мембранных гликопротеинов и гликолипидов, освобождающиеся в результате повреждения, трансформации, усиленной пролиферации или старения клетки. Это, так называемое “универсальное чужое” без дифференциации на индивидуальные антигены. Совершенно прав А. А. Ярилин (1999), который говорит, что “на уровне первой линии защиты понятие антиген не имеет смысла”. Мы не будем останавливаться на деталях и этапах воспалительного процесса, которые достаточно хорошо описаны и всем известны. Выделим только главное, необходимое для понимания логики иммунитета и возможных механизмов его участия в повреждении.
Основными действующими лицами воспаления являются нейтрофилы, макрофаги/моноциты, NK-клетки, иногда эозинофилы, система комплемента, воспалительные цитокины (ИЛ-1, ИЛ-6, ФНО-альфа, интерфероны), белки острой фазы, БАВ (кинины, гистамин, гепарин, простагландины, лейкотриены и др.). В своем взаимодействии они способствуют локализации и уничтожению патогена. Главный удар на себя в этом процессе берут нейтрофилы и макрофаги/моноци- ты. Нейтрофилы не только фагоцитируют, но и могут осуществлять внеклеточный цитолиз, а также секрецию цитокинов и других БАВ. Благодаря возможности развития внеклеточного цитолиза, длительно существующее воспаление может способствовать повреждению собственных тканей и приобретать все черты локального аутоиммунного процесса, особенно если для участия в ликвидации патогена привлекаются эозинофилы, известные своим приоритетом в реализации внеклеточного цитолиза.
Чрезвычайно важным является участие в воспалении макрофагов/моноцитов. Становится понятной столь значимая роль этих клеток в презентации антигена и запуске специфичного иммунного ответа. Первично контактируя с патогеном макрофаги/моноциты не только участвуют в его ликвидации, но и презентируя его антигены инициируют присоединение следующего более мощного этапа, включающего весь арсенал иммунной системы (клеточный, гуморальный иммунитет, ГНТ, ГЗТ) уже специфически ориентированный на данные антигены. Естественно, что это относится к тимусзависимым антигенам, однако в последнее время появились данные о существовании презентации и при тимуснезависимых антигенах. Специфический этап – это не только более мощный, но и более качественный этап защиты, поскольку специфическая ориентация практически исключает возможность повреждения нормальных структур организма, существующую при обычном воспалении. Специфический этап лимитирует возможности повреждения организма патогеном. Надо думать, что подключение специфического этапа снимает необходимость в воспалительной реакции, а время развертывания этого этапа определяет длительность существования клинической картины заболевания. Логическим завершением этого этапа является не только полноценная и качественная санация от патогена, но и создание иммунологической памяти, обеспечивающей оперативную защиту при повторном попадании антигена без какого-либо ущерба для организма.
Таким образом, длительное существование воспалительного процесса (хроническое воспаление) однозначно свидетельствует о несостоятельности специфического этапа иммунного ответа, связанного со структурными или функциональными дефектами в иммунной системе и всегда является риском развития иммунопатологии.
Приведенные данные позволяют более четко представить логику взаимосвязи неспецифического и специфического в обеспечении рационального и качественного иммунного ответа. Вместе с тем, нет единого мнения о центральной роли макрофагов/моноцитов, участвующих в воспалительной реакции, в инициации специфического этапа. А. А. Ярилин (1999) считает, что эти клетки не могут значимо участвовать в презентации антигена, поскольку они не мигрируют в лимфатические узлы и в активированном состоянии делят антиген на слишком мелкие фрагменты. Однако известный факт более качественного иммунитета после перенесенной болезни по сравнению с вакцинацией позволяет считать, что презентация антигена из очага воспаления обеспечивает лучший иммунный ответ по сравнению с другими источниками. По крайней мере, для кожи такие клетки известны – это клетки Лангерганса или белые эпидермиоциты, которые, захватывая в очаге поражения антиген, мигрируют в лимфоузлы по пути трансформируясь в дендритные клетки. Что касается слизистых – требуются дальнейшие исследования, однако не считаться со значимостью макрофагов/моно- цитов в этом процессе в настоящее время нельзя.
Раздел: Медицинские науки
Количество знаков с пробелами: 265451
Количество таблиц: 0
Количество изображений: 0
… показало, что эпидемия аллергии вызвана не загрязнением воздуха. Если бы виной аллергии было загрязнение окружающей среды, то астма получила бы более широкое распространение в Восточной Германии. При этом эпидемическая аллергия не является некоторым видом генетического заболевания. До недавнего времени большинство экспертов полагало, что аллергия передается по наследству. Если у обоих родителей …
… разнообразными нарушения функций легких (эозинофильные пневмонии, бронхиальная астма), желудочно-кишечного тракта, сердечнососудистой системы, почек и других органов. Особое место занимают лекарства в возникновении больших коллагенозов. Проявления лекарственной аллергии многообразны. Наиболее частыми симптомами лекарственной аллергии оказались: экзантема, отек лица и слизистой оболочек, падение …
… способствуют социальные и общебиологические причины, такие как: 1. Нарастающее загрязнение окружающей среды: атмосферного воздуха, водоемов, почвы. 2. Изменение питания. В развитие аллергических заболеваний кожи оказывает влияние несбалансированное питание: употребление большого количества жирной и жаренной пищи, сладостей, что существенно усиливает нагрузку на ферментную систему …
анизмы развития аллергических заболеваний у спортсменов до настоящего времени мало изучены. Цель исследования – изучение влияния интенсивных физических нагрузок на развитие аллергии немедленного типа. Материал и методы. Так как моделирование аллергических реакций (АР) на спортсменах чревато осложнениями, исследования проводились на морских свинках по следующим схемам: схема 1 – АР моделировалась …
Источник
Эта форма иммунного ответа предназначена для защиты от внутриклеточных патогенов, локализующихся в цитоплазматических гранулах — микроорганизмов, фагоцитированных клетками, но не разрушенных из-за недостатка адекватных эффекторных механизмов или их блокады патогенами. Типичные представители таких патогенов — различные виды микобактерий, а также многие простейшие (например, лейшмании, хламидии), риккетсии, плазмодии, грибы (кандиды) и др.
Клеточный иммунный ответ воспалительного типа осуществляется в 4 этапа (рис. 3.109).
- Презентация дендритными клетками антигена CD4+ Т-лимфоци- там, приводящая к их активации.
- Развитие хелперных Т-лимфоцитов типа ТЫ.
- Презентация антигена макрофагами ранее сформировавшимся Т-хелперам (ТЫ-типа), их взаимная активация и выделение цитокинов.
- Активация цитолиза в фагосомах макрофагов.
За реализцию этой формы защиты отвечают Thl-клетки и макрофаги. Thl-клетки формируются на этапе запуска иммунного ответа и отвечают за специфическую составляющую реакции (распознавание антигена и направление реакции на его носителя). Макрофаги выступают в качестве эффекторных клеток. Начальный этап реакции против внутриклеточных патогенов, локализованных в фаголизосомах, осуществляется так же, как при запуске любой формы иммунного ответа: дендритные клетки, захватившие патоген или его фрагмент, презентируют антигенный пептид CD4+ Т-клеткам, которые активируются, пролиферируют и дифференцируются в хелперные Т-лимфоциты. Уже на этапе распознавания антигена происходит ориентация дифференцировки CD4+ Т-лимфоцитов в хелперы Thl-типа, которая затем поддерживается цитокинами, продуцируемыми дендритными клетками — IL-12, IFNy (см. раздел 2.5.5.5).

Рис. 3.109. Схема развития клеточного иммунного ответа воспалительного типа
Активирующее взаимодействие Thl-клеток с макрофагами
Этот этап характерен именно для воспалительного иммунного ответа. Он состоит во взаимодействии специфических TM-клеток с макрофагами, которые содержат на своей поверхности молекулы MHC-II, несущие пепидный фрагмент антигена. При взаимодействии формируется иммунный синапс. В результате генерируются активирующие сигналы, направленные как в ТЫ-клетку, так и в макрофаг. В TW-лимфоцит сигналы поступают через молекулы TCR/CD4 и CD28. В результате этой повторной стимуляции Т-клетки (первая стимуляция была вызвана презентацией антигена дендритной клеткой) происходит усиление выработки цитокинов, важных для реализации последующих событий (в частности IFNy и TNFa).
Стимуляция макрофага при взаимодействии с TW-клеткой реализуется с помощью двух механихмов (рис. 3.110). Один из них — контактный — через костимулирующую молекулу CD40, с которой связывается ее лиганд CD154. CD40 спонтанно экспрессируется макрофагами, тогда как ее лиганд появляется на поверхности TM-клеток в результате активации при формировании иммунного синапса. В передаче сигнала от молекулы CD40 участвуют адапторные факторы TRAF-1, TRAF-2, TRAF-6. В результате происходят активация фактора NF-kB и запуск Rac-зависимой ветви MAP-каскада, завершающейся формированием транскрипционного фактора с-Jun. Второй механизм активации опосредуется IFNy. При связывании этого цитокина с рецептором включается сигнальный путь, вовлекающий киназы Jak1 и Jak2, транскрипционный фактор STAT1, а также дополнительные пути с участием MAP-каскада.
Результат активации макрофагов — экспрессия многочисленных генов, приводящая к повышению содержания на поверхности клетки молекул MHC-I и особенно MHC-II, сборке NADPH-оксидазы, активации ферментов окислительного метаболизма. Наиболее специфичное проявление ответа макрофагов на стимулирующее действие IFNy — экспрессия гена индуцибельной NO-синтазы. Именно NO и его производные, такие

Рис. 3.110. Активация макрофагов Т-хелперами. Показаны механизмы воздействия Thl-клеток на макрофаги (контактный и опосредованный цитокинами), а также индуцируемые Т-клетками проявления активации макрофагов
как пероксинитрит (ОО*NO), вызывают гибель микобактерий и других внутриклеточных патогенов, сохранявшихся и даже размножавшихся в фагосомах. Все эффекты IFNy, в том числе способность индуцировать образование NO-синтазы, усиливаются TNFa, продуцируемым как Th1- клетками, так и самими макрофагами. Эффективность действия цитокинов, вырабатываемых TM-клетками, существенно повышается в связи с сосредоточением их секреции в области контакта с макрофагами. Это, кроме того, уменьшает активацию посторонних клеток и их повреждение. Для обеспечения этой ориентированной секреции необходима поляризация клеток в ходе формирования иммунного синапса.
Особого внимания заслуживает взаимодействие цитокинов IL-12 и IFNy при воспалительном иммунном ответе (рис. 3.111). Экспрессия IL-12 в макрофагах индуцируется при связывании PAMP с TLR. Экспрессия гена IL12 — один из результатов сигнального пути, вовлекающего адапторный белок MyD88 и транскрипционный фактор NF-kB. IL-12 играет решающую роль в индукции дифференцировки TM-клеток и стимулирует выработку этими клетками IFNy, один из важнейших эффектов которого — усиление выработки макрофагами IL-12. Таким образом, эти цитокины вместе с рецепторами и сигнальными путями, ответственными за экспрессию их генов, образуют единую функциональную систему, которой принадлежит ключевая роль в реализации воспалительной формы клеточного иммунного ответа. Дефекты в любом звене этой системы приводят к развитию иммунодефицитов, сопровождающихся повышенной чувствительностью к микобактериям и другим патогенам, в ответ на которые вовлечены ТЫ-клетки и макрофаги.
Воспалительная составляющая Thl-клеточного иммунного ответа
В отличие от цитотоксического иммунного ответа, не связанного очевидным образом с воспалительной реакцией, иммунный ответ, опосредованный TW-клетками, полностью реализуется в ее рамках. Запуск ответа происходит по классической схеме. В очаге инфицирования (обычно в

Рис. 3.111. Роль интерферона у в дифференцировке и реализации функций Т-хел- перов. Интерферон у, продуцируемыйклеткамиврожденногоиммунитета, определяет направление развития адаптивного иммунного ответа, в ходе которого он также секретируется Thl-клетками и активирует основные эффекторы воспалительной формы клеточного ответа — макрофаги
барьерных тканях) дендритные клетки поглощают патоген или его фрагмент и транспортируют его в региональный лимфатический узел или иные вторичные лимфоидные органы. Дифференцировавшиеся специфические ХЫ-клетки поступают в рециркуляцию. Подобно цитотоксическим Т-лимфоцитам, они утрачивают мембранные молекулы, направляющие их миграцию в лимфоидные органы (CD62L, CCR7) и приобретают обычные свойства эффекторных клеток, включая усиленную экспрессию мембранных интегринов (LFA-1, VLA-4) и рецепторов для хемокинов, секретируе- мых в очагах воспаления и барьерных тканях (для Thl-клеток — CXCR3, CCR5, CCR2 и др.).
Оказавшись в очагах инфицирования, Thl-клетки в кооперации с макрофагами осуществляют реакции, описанные выше. В результате взаимодействия этих клеток, особенно действия IFNy, происходит максимально выраженная активация макрофагов. Эта активация результативна с точки зрения защиты от внутриклеточных патогенов, но деструктивна для окружающих тканей. Активированные макрофаги выделяют весь спектр своих секреторных продуктов. Он включает разнообразные провоспалительные факторы и факторы бактерицидности. К последним относят активные формы кислорода, их галоидные производные, оксид азота и его дериваты, ферменты и т.д. Среда в окружении таких клеток закисляется. Поскольку контакт макрофагов с Thl-клетками к этому моменту прекращается, секреция уже не носит ориентированного характера. Выделяемые молекулы выступают как факторы внеклеточной
микробицидности и одновременно вызывают повреждение окружающих нормальных клеток организма. Таким образом, продукты Th1-клеток дополнительно усиливают воспалительную реакцию, в то же время придавая ей специфичность в отношении конкретных возбудителей.
Вариант воспаления, реализуемый с участием Th1-клеток, называют иммунным воспалением, а сам Th1-клеточный иммунный ответ носит название воспалительного клеточного иммунного ответа. В рамках этой формы иммунного ответа особенно ярко проявляется соотношение факторов врожденного и адапативного иммунитета: эффекторным механизмом служит типичная реакция врожденного иммунитета — фагоцитоз, однако он усиливается и приобретает специфичность в отношении конкретных антигенов благодаря вовлечению в реакцию клеток адаптивного иммунитета.
Гранулема

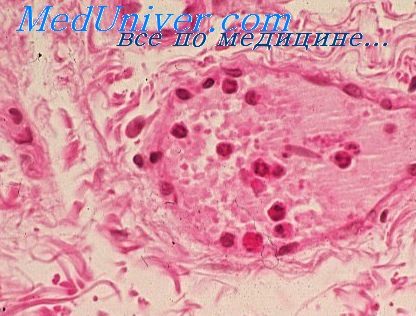
При неэффективном клеточном ответе воспалительного типа, т.е. в случаях, когда разрушения и переваривания внутриклеточных патогенов не происходит, формируется гранулема (рис. 3.112). Гранулема представляет собой морфологическую структуру округлой формы, в центре которой расположены инфицированные макрофаги, а также клеточный детрит и патогены, освободившиеся в результате разрушения макрофагов. Вследствие слияния макрофагов образуются гигантские многоядерные клетки. Некоторые макрофаги претерпевают морфологические изменения, приобретая фенотип так называемых эпителиоидных клеток. Периферическая часть гранулемы образована активированными макрофагами, лишенными патогенов, и Т-лимфоцитами (преимущественно TM-клетками). Т-клетки постоянно
перемещаются, причем эта подвижность важна для сохранения структурной целостности гранулемы. Формирование гранулемы сопряжено с деструкцией ткани и нарушением функционирования большого участка пораженных органов (например, легких при туберкулезе), что делает ее патологическим образованием. С другой стороны, гранулема представляет способ изоляции патогена, с уничтожением которого иммунная система не справляется, и в этом смысле выступает как защитное приспособление организма.
Эффекторные реакции, опосредованные ТН2-клетками
^2-клетки участвуют в эффекторных реакциях, направленных на защиту от многоклеточных паразитов. Эти реакции изучены пока крайне мало. При этом, подобно TM-клеткам, ^2-лимфоциты вовлекают в защитную реакцию клетки миелоидного ряда. В отличие от реакций, опосредованных TW-клетками, эти клетки представлены не макрофагами, а эозинофилами и тучными клетками.
Роль ^2-клеток в этих процессах в значительной степени состоит в секреции цитокинов: IL-4, IL-5, IL-13, IL-9, IL-3 и GM-CSF. Каждый из них в той или иной степени участвует во взаимодействии с исполнительными клетками. Основную роль при этом играет IL-5. Этот цитокин служит фактором выживания эозинофилов, поддерживает их развитие и привлекает эти клетки в очаг поражения. Эозинофилы инфильтрируют ткань вокруг паразита и выделяют продукты своих гранул, из которых главный белок эозинофилов (MBP), пероксидаза эозинофилов (EPO) и катионный белок эозинофилов (ECP) обладают цитопатогенной активностью в отношении клеток гельминтов и других макропаразитов.
Вспомогательную роль в подобных реакциях играют антитела класса IgE. Полагают, что этот минорный класс иммуноглобулинов, известный как ключевой фактор аллергии немедленного типа, предназначен для осуществления антипаразитарной защиты. Помимо прямого блокирующего действия на паразитов, IgE способен «армировать» макрофаги, связываясь с высокоаффинными FceRI-рецепторами на их поверхности, что придает прицельность действию макрофагов и служит дополнительным фактором их активации.
Источник