Инфекционное воспаление кишечника симптомы

Инфекционный колит – это полиэтиологическая группа воспалительных заболеваний толстого кишечника, которые возникают вследствие активизации условно-патогенной кишечной флоры или попадания патогенных микроорганизмов из внешней среды. Проявляются поносом со слизью, иногда с кровью и неприятным запахом, болями в животе, симптомами общей интоксикации и обезвоживания. Диагностируются на основании клинических данных, посевов кала, общего анализа крови. При необходимости проводят ректороманоскопию и колоноскопию. Лечение инфекционного колита консервативное, включает антибиотикотерапию, противопаразитарные препараты, дезинтоксикацию, борьбу с обезвоживанием).
Общие сведения
Инфекционный колит – это острое (реже – хроническое) заболевание толстого кишечника, которое вызывается разными видами бактерий, простейшими, иногда паразитами и некоторыми вирусами, сопровождается общей интоксикацией, обезвоживанием; в процесс часто вовлекаются другие отделы желудочно-кишечного тракта. Распространено повсеместно: считается, что не существует людей, которые хотя бы раз в жизни не сталкивались с проявлениями острого инфекционного колита. Проблема становится более актуальной в теплый период года.
Заболевание больше распространено в странах с жарким климатом, на тех территориях, где затруднен доступ к питьевой воде, не развиты коммуникации. Наиболее опасные регионы – страны Африки, Юго-Восточной и Средней Азии. Мужчины и женщины болеют одинаково, несколько чаще инфекционный колит диагностируют у детей раннего возраста. Лечением занимаются врачи-инфекционисты. Пациенты могут попадать в отделение проктологии, если заболевание ошибочно принимают за неспецифический инфекционный колит или другие болезни толстого кишечника.
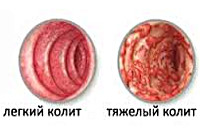
Инфекционный колит
Причины
Основной причиной возникновения инфекционного колита являются разного рода бактерии. Чаще всего заболевание вызывают шигеллы (возбудители дизентерии), кишечная палочка, сальмонеллы, клостридии, иерсинии, брюшнотифозная палочка, кампилобактерии, протей, стафилококки. Симптомы инфекционного колита наблюдаются при аденовирусной, энтеровирусной инфекции, иногда при заболеваниях, вызванных ротавирусом. Также причиной возникновения колита могут стать амебы, лямблии, некоторые другие виды паразитов.
Инфекционный колит иногда развивается как осложнение туберкулеза или сифилиса. У ослабленных пациентов с угнетенным иммунитетом заболевание могут вызывать грибки (кандида, актиномицеты). Грибковый инфекционный колит является одним из маркеров СПИДа, также он возникает у онкологических больных, принимающих химиотерапию, или у лиц, которые длительное время лечатся стероидными гормонами. При дисбактериозе, спровоцированном антибиотикотерапией или химиопрепаратами, инфекционный колит могут вызвать условно патогенные бактерии, например, клостридии.
Патогенез
При инфекционном колите в толстом кишечнике возникают воспалительные изменения, нарушается моторика, усиливается выделение жидкости эндотелиальными клетками и нарушается обратное всасывание воды, повышается проницательность стенок кишечника для различных токсинов, которые вызывают общую интоксикацию организма.
Классификация
С учетом морфологических изменений различают следующие формы инфекционного колита: катаральную, фиброзную, катарально-геморрагическую, флегмонозную, флегмонозно-гангренозную и некротическую. Процесс может довольно быстро прогрессировать и переходить из одной формы в другую, а может приостановиться на одном этапе развития. Кроме того, форма зависит от вида возбудителя. Катаральные формы характерны для вирусных заболеваний, катарально-геморрагическая типична для дизентерии. Клостридии часто вызывают некротический и флегмонозно-гангренозный инфекционный колит.
Симптомы инфекционного колита
Клинические проявления заболевания во многом зависят от его причины. Общими для всех форм являются острое или подострое начало, понос с выделением большого количества слизи, боли в животе, часто спазматического характера, повышение температуры тела, ухудшение общего самочувствия, слабость, сухость слизистых, обложенный белым налетом язык. Если в процесс вовлекается тонкий кишечник (развивается энтероколит), количество каловых масс увеличивается, усиливаются процессы потери жидкости и усугубляются симптомы обезвоживания. В случае поражения и желудка (гастроэнтероколит) заболевание может начинаться с рвоты.
При дизентерии чаще поражается сигмовидная кишка. Заболевание проявляется поносом с небольшим количеством каловых масс, дефекацией 3-20 раз в сутки и больше. В кале выявляют слизь и кровь, в тяжелых случаях при дефекации выделяются только небольшие слизистые сгустки с прожилками крови (ректальный плевок). Пациенты жалуются на резкие боли в животе, у них повышается температура тела до высоких цифр, выражены явления общей интоксикации, иногда до спутанности или потери сознания.
Похожую клинику имеет амебиаз. Этот вид инфекционного колита развивается менее остро, в процесс вовлечена слепая, восходящая ободочная кишка или весь толстый кишечник. Кал с большим количеством слизи, перемешанной с кровью, напоминает малиновое желе. Симптомы интоксикации не очень выражены, заболевание может приобретать хронический или рецидивирующий характер.
Инфекционный колит, вызванный сальмонеллами, проявляется поносом цвета болотной тины с неприятным запахом. Каловые массы жидкие, так как поражен и тонкий кишечник. У пациентов поднимается температура, тяжелый инфекционный колит может осложняться сепсисом и септицемией.
Псевдомембранозный колит, обусловленный клостридиями, возникает на фоне антибиотикотерапии, химиотерапии или при тяжелом дисбиозе. Проявляется лихорадкой, схваткообразными болями в животе, обильным поносом с гнилостным запахом. Псевдомембранозный инфекционный колит часто рецидивирует, может осложняться некрозом кишечника.
Диагностика
Главное значение в диагностике инфекционного колита имеют лабораторные анализы. Для выяснения этиологии заболевания проводят вирусологические, паразитологические бактериологические исследования кала. Реже исследуют сыворотку крови для выявления антител к тому или иному возбудителю. Посев крови на стерильность могут проводить при подозрении на септические осложнения. В общем анализе крови при бактериальном инфекционном колите можно выявить лейкоцитоз со сдвигом формулы влево, повышение СОЭ. При вирусном колите повышается уровень лимфоцитов, а при паразитарном – преимущественно эозинофилов.
Эндоскопические исследования имеют вспомогательный характер, так как картина морфологических изменений не является специфической, и данный вид диагностики проводится с целью дифференцирования от других заболеваний толстого кишечника. Ректороманоскопию проктологи или инфекционисты выполняют при бактериальной дизентерии, псевдомембранозном инфекционном колите. УЗИ органов брюшной полости показано при подозрении на осложнения. Дифференцируют инфекционный колит с болезнью Крона, дивертикулитом, дивертикулярной болезнью, дисбиозом. Также очень важно различать между собой разные виды инфекционного колита, так как от причины зависит специфическая терапия.
Лечение инфекционного колита
Для специфического лечения в первую очередь используют антибиотики, желательно перорального применения. Для дизентерии препаратами выбора являются фторхинолоны или 8-оксихинолоны. Сальмонеллез или инфекционный колит, вызванные кишечной палочкой, требуют применения цефалоспоринов III и IV поколений, действующих на грамотрицательную флору. Псевдомембранозный колит лучше всего поддается лечению метронидазолом. При амебиазе используют амебоциды прямого и непрямого действия ( хиниофон, хлорохин), антибиотики тетрациклинового ряда, метронидазол. При грибковом инфекционном колите назначают противогрибковые препараты.
Важным направлением лечения инфекционного колита является регидратация. При незначительной и средней степени потери жидкости, отсутствии рвоты применяют пероральные солевые растворы. Если состояние больного тяжелое, проводят инфузионную регидратацию и дезинтоксикационную терапию. При инфекционном колите рекомендуют принимать пробиотики и ферментные препараты (панкреатин).
Прогноз и профилактика
Прогноз при инфекционном колите довольно благоприятный, так как на сегодняшний день известны эффективные методы этиотропной терапии данного заболевания. Ухудшается прогноз при тяжелых формах инфекционного колита, вызванного клостридиями, сальмонеллами, грибками, а также у ослабленных пациентов с онкопатологией, у больных СПИДом. Более тяжело инфекционный колит переносят дети. Из профилактических мероприятий главным является гигиена. Следует тщательно контролировать чистоту и срок годности пищевых продуктов, особенно тех, которые употребляются без термической обработки, а также качество употребляемой воды.
Источник
Лечение воспалительных заболеваний кишечника
Несколько классов медицинских препаратов эффективны при лечении воспалительных заболеваний кишечника. Детали их выбора и использования обсуждаются в отношении каждого заболевания.
5-аминосалициловая кислота
(5-АСК, месаламин). 5-АСК блокирует продукцию простагландинов и лейкотриенов и оказывает другие благоприятные эффекты на воспалительный каскад. Поскольку 5-АСК активна только внутри просвета кишечника и быстро абсорбируется в проксимальных отделах тонкой кишки, это должно быть учтено для создания условий замедленной абсорбции при пероральном приеме. Сульфасалазин, оригинальный препарат в этом классе, задерживает абсорбцию комплекса 5-АСК с сульфагруппой сульфапиридина. Комплекс расщепляется бактериальной флорой в терминальных отделах подвздошной и толстой кишки, освобождая 5-АСК. Сульфагруппа, однако, вызывает многочисленные нежелательные эффекты (напр., тошноту, диспепсию, головную боль), нарушает абсорбцию фолиевой кислоты и, иногда, вызывает тяжелые неблагоприятные реакции (напр., гемолитическую анемию и агранулоцитоз и, редко, гепатит или пневмонит).
Обратимое снижение в сперме количества сперматозоидов и их подвижности наблюдается у 80 % мужчин. При использовании сульфасалазина его необходимо принимать с пищей, первоначально в низкой дозировке (напр., 0,5 г перорально 2 раза в день) и постепенно увеличивать дозу в течение нескольких дней до 1-2 г 2-3 раза в день. Пациенты должны дополнительно ежедневно принимать перорально 1 мг фолата и контролировать общий анализ крови и печеночные тесты каждые 6-12 месяцев.
Более современные препараты, состоящие из комплекса 5-АСК с другими транспортными средствами, также эффективны, но обладают меньшими неблагоприятными эффектами. Олсалазин (димер 5-АСК) и балсалазин (5-АСК, конъюгированная с неактивным компонентом) расщепляются бактериальной азоредуктазой (как и сульфасалазин). Эти препараты активируются главным образом в толстой кишке и менее эффективны при поражениях проксимальных отделов тонкой кишки. Дозировка олсалазина составляет 500-1500 мг 2 раза в день и балсалазина – 2,25 г 3 раза в день. Олсалазин иногда вызывает диарею, особенно у пациентов с панколитом. Эта проблема минимизируется постепенным увеличением дозы и приемом препарата с пищей.
Другие формы 5-АСК предусматривают покрытия для задержки выхода препарата. Асакол (обычная доза 800-1200 мг 3 раза в день) представляет собой 5-АСК, покрытую акриловым полимером, рН растворимость которого задерживает выход препарата до дистального отдела подвздошной и толстой кишки. Пентаза (1 г 4 раза в день) представляет собой 5-АСК, заключенную в капсулу из микрогранул этилцеллюлозы, и в тонкой кишке освобождается только 35% препарата. Вторичный острый интерстициальный нефрит из-за применения месаламина развивается редко; желателен периодический контроль функции почек, так как в большинстве случаев нарушения обратимы при своевременном выявлении осложнения.
При проктитах и поражении левой половины толстой кишки возможно применение 5-АСК в форме суппозиториев (500 мг 2-3 раза в день) или в виде клизм (4 г перед сном или 2 раза в день). Ректальное применение препарата эффективно при остром течении заболевания и длительном использовании и может быть целесообразным в комбинации с пероральным приемом 5-АСК.
[27], [28], [29], [30], [31], [32], [33], [34], [35], [36], [37], [38], [39], [40]
Глюкокортикоиды
Глюкокортикоиды показаны в острых случаях большинства форм воспалительных заболеваний кишечника, если препаратов 5-АСК недостаточно, но они не предназначены для поддерживающего лечения. В тяжелых случаях используется внутривенно гидрокортизон 300 мг/день или метилпреднизолон 60-80 мг/день непрерывно капельно или разделенными дозами; при средней степени тяжести можно применять перорально преднизолон или преднизолон 40-60 мг 1 раз в день. Лечение воспалительных заболеваний кишечника продолжается до исчезновения симптомов (обычно 7-28 дней) и доза снижается постепенно с 5 до 10 мг еженедельно до 20 мг 1 раз в день с последующим снижением с 2,5 до 5 мг еженедельно с назначением поддерживающей терапии 5-АСК или иммуномодуляторами. Неблагоприятные эффекты кратковременной терапии глюкокортикоидами в высоких дозах включают гипергликемию, гипертонию, бессонницу, повышенную активность и острые эпизоды психотических расстройств.
Клизмы с гидрокортизоном или орошения могут использоваться при проктитах и поражении левого фланга толстой кишки; в виде клизмы вводится 100 мг препарата в 60 мл изотонического раствора 1-2 раза в день. Этот состав следует задержать в кишке как можно дольше; инстилляции перед сном при положении пациента на левом боку с приведенными к животу бедрами позволяют пролонгировать время задержки раствора и увеличить зону воздействия. В случае эффективности ежедневное лечение должно быть продлено приблизительно на 2-4 недели, затем через день в течение 1-2 недель с последующей постепенной отменой в течение более чем 1-2 недель.
Будезонид – глюкокортикоид с высоким (> 90%) метаболизмом в печени в течение первого цикла; таким образом, пероральное применение может иметь существенный эффект на заболевание ЖКТ, но минимальный супрессивный эффект на надпочечники. Пероральное применение будезонида имеет меньше неблагоприятных эффектов, чем преднизолон, но он не столь эффективен и обычно используется в менее тяжелых случаях заболевания. Его дозировка – 9 мг 1 раз в день. Его применение также доступно за пределами США, как и клизма. Как и другие глюкокортикоиды, будезонид не рекомендован при длительном применении.
Иммуномодулирующие препараты
Азатиоприн и его метаболит 6-меркаптопурин ингибируют функцию Т-клеток. Они эффективны при длительном применении и могут уменьшать потребность в глюкокортикоидах и поддерживать ремиссию в течение многих лет. Для достижения клинического эффекта часто необходимо применение этих препаратов в течение 1-3 месяцев, поэтому глюкокортикоиды не могут быть исключены из лечения, по крайней мере, 2 месяца. Обычная дозировка азатиоприна 2,5-3,0 мг/кг перорально 1 раз в день и 6-меркаптопурина 1,5-2,5 мг/кг перорально 1 раз в день, но дозировка индивидуально может варьировать в зависмости от метаболизма. Признаки супрессии костного мозга должны регулярно контролироваться подсчетом лейкоцитов (каждые две недели в 1-м месяце, затем каждые 1-2 месяца). Панкреатит или высокая лихорадка наблюдаются приблизительно у 3-5% пациентов; любое из них является абсолютным противопоказанием к повторному применению. Гепатотоксичность развивается более редко и может контролироваться биохимическими анализами крови каждые 6-12 месяцев.
У ряда пациентов, нечувствительных к глюкокортикоидам, может быть успешным применение метотрексата перорально, внутримышечно или подкожно в дозе 15-25 мг, и даже у тех пациентов, которые были нечувствительны к азатиоприну или 6-меркаптопурину. Характерны тошнота, рвота и бессимптомные изменения функциональных печеночных тестов. Пероральное применение фолата 1 мг 1 раз в день может уменьшить некоторые из неблагоприятных эффектов. Употребление алкоголя, тучность и диабет являются факторами риска развития гепатотоксичности. Пациентам с этими факторами риска необходимо выполнить биопсию печени после полной дозы 1,5 г.
Циклоспорин, который блокирует активацию лимфоцитов, может быть эффективным у пациентов с тяжелым течением язвенного колита, нечувствительного к глюкокортикоидам и требующего колэктомии. Его применение абсолютно показано у пациентов с болезнью Крона и неподдающимися лечению свищами или пиодермией.
Начальная доза – 4 мг/кг внутривенно 1 раз в день; при эффективности пациентов переводят на пероральный прием 6-8 мг/кг 1 раз в день и затем быстро переводят на азатиоприн или 6-меркаптопурин. Многочисленные неблагоприятные эффекты (напр., почечная токсичность, приступы эпилепсии, оппортунистические инфекции) являются противопоказанием к длительному применению препарата (> 6 месяцев). В целом пациентам не предлагают лечение циклоспорином, если нет причины избежать более безопасного метода лечения, чем колэктомия. При применении препарата его уровни в крови должны сохраняться между 200-400 нг/мл и при этом рассматриваться как профилактика Pneumocystis jiroveci (ранее именовалась P. carinii). Такролимус – иммунодепрессант, используемый в трансплантологии, так же эффективен, как и циклоспорин.
Антицитокиновые препараты
Инфликсимаб, CDP571, CDP870 и адалимумаб являются антителами против TNF. Натализумаб является антителом против молекулы адгезии лейкоцита. Эти вещества могут быть эффективными при болезни Крона, но их эффективность при ЯК неизвестна.
Инфликсимаб применяется в режиме отдельной внутривенной инфузии в дозе 5 мг/кг в течение 2 часов. Некоторые клиницисты начинают лечение с параллельного назначения 6-меркаптопурина, используя инфликсимаб в качестве поддерживающего препарата, пока эффективность основного медикамента не достигнет наибольшей активности. Плавное снижение дозы глюкокортикоида можно начать через 2 недели. При необходимости повторные введения инфликсимаба можно повторять каждые 8 недель. Неблагоприятные эффекты включают отсроченные реакции гиперчувствительности, головную боль и тошноту. Несколько пациентов погибли от сепсиса после использования инфликсимаба, поэтому генерализованная бактериальная инфекция является противопоказанием к применению препарата. Кроме того, на фоне применения этого препарата зарегистрирована реактивация туберкулеза; поэтому перед назначением препарата необходимо выполнение туберкулиновой пробы с PPD и рентгенографии органов грудной клетки.
Талидомид снижает продукцию aTNF и интерлейкина 12 и в некоторой степени подавляет ангиогенез. Препарат может быть эффективным при болезни Крона, но тератогенность и другие неблагоприятные эффекты (напр., сыпь, гипертония, нейротоксичность) ограничивают его применение пока только научными исследованиями. Изучается эффективность других антицитокинов.антиинтегриновых антител и факторов роста.
[41], [42], [43], [44], [45], [46], [47], [48], [49], [50], [51]
Антибиотики и пробиотики
Антибиотики эффективны при болезни Крона, но их применение ограничено при язвенном колите. Метронидазол в дозе 500-750 мг перорально 3 раза в день в течение 4-8 недель купирует проявления заболевания при средней степени тяжести и достаточно эффективен при развитии свищей. Однако неблагоприятные эффекты (особенно нейротоксичность) могут препятствовать полному курсу лечения. Ципрофлоксацин в дозе 500-750 мг перорально 2 раза в день оказывается менее токсичным. Некоторые эксперты рекомендуют комбинированное применение метронидазола и ципрофлоксацина.
Различные непатогенные микроорганизмы (напр., комменсал Escherichia coli, Lactobacillus species, Saccharomyces) каждодневно используются как пробиотики и могут быть эффективными в профилактике синдрома воспаления илео-анального резервуара (pouchitis syndrom), но все же должна быть ясно определена и другая их роль в лечении.
[52], [53], [54], [55], [56], [57], [58], [59], [60], [61], [62], [63], [64], [65], [66]
Заместительная терапия
Большинство пациентов и их семьи волнует режим питания и влияние стресса. Хотя имеются единичные сообщения о клиническом эффекте определенных диет, включая одну с жестким ограничением углеводов, контрольные исследования не доказали какой-либо эффективности. Исключение стрессовых перегрузок может быть эффективным.
Источник
