Изменение лейкоцитов при воспалении
Повышение белых кровяных телец в крови (лейкоцитов) называется лейкоцитозом. Лейкоциты – это важная составляющая иммунной системы человека, так как они защищают организм от различных «врагов» и не допускают, что бы некоторые вредные клетки размножались.
Почему же порой анализ обнаруживает повышенные лейкоциты в крови? Что это значит, и каковы причины данного состояния? Попробуем разобраться.
Для чего нужны лейкоциты?
Основные задачи белых кровяных телец можно представить следующим образом:
- Выходят в желудочно-кишечный тракт, захватывают питательные вещества и переносят их в кровь, что в особенности важно для новорожденных, которые, находясь на грудном вскармливании, вместе с молоком получают готовые неизмененные иммуноглобулины матери, способные защитить от многих инфекций маленького человека.
- Лейкоциты принимают участие в формировании клеточного и гуморального иммунитета, что составляет их защитную функцию.
- Уничтожают различные закладки, которые и не нужны вовсе, еще в эмбриональном периоде – морфогенетическая функция.
- Растворяют поврежденные ткани и осуществляют гистолитическую задачу.
Развернутый анализ крови предусматривает подсчет не только общего количества лейкоцитов, но и процентное содержание в мазке всех видов белых кровяных телец.
Норма лейкоцитов в крови
Анализ крови на лейкоциты проводят для диагностики всевозможных состояний организма. Норма лейкоцитов у взрослого человека составляет – 4-8,8 х 109 /л.
В крови у ребенка лейкоциты всегда значительно повышены. В норме лейкоциты в крови у новорожденных содержатся в количестве – 9,2-13,8 х 109 /л. Лейкоциты у детей, норма с года до трех лет – 6-17 х 109 /л. Лейкоциты в крови у ребенка до десяти лет в норме – 6,1-11,4 х 109 /л.
При беременности, как правило, уровень лейкоцитов в крови повышенный, ближе к родам такой уровень вообще считается нормой – чем больше нагрузки, тем он выше.
Когда повышение лейкоцитов можно считать нормой
В течение дня количество лейкоцитов в крови изменяется. В некоторых случаях оно может даже превышать норму, но беспокоиться по этому поводу нет смысла.
Такой лейкоцитоз называется физиологическим и его причинами могут стать:
- Курение.
- Стрессы, серьезные эмоциональные переживания.
- Рацион питания. Некоторые продукты могут влиять на лейкоциты.
- Во второй половине беременность повышение лейкоцитов в крови тоже является нормой.
- Спорт и физические нагрузки всегда приводят к колебанию уровня лейкоцитов в крови.
- Пребывание в условиях горячего воздуха. Это может быть чрезмерное увлечение солнечными ваннами или рабочая обстановка, например, в определенных производственных цехах. Сюда же можно отнести посещение бани и сауны.
Чтобы исключить влияние всех этих факторов, анализ крови сдают в спокойном состоянии утром и натощак. И если ваш анализ показывает высокое значение, то речь уже идет о патологическом лейкоцитозе, то есть связанном с течением какого-то заболевания.
Повышенные лейкоциты в крови: причины
Почему у взрослого человека лейкоциты в крови повышены, и что это значит? Патологический лейкоцитоз указывает на наличие проблем со здоровьем. Так, повышенные лейкоциты в крови появляются в следствие:
- Любых инфекционных заболеваний: бронхит, пневмония, ОРВИ и т.д.
- Аутоиммунные заболевания, типичным проявлением которых является распознавание иммунной системой собственных тканей, как чужеродных, и формирование ответа организма.
- Хронические воспалительные заболевания, локализованные в любом органе, тоже дают лейкоцитоз, правда, не такой выраженный, так как организм как бы привыкает и борется не так активно.
- Острые бактериальные инфекции: холецистит, аппендицит, пиелонефрит. Как правило, в этом случае повышение происходит за счет увеличения нейтрофилов.
- Аллергия – неадекватная реакция иммунной системы, сопровождающаяся синтезом повышенного количества лейкоцитов и иммуноглобулинов.
- При поражении вирусами (краснуха, гепатит, инфекционный мононуклеоз, ВИЧ).
- Повышенный уровень лейкоцитов может наблюдаться при сильных болевых и эмоциональных воздействиях, потому что белые клетки крови не останутся безучастными к боли, тяжелой физической и психоэмоциональной нагрузке.
- Гнойные инфекции (перитонит, абсцессы) или сепсис могут стать причиной очень высокого уровня лейкоцитов (до 50х109/л).
- Онкологические процессы в различных органах и тканях также нередко сопровождаются значительным увеличением количества лейкоцитов в крови.
- Обширные ожоги и обморожения, при которых кожа не способна сохранять барьерную функцию.
- При различных видах паразитоза в крови наблюдается увеличение эозинофилов (один из видов лейкоцитов).
Степень повышения лейкоцитов отражает тяжесть заболевания и зависит от возраста. Правило лечения лейкоцитоза одно – установить причину увеличения количества лейкоцитов в крови и устранить ее.
Какие симптомы?
Данное состояние часто сопровождается следующими признаками:
- недомогание, усталость;
- умеренная и высокая гипертермия;
- снижение зрения, нарушение сна;
- потеря веса и боли в суставах и мышцах;
- излишнее потоотделение, головокружение, потеря аппетита.
Иногда лейкоцитоз можно выявить лишь при очередном общем анализе крови. Существует ряд малоизученных состояний человека, при которых может повышаться СОЭ, лейкоциты, температура. Как правило, проходит время, и все показатели приходят в норму. Каких-либо проявлений эти отклонения от нормы не имеют.
Как понизить уровень лейкоцитов в крови
Порядок лечения лейкоцитоза устанавливает врач после дополнительных обследований. Терапия, прежде всего, направляется на устранение факторов, спровоцировавших повышение уровня лейкоцитов. Отдельного лечения для снижения уровня лейкоцитов в крови не предусматривается.
Если повышенное количество лейкоцитов в крови вызвано физиологическими причинами (неправильным питанием, беременностью, перенапряжением), то для того, чтобы его снизить, необходимо изменить свой образ жизни:
- правильно питаться.
- больше отдыхать.
- избегать переохлаждения или перегрева на фоне пониженного иммунитета.
При выявлении лейкоцитоза ни в коем случае нельзя заниматься самолечением. Данное нарушение может иметь временный характер или свидетельствовать о тяжелых заболеваниях, которые требуют медицинского вмешательства, и только специалист способен выяснить, почему количество лейкоцитов растет и как с этим бороться.
Источник
Важная функция воспалительной реакции заключается в накоплении в очаге повреждения лейкоцитов и их активации для элиминации повреждающих агентов. Лейкоциты при типичных воспалительных реакциях отвечают за фагоцитоз и представлены ней-трофилами и макрофагами, которые поглощают бактерии и другие микробы и элиминируют некротическую ткань и инородные субстанции. Цена этого защитного потенциала лейкоцитов высока.
При излишней активации лейкоциты, разрушающие бактерии и некротические ткани, могут повредить и нормальную ткань, вызвать ее вторичное повреждение и продлить воспаление.
Участие лейкоцитов в воспалительном процессе осуществляется в следующей последовательности:
(1) выход из кровотока через стенку сосуда в окружающую ткань;
(2) распознавание микробов и некротической ткани;
(3) фагоцитоз и удаление повреждающего агента.
Мобилизация лейкоцитов из просвета сосуда через его стенку в интерстициальную ткань (экстравазация) может быть разделена на несколько последовательных этапов:
– маргинация, роллинг и адгезия лейкоцитов к эндотелию в просвете сосуда. В норме сосудистый эндотелий в неактивном состоянии не адгезирует клетки из кровотока и не препятствует их проходу. При воспалении лейкоциты приклеиваются к эндотелию перед выходом из просвета сосуда через стенку;
– миграция лейкоцитов через слой эндотелия и стенку сосуда;
– миграция лейкоцитов в ткани под действием хемотаксической активации.
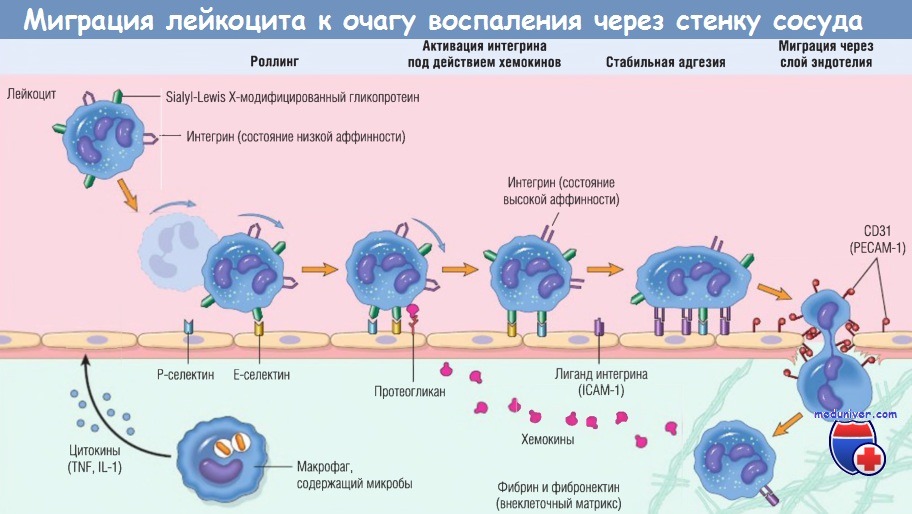
Многоступенчатый процесс миграции лейкоцита через стенку сосуда на примере нейтрофила.
Сначала лейкоцит перекатывается по поверхности эндотелия, потом становится активированным и адгезируется к эндотелию, затем проходит сквозь него,
проникает через базальную мембрану и мигрирует в участок повреждения ткани под действием хемоаттрактантов.
На разных этапах этого процесса работают разные основные молекулы:
селектины — при роллинге, хемокины (обычно представленные в связанном виде с протеогликанами) — при активации нейтрофилов для повышения сродства интегринов,
интегрины — для стойкой адгезии, CD31 (РЕСАМ-1) — для трансмиграции. Нейтрофилы экспрессируют низкие уровни L-селектина;
они связываются с эндотелием преимущественно через Р- и Е-селектины.
ICAM-1 — молекула межклеточной адгезии 1; IL — интерлейкин; РЕСАМ-1 — тромбоцитарная молекула адгезии эндотелиальных клеток 1; TNF — фактор некроза опухоли.
а) Маргинация, роллинг и адгезия лейкоцитов к эндотелию в просвете сосуда. При нормальном венозном кровотоке эритроциты движутся в центре потока крови, оттесняя лейкоциты к стенке сосуда. Поскольку уже на ранних стадиях воспаления кровоток замедляется (стаз) и меняются гемодинамические условия (падает напряжение сосудистой стенки), то все большее количество лейкоцитов занимает периферическую позицию в кровотоке вдоль поверхности эндотелия.
Этот процесс перераспределения лейкоцитов называют маргинацией. Далее отдельные лейкоциты или их скопления ненадолго прилипают к эндотелию, отделяются и опять прилипают, как бы перекатываясь по стенке сосуда. Такое перемещение лейкоцитов вдоль сосудистой стенки называют роллингом. В некоторой точке клетка останавливается и в этот момент плотно прилипает к эндотелию (происходит адгезия).
Адгезия лейкоцитов к эндотелиальным клеткам опосредована молекулами адгезии, экспрессию которых на обоих типах клеток усиливают секретирован-ные белки — цитокины. Цитокины секретиру-ются клетками тканей в ответ на появление микробов или других повреждающих агентов, тем самым обеспечивая миграцию лейкоцитов в места присутствия этих агентов.
Начальные роллинговые взаимодействия опосредованы семейством белков селектинов. Существует три типа селектинов: один экспрессируется на лейкоцитах (L-селектин), другой — на эндотелии (Е-селектин), а третий — на тромбоцитах и эндотелии (Р-селектин). Лиганды к селектинам — это сиалированные олигосахариды, связанные с муциноподобными гликопротеиновыми структурами. Экспрессия селектинов и их лигандов регулируется цито-кинами, продуцируемыми в ответ на инфекционное повреждение.
Тканевые макрофаги, тучные клетки и эндотелиальные клетки первыми взаимодействуют с микробами и некротической тканью и реагируют, секретируя несколько цитокинов, в т.ч. TNF, интерлейкин-1 (IL-1) и хемокины (хемотак-сические цитокины, хемоаттрактанты). TNF и IL-1, выявляемые на эндотелиальных клетках посткапиллярных венул, соседствующих с инфекцией, индуцируют скоординированную экспрессию множества молекул адгезии. В течение 1-2 час эндотелиальные клетки начинают экспрессировать Е-селектин и лиганды к L-селектину.
Другие медиаторы, такие как гистамин, тромбин и фактор активации тромбоцитов, описанные далее, стимулируют перераспределение Р-селектина из его обычного внутриклеточного депо в гранулах эндотелиоцитов (названных тельцами Вейбеля-Паладе) на поверхность клетки. Лейкоциты экспрессируют L-селектин, а также лиганды к Е- и Р-селектинам, все они связываются с молекулами на эндотелиальных клетках. Эти низкоаффинные связи легко разрушаются под действием сил кровотока. В результате связанные лейкоциты прилипают, отделяются, опять прилипают, таким образом перемещаясь по поверхности эндотелия.
Слабые роллинговые связи позволяют лейкоцитам замедлить ход и связаться с эндотелием более прочно. Плотность адгезии опосредована семейством лейкоцитарных поверхностных гетеродимерных белков интегринов. TNF и IL-1 индуцируют экспрессию эндотелиальными клетками лигандов к интегринам, в основном к молекулам адгезии сосудистого эндотелия 1 (VCAM-1) (для интегрина VLA-4) и к молекулам межклеточной адгезии 1 (ICAM-1) (для интегринов LFA-1 и Мас-1). В норме лейкоциты экспрессируют интегрины с низкой аффинностью.
Тем временем хемокины, образованные в месте повреждения, попадают в просвет сосуда, прикрепляются к протеогликанам эндотелиальных клеток и концентрируются на поверхности эндотелия. Эти хемокины связываются и активируют роллинговые лейкоциты. В результате лейкоцитарные интегрины VLA-4 и LFA-1 превращаются в высокоаффинные. Комбинация цитокин-индуцированной экспрессии лигандов интегринов на эндотелии и активация лейкоцитарных интегринов приводит к плотному интегрин-опосредованному сцеплению лейкоцитов с эндотелием в очаге воспаления. Лейкоциты перестают перемещаться, их цитоскелет реорганизуется, и они распределяются по эндотелиальной поверхности.
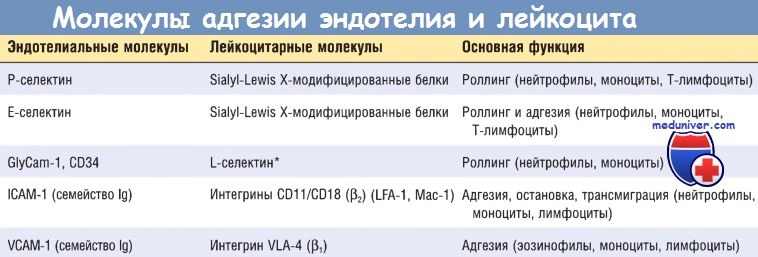
* Нейтрофилы слабо экспрессируют L-селектин, который участвует в адгезии циркулирующих Т-лимфоцитов в венуле с высоким эндотелием лимфатических узлов и лимфоидной ткани слизистых оболочек, а затем в хоуминге лимфоцитов.
ICAM-1 — молекулы межклеточной адгезии 1; lg — иммуноглобулин; VCAM-1 — молекулы адгезии сосудистого эндотелия 1.
б) Миграция лейкоцитов через слой эндотелия и стенку сосуда. Следующий этап в процессе мобилизации лейкоцитов — трансмиграция, или диапедез (миграция лейкоцитов через слой эндотелия). Трансмиграция происходит преимущественно в посткапиллярных венулах. На адгезированные лейкоциты действуют хемокины, стимулируя выход лейкоцитов через межэндотелиальные пространства в соответствии с градиентом концентрации хемокинов и перемещение к месту раны или инфекции, где хемокины были образованы. В процессе миграции лейкоцитов участвуют несколько молекул, располагающихся в межклеточных соединениях между эндотелиальными клетками.
Эти молекулы включают тромбоцитарную молекулу адгезии эндотелиальных клеток 1 (РЕСАМ-1), или CD31, из суперсемейства Ig и несколько молекул адгезии. После прохождения через эндотелий лейкоциты просачиваются через базальную мембрану (возможно, за счет выделения коллагеназ) в окружающую сосуды ткань. Затем клетки мигрируют по градиенту концентрации хемокинов и накапливаются вне сосуда. В соединительной ткани лейкоциты адгезируются к ВКМ за счет способности интегринов и CD44 связываться с белками матрикса. Таким образом лейкоциты попадают в нужное место.
Наиболее яркое доказательство важности лейкоцитарных молекул адгезии — существование генетических дефектов этих молекул, приводящих к интеркур-рентным бактериальным инфекциям, развивающимся вследствие нарушения адгезии лейкоцитов и недостаточной воспалительной реакции. Индивиды с дефицитом адгезии типа I имеют нарушения биосинтеза b2-цепи, общей для интегринов LFA-1 и Мас-1. Дефицит адгезии типа II вызывается отсутствием sialyl-Lewis X (фукозосодержащего лиганда к Е- и Р-селектинам) в результате дефекта фукозилтрансферазы — фермента, присоединяющего части фукозы к белковым каркасам.
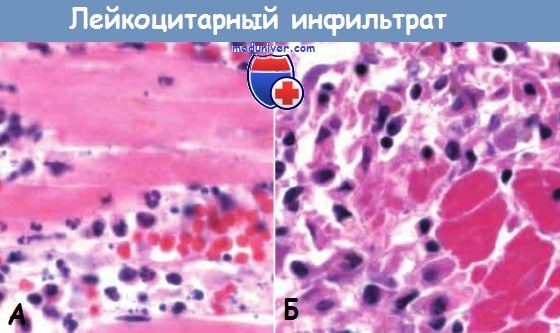
Лейкоцитарный инфильтрат при воспалительных реакциях.
Ранняя (нейтрофильная) (А) и поздняя (мононуклеарная)
(Б) фазы образования инфильтрата в зоне демаркационного воспаления при инфаркте миокарда.
в) Миграция лейкоцитов в ткани под действием хемотаксической активации. После выхода из просвета сосуда лейкоциты направляются в очаг повреждения. Этот процесс называют хемотаксисом. Хемоаттрактантами могут быть и экзогенные, и эндогенные субстанции. Самые распространенные экзогенные агенты — продукты бактерий, в т.ч. пептиды, которые имеют в своем составе концевую аминокислоту N-формилметионин и некоторые липиды. Эндогенные хемоаттрактанты включают следующие химические медиаторы воспаления:
(1) цитокины, особенно семейства хемокинов (например, IL-8);
(2) компоненты системы комплемента, особенно С5а;
(3) метаболиты арахидоновой кислоты, в основном лейкотриен В4.
Все эти хемотаксические агенты связываются со специфическими 7-трансмембранными G-белок-связанными рецепторами на поверхности лейкоцитов. Сигналы, передающиеся через эти рецепторы, активируют вторичные мессенджеры, повышающие уровень кальция в цитозоле и, в свою очередь, активирующие малые гуанозинтрифосфатазы семейства Rac/Rho/cdc42 и множество киназ. Эти сигналы вызывают полимеризацию актина, приводящую к увеличению его количества в передней части клетки и оттеснению миозиновых филаментов назад.
Лейкоцит передвигается, образуя свои филоподии, которые тянут заднюю часть клетки в направлении движения, как автомобиль с передним приводом. В конечном итоге лейкоцит мигрирует к агенту воспаления в соответствии с градиентом концентрации локально продуцируемых хемоаттрактантов.
Природа лейкоцитарного инфильтрата варьирует в зависимости от длительности воспаления и типа его агента. При большинстве форм острого воспаления в воспалительном инфильтрате в первые 6-24 час доминируют нейтрофилы, через 24-48 час они заменяются моноцитами. Есть несколько причин для раннего появления нейтрофилов: они самые многочисленные в крови; быстрее реагируют на хемокины и могут более плотно прикрепляться к адгезивным молекулам, таким как Р- и Е-селектины. Нейтрофилы имеют короткий период жизни: после выхода в ткани подвергаются апоптозу и исчезают в течение 24-48 час. Моноциты могут не только дольше сохраняться в тканях, но и делиться посредством митоза, становясь доминирующей популяцией клеток при хроническом воспалении.
Однако есть исключения. При определенных инфекциях, например синегнойной, клеточный инфильтрат представлен преимущественно нейтрофилами, при вирусных инфекциях первыми клетками, появляющимися в воспалительном инфильтрате, могут быть лимфоциты, а при некоторых реакциях гиперчувствительности основными клетками инфильтрата могут быть эозинофилы.
Понимание молекулярных механизмов мобилизации и миграции лейкоцитов привело к открытию большого количества потенциальных мишеней для лечения и контроля воспаления. Вещества, блокирующие TNF (один из основных цитокинов при мобилизации лейкоцитов), являются наиболее эффективными лекарственными средствами, когда-либо разработанными для лечения хронических воспалительных заболеваний. Антагонисты лейкоцитарных интегринов (например, VLA-4), селектинов и хемокинов одобрены для лечения воспалительных заболеваний или находятся в стадии клинических исследований. Предположительно эти антагонисты смогут не только эффективно контролировать воспаление, но и нарушать у пролеченных больных защитные антимикробные механизмы — физиологическую функцию воспалительного ответа.
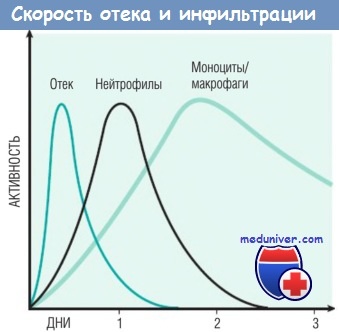
Кинетика отека и клеточной инфильтрации

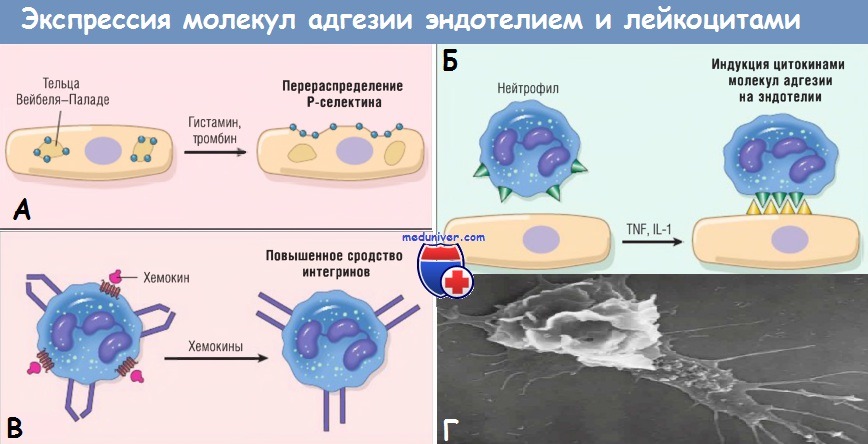
Регуляция экспрессии молекул адгезии эндотелиальными клетками и лейкоцитами.
(А) Перераспределение Р-селектина из внутриклеточных запасов на поверхность клетки.
(Б) Повышенная экспрессия на поверхности клетки селектинов и лигандов к интегринам при цитокиновой активации эндотелия.
(В) Повышение сродства интегринов, индуцированное хемокинами. Кластеризация интегринов участвует в повышении их сродства (не показано).
IL — интерлейкин; TNF — фактор некроза опухоли.
(Г) На электронограмме двигающегося лейкоцита в клеточной культуре видны его филоподии (снизу справа) и тянущийся хвост.
– Рекомендуем ознакомиться со следующей статьей “Рецепторы лейкоцитов для выявления микробов и поврежденных тканей”
Оглавление темы “Патофизиология”:
- Механизмы накопления пигментов в клетке
- Дистрофическая кальцификация аорты как патологическая
- Причины, механизмы метастатической кальцификации тканей и органов
- Механизмы старения клетки и ее этапы
- Определение воспаления и его характеристика
- История изучения воспаления
- Причины острого воспаления
- Изменения сосудов в очаге воспаления: образование транссудата и экссудата
- Реакция лейкоцитов на воспаление – миграция и накопление
- Рецепторы лейкоцитов для выявления микробов и поврежденных тканей
Источник
