Изменения в клетке при воспалении
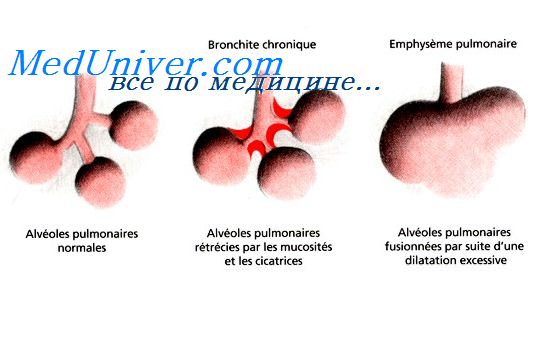
Клеточные механизмы защитных реакций организма при воспалении.Основные закономерности развития необратимых патологических изменений в клетках при первичной и вторичной альтерации Рассматривая воспаление как типовой патологический процесс, протекающий в виде последовательно сменяющих друг друга, а в ряде случаев развивающихся параллельно стадий альтерации, экссудации и пролиферации, необходимо отметить, что при определенных условиях течение воспалительных реакций может иметь как преимущественно защитно-приспособительный, так и разрушительный характер. Воздействие на ткани различных по своей природе факторов (химических, физических, бактериальных), как правило, приводит к развитию первичной альтерации. Степень выраженности и распространенность альтеративных изменений определяется интенсивностью действующего фактора, устойчивостью клеток к этому воздействию и способностью клеточных механизмов компенсировать патологические изменения. Повреждение ткани сопровождается выделением биологически активных веществ, способных еще в большей степени увеличивать альтеративные процессы – вызывать вторичную альтерацию. Независимо от особенностей воздействующего фактора, индуцирующего воспалительный процесс, все изменения в клетках можно свести к следующим типам:
Деструктивные процессы в тканях, возникающие в альтернативной стадии (фазе) воспаления, имеют преимущественно патологический характер. Их выраженностью в значительной степени определяется возможная степень неблагоприятного течения воспалительного процесса в целом. При обратимых сублетальных изменениях клетка способна адаптироваться и восстанавливать свою структуру и функцию. В этом случае, как правило, происходит снижение интенсивности метаболических процессов, ограничение потребления кислорода, угнетение процессов окислительного фосфорилирования, активирование гликолиза, уменьшение запасов макроэргических фосфорных соединений, падение уровня активности K-Na-АТФ-азы, ингибирование внутриклеточных ферментов, активирующих анаболические процессы. В процессе необратимого повреждения клетки наблюдается постепенное увеличение объема внутриклеточных структур (расширение эндоплазматической сети, набухание митохондрий, увеличение объема лизосом). Летальные изменения в клетках сопровождаются повреждением наружной и внутриклеточных мембран, в результате чего повышается их пассивная проницаемость для ионов. Одним из кардинальных признаков повреждения клетки является увеличение содержания натрия в цитозоле и выход во внеклеточную среду калия. Тяжелые метаболические расстройства клеточных функций сопровождаются увеличением содержания кальция в цитозоле. В нормальных условиях в цитоплазме регистрируется низкая концентрация кальция, не превышающая 10″‘ моль/л, которая обеспечивается непрерывной работой Са-АТФаз. Основные запасы кальция содержатся в эндоплазматическом ретикулуме, большая часть мембраны которого плотно покрыта белком с молекулярной массой 110 кДа, являющегося Са-насосом. Концентрация кальция в эндоплазматическом ретикулуме в 10 000-100 000 раз выше чем в цитозоле. Деполяризация клеточной мембраны и гидролиз мембранных липидов сопровождаются раскрытием кальциевых каналов, по которым кальций из внутриклеточных депо (цистерн эндоплазматического ретикулума, митохондрий) или интерстициального пространства устремляется в цитозоль. Возникающие в ходе воспаления метаболические нарушения энергообеспечения работы транспортных систем клеток изменяют нормальное протекание процессов реабсорбции кальция, который устремляется из кальцийсодержащих структур и внеклеточной среды в цитозоль по механизмам пассивного транспорта. – Также рекомендуем “Изменения клеток при альтеративной стадии воспаления.” Оглавление темы “Ключевые механизмы воспаления легких.”: |
Источник
Изменения клеток при альтеративной стадии воспаления.Наибольшее увеличение цитозольной фракции кальция наблюдается в условиях деградации клеточных мембран, нарушений структурной целостности мембран митохондрий, повышения проницаемости лизосомальных мембран с лабилизацией лизосомальных ферментов. Все перечисленные изменения влекут за собой увеличение зоны деструкции в очаге воспаления. Принято считать, что появление в плазмолемме дефектов на протяжении более 3-4 нм, а также снижение цитоплазматического рН на 2 единицы и более свидетельствует о необратимом повреждении клетки (Пермяков Н.К., 1986). В развитии летальных клеточных изменений существенную роль играет активирование свободнорадикального окисления мембранных фосфолипидов. Воздействие патогенных факторов, вызывающих альтерацию, приводит к нарушению оптимального для неповрежденной клетки соотношения функциональной активности прооксидантных и антиоксидантных систем, что сопровождается активированием свободнорадикальных процессов. В ходе альтерации наблюдается ухудшение сопряжения окисления и фосфорилирования, приводящее к нарушениям утилизации кислорода. Это создает дополнительные условия для увеличения интенсивности свободнорадикального окисления мембранных фосфолипидов.
Активирование свободнорадикальных процессов влечет за собой повреждение клеточных мембран, в результате чего нарушаются основные их функции (транспортная, каталитическая и рецепторная). Изменения структуры полиненасыщенных жирных кислот, входящих в состав мембранных фосфолипидов, сопровождаются снижением гидрофобности фосфолипидного бислоя, уменьшением молекулярной подвижности фосфолипидов и нарушениями процессов липид-белковых взаимодействий. Это приводит к увеличению пассивной проницаемости клеточных мембран для ионов, изменениям ионных градиентов, нарушениям процессов биоэлектрогенеза, дисбалансу обмена жидкости между клеткой и внеклеточной средой. Свободнорадикальное окисление фосфолипидов мембран митохондрий сопровождается снижением уровня активности мембраносвязанных ферментов, участвующих в процессах окислительного фосфолирирования, в результате чего снижается его интенсивность. Повреждение в ходе альтеративных процессов клеточных мембран сопровождается нарушением их рецепторных свойств. При этом понижается, вплоть до полного угнетения, способность клетки реагировать на физиологические концентрации биологически активных веществ. Результатом альетеративных изменений в клеточных мембранах является ингибирование процессов, протекающих с участием таких внутриклеточных посредников, как цАМФ и цГМФ, а также триггерных белков. Таким образом, альтеративная стадия воспаления, независимо от вида ткани, в которой оно развивается, имеет преимущественно патологический характер, выраженность которого коррелирует с глубиной и тяжестью деструктивных процессов. В ответ на повреждение в клетке происходят защитно-приспособительные изменения: – Также рекомендуем “Эксудация и эксудативные процессы в ходе воспаления.” Оглавление темы “Ключевые механизмы воспаления легких.”: |
Источник
Воспалительный процесс — это ответная реакция организма на различные виды повреждения. Воспаление очень распространённое патологическое состояние различных органов и систем, в процесс вовлекаются не только кожные покровы, но и различные органы. Следует понимать, что воспаление это всего лишь реакция организма, а не отдельное заболевание.
Этиология воспалительного процесса. К самым основным причинам относятся ранения, ожоги, бактериальные инфекции, химические вещества и излучение.
Аллергические реакции организма тоже могут повлечь за собой воспалительные процессы.
При инфекционном или вирусном заболевании патогенные микроорганизмы активно паразитируют в организме человека, они вырабатывают токсины и тем самым защитные силы организма вырабатывают специфические химические вещества, которые и вызывают воспалительный процесс. Таким образом основная задача воспаления — это выявление и полное уничтожение патогенного микроорганизма.
Механизмы возникновения.
В развитии воспаления огромную роль играют самые мелкие кровеносные сосуды организма капилляры. Таким образом роговица никогда не может вовлечься в патологический процесс так как она абсолютно не имеет кровоснабжения. Капилляры в виде густой кровеносной сети расположены во всех органах. Давление в мелких сосудах относительно не велико и их диаметр практически одинаков с красными кровяными клетками. Белки плазмы через стенки капилляров не могут проникать, хотя некоторые вещества более мелкого размера могут свободно проникать в ткани. При воспалительном процессе диаметр капилляров становится шире, кровоток становится быстрее, таким образом стенки сосуда растягиваются и становятся проницаемыми. Различные белковые молекулы, антитела могут свободно проникать в ткани. Такой процесс взывает на пораженном участке покраснение, припухлость и болезненность тканей. В участке воспаления могут скапливаться фибробласты клетки, которые принимают участие в восстановлении поврежденных клеток. Фибробласты способны полностью восстанавливать функцию поврежденной ткани. Болезненные ощущения при воспалении возникают при высвобождении простагландинов. Они оказывают стимулирующее влияние на нервные окончания болевых рецепторов. Для устранения такого эффекта предпочтительно использовать не стероидных противовоспалительных препаратов в необходимой дозировке.
Функции белых клеток крови в воспалительном процессе очень важны и незаменимы. Такие клетки относятся к системе иммунной защиты, они имеют различную форму. Главная роль в воспалительном процессе принадлежит макрофагу. Макрофаг — это белая клетка крови, относящаяся к иммунной системе, она захватывает чужеродный организм всей поверхностью своего тела и уничтожает его.
Фагоциты защитные клетки организма, которые свободно могут проникать даже через самые узкие щели, их структура имеет геле образную консистенцию, покрытую эластической оболочкой. Фагоцит имеет специфическую ножку, с помощью которой он может свободно передвигаться, также с помощью этой ножки фагоцит захватывает и прикрепляется к микроорганизму затем обволакивает и поглощает. Фагоцит наполнен жидкостным содержимым наполненным ферментами. Ферменты способствуют расщеплению микроорганизма уничтожению и перевариванию. Основные клинические проявления. Основные симптомы: покраснение, гипертермия участка, припухлость и болезненные ощущения. Так же к симптоматике следует отнести тот факт, что при любом воспалительном процессе происходит нарушение функции определенного участка. Лечебные мероприятия направленны на устранение основных причин возникновения процесса. Прогноз на выздоровление благоприятен.
Источник
Оглавление темы “Изменения клеток при воспалении.”:
1. Изменение клеток при воспалении. Изменение морфологии и обмена веществ при воспалении.
2. Метаболизм углеводов при воспалении. Нарушение обмена углеводов при воспалении.
3. Метаболизм липидов при воспалении. Нарушение обмена липидов при воспалении.
4. Метаболизм белков при воспалении. Нарушение обмена белков при воспалении.
5. Метаболизм ионов и воды при воспалении. Нарушение обмена ионов и воды при воспалении.
6. Физико-химические изменения в очаге воспаления. Ацидоз.
7. Гиперосмия в очаге воспаления. Гиперонкия в очаге воспаления.
8. Изменение поверхностного натяжения мембран в очаге воспаления. Изменения коллоидного состояния цитозоля в очаге воспаления.
9. Медиаторы воспаления. Виды медиаторов воспаления.
10. Биогенные амины. Серотонин. Адреналин. Норадреналин.
Причины изменения структуры клеток и других гистологических элементов:
• в течение первых минут — прямое действие флогогенного фактора;
• на более поздних этапах и дополнительно к прямому эффекту флогогенного фактора — влияние вторичных причин: метаболических, физико-химических, микроциркуляторных и регуляторных расстройств.
Основные механизмы морфологических изменений клетки:
• нарушения процессов энергетического обеспечения клеток;
• повреждение мембранного аппарата и ферментных систем;
• дисбаланс ионов и воды;
• нарушения местных (клеточных и органно-тканевых) механизмов регуляции. Проявления
• Развивающиеся в тканях изменения весьма разнообразны: от минимальных структурных отклонений до деструкции и некроза.
• Структурные изменения наблюдаются как в паренхиматозных клетках, так и в строме тканей и органов.
• Существенную роль в потенцировании повреждения клеточных и неклеточных структур играют высвобождающиеся из лизосом и активирующиеся в очаге воспаления гидролазы: протеазы, липазы, фосфолипазы, эластазы, коллагеназы и другие ферменты. Источником их являются как клетки самой повреждённой ткани, так и находящиеся в ней лейкоциты, а при септическом воспалении — и микроорганизмы.
• Для клеток при воспалительной альтерации характерны изменения в цитозоле, а также повреждение плазмолеммы и мембран органелл — митохондрий, лизосом, эндоплазматической сети, комплекса Гольджи и др. В связи с этим меняются их форма, размеры, число, а также функции органелл и клетки в целом.
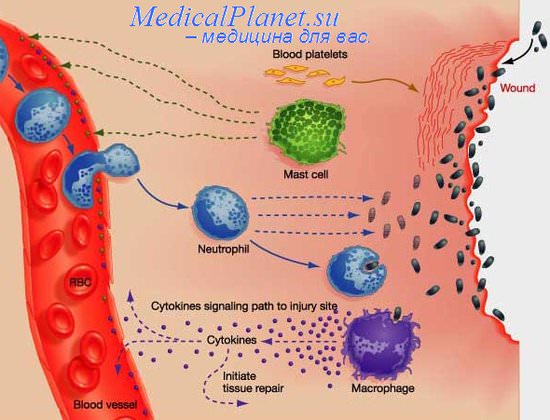
Изменение обмена веществ при воспалении.
В очаге воспаления наблюдаются закономерные фазные изменения метаболизма. Их причины: действие флогогенного фактора и вторичные расстройства в ткани, выражающиеся в перестройке местных механизмов нервной и гуморальной регуляции, микроциркуляции, в формировании физико-химических сдвигов.
На начальном этапе воспаления в ткани (зоны не только первичной, но и вторичной альтерации) преобладают реакции катаболизма, затем — при развитии артериальной гиперемии и активации процессов пролиферации, — как правило, начинают доминировать анаболические реакции.
Конечный «смысл» изменений метаболизма заключается в энергетическом и пластическом обеспечении местных адаптивных реакций в очаге воспаления, направленных на локализацию, уничтожение и элиминацию флогогенного агента, а также на ликвидацию патогенных последствий его воздействия.
– Читать далее “Метаболизм углеводов при воспалении. Нарушение обмена углеводов при воспалении.”
Источник
Изменения обмена веществ
Биологический смысл изменений обмена веществ заключается в энергетическом и пластическом обеспечении процессов, протекающих в очаге воспаления. На начальном этапе воспаления в тканях преобладают реакции катаболизма, а при активации процессов пролиферации начинают доминировать анаболические реакции. Изменения метаболизма в существенной мере регулируются медиаторами воспаления. В очаге воспаления, а нередко и в организме в целом, происходит перестройка всех видов обмена веществ: углеводного, белкового, жирового и водно-солевого, что приводит к физико-химическим изменениям в очаге воспаления.
• Углеводы
♦ Активируются гликогенолиз и гликолиз, обеспечивающие увеличение выработки макроэргических соединений.
♦ Под влиянием разобщителей окисления и фосфорилирования нарушается образование АТФ в цикле Кребса и энергия выделяется в виде тепла.
♦ Гликолиз в условиях гипоксии в очаге воспаления переходит на анаэробный путь, следствием чего является накопление избытка лактата и пирувата, которые формируют метаболический ацидоз.
♦ Возобновление оксигенации тканей, как правило, сопровождается нормализацией энергетического обеспечения клеточных процессов.
• Липиды
♦ Усиливаются липолиз (он сопровождается накоплением свободных ВЖК) и деструкция липидов за счёт интенсификации реакций СПОЛ (с образованием перекисей и гидроперекисей липидов, кетокислот).
♦ В связи с накоплением в клетках свободных ВЖК отмечаются их разобщающий эффект и снижение эффективности тканевого дыхания в митохондриях. ВЖК обладают также детергентным действием (см. раздел «Повреждение мембран», глава 4).
♦ Накопление избытка кетокислот (ацетоуксусной, β-оксимасляной, β-кетоглутаровой и других) вследствие нарушения окисления ВЖК обусловливает ацидоз и вторичную альтерацию в очаге воспаления.
♦ Образующаяся в избытке арахидоновая кислота служит субстратом для образования Пг, тромбоксанов и лейкотриенов.
• Белки
♦ Активируется протеолиз, продукты которого служат субстратом синтеза клеточных компонентов взамен повреждённых.
♦ Развиваются иммунные (в том числе – иммунопатологические) реакции (в связи с денатурацией белков как собственных погибших клеток, так и флогогенного агента). Включение клеточных и гуморальных механизмов иммунитета обеспечивает обнаружение, деструкцию и элиминацию антигенно чужеродных структур.
• Ионы и вода
♦ Расстраивается энергетическое обеспечение селективного переноса катионов и снижается активность катион-зависимых мембранных АТФаз (?+,К+-АТФазы, Са2+Mg2+-АТФазы). Это вызывает нарушение формирования МП и ПД, развитие стойкой деполяризации мембран возбудимых клеток (например, кардиомиоцитов и нейронов).
♦ Нарушается вне- и внутриклеточное соотношение между отдельными ионами. Происходит потеря клеткой К+, Mg2+ и накопление их в межклеточной жидкости. В клетку поступают Na+ и Са2+.
♦ Высвобождается дополнительное количество катионов (К+, Na+, Са2+, железа, цинка) при гидролизе солей и поступлении большого количества Са2+ из повреждённых внутриклеточных депо (митохондрий и цистерн эндоплазматической сети).
♦ Значительно увеличивается осмотическое давление внутри клеток и их органелл, что сопровождается перерастяжением и разрывом их мембран.
Реакция сосудов микроциркуляторного русла при воспалении Изменения регионарного кровотока, стадии и механизмы развития этих изменений в динамике воспалительного процесса.
Источник