Клетки воспаления при астме

Медиаторы бронхиальной астмы. Тучные клетки и ответы типа I при астмеПодробное обсуждение неиммунологических факторов, вызывающих и поддерживающих астму, выходит за рамки наших статей. Однако необходимо остановиться вкратце на фармакологических и неврологических событиях, чтобы не потерять из виду все многочисленные факторы, связанные с индукцией астмы. Значение их особенно велико в настоящее время, когда вся область иммунофармакологии так быстро развивается. Многие исследователи подробно изучали медиаторы, высвобождающиеся из тучных клеток, и было опубликовано несколько интересных обзорных работ на эту тему за последнее время [Orange, 1971; Vane, 1971; Austen, Lichtenstein, 1973; Piper, 1974]. Медиаторы у человека изучались в периферических базофилах, в гомогенатах легочной ткани п в ее разделенных клеточных фракциях, и экспериментально на перфузируемых легких ин-тактных животных. Легочная ткань больных астмой выделяет как гистамин [Schild et al., 1951], так и медленно реагирующую субстанцию анафилаксии (МРС-А) [Brocklehurst, 1960, 1975] при воздействии соответствующих антигенов in vitro. Позднее был открыт фактор хемотаксиса эозинофилов (ФХЭ-А) [Кау, Austen, 1971]. При анафилактическом воздействии на легочную ткань in vitro было обнаружено также несколько типов простагландинов [Piper, Vane, 1969; Riper, Walker, 1973]. Простагландины E1 и Е2 обладают способностью воздействовать на гладкие мышцы, расширяя бронхи. Кроме того, после антигенного воздействия из сенсибилизированных легких человека был выделен фактор, активирующий тромбоциты [Siraganian, Osier, 1971]. При определении количества медиаторов в надосадоч-пой жидкости и в остаточной легочной ткани после антигенного воздействия на сенсибилизированные клетки легких человека или их фрагменты удалось установить, какие медиаторы образуются раньше и какие синтезируются после иммунологической стимуляции.
Гистамин образуется заранее и хранится в гранулах тучных клеток [Ishizaka et al., 1972]. При анафилаксии он высвобождается путем экзоцитоза — на этом биохимическом пути действуют диизопропилфиорофосфат (ДФФ), серинэстераза и ионы кальция [Austen, 1973]. ФХЭ-А также заранее образуется в легких [Wasserman et al., 1973]. Напротив, МРС-А и простагландины не образуются заранее и синтезируются вследствие анафилактической стимуляции. Интересно, что в отличие от образования простагландинов синтез МРС-А может быть заторможен гликатом натрия-хрома [Dawson, Tomlison, 1974]. Особенно важно то, что секреция этих веществ в гомогенатах легочной ткани, видимо, находится под влиянием стимуляции а- и бета-адренергических и холииергических рецепторов [Kaliner et al., 1972; Orange et al., 1971]. Такие адренергические агенты, как изопреналин, увеличивают внутриклеточное содержание циклического аденозин-3,5-монофосфата (циклический АМФ) и подавляют высвобождение гистамина и МРС-А. Такие а-адренергические агенты, как фенилэприн, снижают уровень циклического АМФ и оказывают обратное действие, повышая выделение гистамина и МРС-А [Lichtenstein, Margolis, 1968]. При холинергической стимуляции повышается уровень гуанозина-3,5-монофосфата (циклического ГНФ) и увеличивается высвобождение гистамина и других медиаторов [Orange, 1971]. – Также рекомендуем “Иммунофармакология реакций типа III при астме. Иммунонейрофармакология астмы” Оглавление темы “Виды и формы бронхиальной астмы”: |
Источник
Преимущественно эозинофильные варианты воспаления бронхов при бронхиальной астме.Бронхиальная астма – самое частое заболевание легких, в основе которого лежит эозинофильное воспаление, но принимают участие также другие клетки, причем точное значение каждого типа клеток и медиаторов в его патогенезе неизвестно. При бронхиальной астме отмечается разнообразие воспалительных изменений в бронхах. Принятое в 1993 г. международное соглашение “Global Strategy for Asthma Management” определяет бронхиальную астму как “хроническое воспалительное заболевание дыхательных путей, при котором многие клетки играют определенную роль, включая тучные клетки и эозинофилы”. Только у больны бронхиальной астмой обнаружено интраэпителиальное присутствие эозинофилов и наличие дегранулированных эозинофилов в повышенном количестве под базальной мембраной, вместе с тем найдена корреляция между содержанием дегранулированных эозинофилов, повреждением эпителия бронхов и тяжестью течения бронхиальной астмы. Эозинофилы в содержимом бронхоальвеолярного лаважа сохраняются у больных бронхиальной астмой в межприступный период и выявлена прямая зависимость между уровнем эозинофилов в лаважной жидкости и тяжестью течения бронхиальной астмы. Сохранение воспалительных изменений в бронхах у больных бронхиальной астмой в межприступный период, которое проявляется повышенным содержанием в лаважной жидкости эозинофилов и нейтрофилов, а также перманентным состоянием повышенной реактивности бронхов, способствует тому, что любые внешние и внутренние агенты, играющие роль триггера, могут мобилизировать эти клетки воспаления и вызвать обострение болезни. Повреждение эпителия “большим основным протеином” эозинофилов играет важную роль в развитии неспецифической гиперреактивности бронхов (НГБ) и бронхиальной астмы, которую некоторые авторы даже называют “болезнью эпителия”, поскольку клетки эпителия бронхов выделяют вещества, способные модулировать деятельность гладкой мускулатуры брохов, секретируют производные арахидоновой кислоты, а также содержат чувствительные нервные окончания, раздражение которых ведет через рефлекторные механизмы к выделению нейропептидов, в частности, нейрокинов, вещества П, играющих важную роль в развитии бронхообструкции. “Большой основной протеин” эозинофилов а также эозинофильный катионный белок и эозинофильный нейротоксин вызывают повреждение эпителия, десквамацию и разрушение ресничных клеток, что является типичным при бронхиальной астме. Концентрация эозинофильного катионного белка в мокроте и в периферической крови коррелирует со степенью бронхообструкции . Как правило, имеется прямая зависимость между увеличением количества эозинофилов в содержимом бронхоальвеолярного лаважа и в периферической крови. Количество эозинофилов в периферической крови позволяет судить об общей (системной) аллергизации, и предлагается по степени эозинофилии крови судить о тяжести течения бронхиальной астмы и выраженности обострения болезни. Обнаружено, что НГБ коррелирует с повышением количества эозинофилов в периферической крови даже у лиц без клинических признаков бронхиальной астмы. Иногда бывают отклонения от обычного соответствия количества эозинофилов периферической крови и лаважной жидкости. Это может быть объяснено существованием независимых хемотаксических факторов, действующих в капиллярах большого круга и в альвеолах.
Экспериментальные модели бронхообструктивного синдрома у животных а также ингаляционные провокации различными аллергенами больных бронхиальной астмой показали, что возможно развитие одной или двух фаз патологического процесса: ранняя астматическая реакция, характеризуемая быстрой бронхоконстрикцией с максимумом через 10-30 мин после провокации и постепенным ослаблением в течение последующих 2 часов, и поздняя астматическая реакция, возникающая через 6-8 часов после провокации у 60% больных бронхиальной астмой, с максимумом бронхоконстрикции еще через 2-4 часа. Если основной клеткой, ответственной за развитие ранней астматической реакции, является тучная клетка, то поздняя астматическая реакция связана с привлечением в легкие различных видов клеток, прежде всего эозинофилов, и возникновением хронического воспаления в IgE-опосредованных реакциях. Развитие поздней астматической реакции сопровождается транзиторным снижением количества эозинофилов в периферической крови при повышенном их содержании в бронхиальных смывах, что указывает на избирательное привлечение этих клеток из бронхиальных сосудов и сопровождается повышением НГБ. Впрочем, как сейчас считается, у больных с хроническим персистирующим течением бронхиальной астмы различия между ранней и поздней астматической реакциями не столь явные и тучные клетки и их медиаторы принимают активное участие в развитии хронического воспаления. У больных с поздней астматической реакций не просто изменяется количество эозинофилов, но определяются их качественные изменения: начинают преобладать эозинофилы низкой плотности (плотность меньше 1,095 г/мл), которые более активны, экспрессируют на своей мембране больше рецепторов к IgE и выделяют большее количество БАВ, причем увеличение количества активных эозинофилов коррелирует с тяжестью течения бронхиальной астмы обнаружили в биопсинном материале слизистой бронхов даже у больных с легким течением бронхиальной астмы увеличеннное количество активных эозинофилов, тучных клеток, а также клеток, содержащих фактор некроза опухолей а-цитокина, сходного по своим действиям с интерлеикином-1 и являющимся первичным медиатором воспаления. Некоторые авторы подчеркивают, что эозинофил является мощной эффекторной клеткой, главным образом, в позднюю фазу астматической реакции, проявляющейся аллергическим воспалением преимущественно дистальных отделов бронхов. Возможно, что это особенно справедливо в отношении атонической бронхиальной астмы Привлечение, активация и поддержка длительного существования эозинофилов в слизистом и подслизистом слоях бронхиального дерева вызывается действием многих БАВ, среди которых особенно выделяют интерлейкены 3 и 5, гранулоцитарномакрофагальный колониестимулирующий фактор и фактор некроза опухолей. В настоящее время считается, что одним из ключевых моментов в патогенезе бронхиальной астмы является взаимодействие эозинофила и фактора агрегации тромбоцитов (ФАТ). Дело в том, что эозинофилы – клетки, которые продуцируют ФАТ и в то же время являются объектами его действия: ФАТ вызывает активацию и дегрануляцию эозинофилов и обуславливает их хемотаксис. Показано, что ФАТ вызывает усиление экспрессии Fc-рецепторов для IgC на неактивированных эозинофилах у больных бронхиальной астмой, вовлекая эти клетки в иммунные реакции. ФАТ рассматривается как общая эффекторная субстанция анафилаксии, он также индуцирует агрегацию тромбоцитов с выделением ими серотонина, гистамина, 3 и 4 факторов тромбоцитов, что приводит не только к бронхоспазму, но и нарушениям микроциркуляции. ФАТ может непосредственно повышать проницаемость микрососудов дыхательных путей, что приводит к выходу плазмы, нейтрофилов, моноцитов и эозинофилов. Посредством всех этих механизмов ФАТ вызывает состояние гиперреактивности бронхов по отношению к широкому спектру специфических и неспецифических раздражителей и как модулятор воспалительных реакций вместе с другими воспалительными медиаторами вызывает десенситизацию адренорецепторов у больных БА. Показана роль ФАТ как единственного вещества, вызывающего повышение неспецифической бронхиальной гиперчувствительности и гиперреактивности у здоровых лиц. При атопической бронхиальной астме основными продуцентами ФАТ являются эозинофилы и макрофаги, при инфекционнозависимой бронхиальной астме к этим клеткам присодиняются нейтрофилы. Имеются данные о влиянии ФАТ на пролиферацию В-лимфоцитов и стимуляцию продукции IgE: таким образом, ФАТ выступает как медиатор ГНТ. ФАТ обладает действием эндогенного вазодилататора легочных сосудов и принимает участие в поддержании низкого уровня сосудистого сопротивления в системе легочной артерии, с чем, возможно, связана редкость высокого давления в системе легочной артерии у больных ХНЗЛ (в отличие от больных первичной легочной гипертензией и рецидивирующей тромбоэмболией мелких ветвей легочной артерии). С другой стороны, у некоторых больных бронхиальной астмой при возможном развитии легочного эозинофильного микроваскулита этого протективного вазодилатирующего действия оказывается недостаточно, во всяком случае, показано, что у ряда больных бронхиальной астмой по мере нарастания эозинофилии крови и уровня циркулирующих иммунных комплексов (ЦИК) повышается давление в легочной артерии. Эозинофилы и выделяемые ими БАВ ответственны за структурные изменения эпителия бронхов, базальной мембраны, слизистых желез, гладких мышц бронхов и нервных окончаний, а ФАТ, помимо бронхоконстрикторного действия и влияния на НГБ, способен увеличивать количество мелких сосудов слизистой оболочки бронхов и вызывать ее отек. В литературе имеются указания на нарушение микроциркуляции у больных бронхиальной астмой, причем нарушения реологии крови коррелируют с выраженностью бронхиальной обструкции. Однако уже на ранних этапах развития бронхиальной астмы и даже у некоторых больных с состоянием предастмы выявляются нарушения реологии крови, повышается агрегация тромбоцитов и эритроцитов, и эти изменения нарастают параллельно с нарушением бронхиальной проходимости. Сцинтиграфические исследования, проведенные у больных бронхиальной астмой, показали расстройства в капиллярном кровообращении: у многих больных определялась неравномерность распределения радиофармпрепарата в артериально-капиллярном русле легких, иногда – очаговые расстройства кровообращения вплоть до участков с полным выключением капиллярного кровотока. – Также рекомендуем “Бронхиальная астма и микроциркуляторные нарушения.” Оглавление темы “Бронхиальная астма и воспаление при нем.”: |
Источник
Бронхиальная астма – это хроническое неинфекционное заболевание дыхательных путей воспалительного характера. Приступ бронхиальной астмы часто развивается после предвестников и характеризуется коротким резким вдохом и шумным длительным выдохом. Обычно он сопровождается кашлем с вязкой мокротой и громкими свистящими хрипами. Методы диагностики включают оценку данных спирометрии, пикфлоуметрии, аллергопроб, клинических и иммунологических анализов крови. В лечении используются аэрозольные бета-адреномиметики, м-холинолитики, АСИТ, при тяжелых формах заболевания применяются глюкокортикостероиды.
Общие сведения
За последние два десятка лет заболеваемость бронхиальной астмой (БА) выросла, и на сегодняшний день в мире около 300 миллионов астматиков. Это одно из самых распространенных хронических заболеваний, которому подверженные все люди, вне зависимости от пола и возраста. Смертность среди больных бронхиальной астмой достаточно высока. Тот факт, что в последние двадцать лет заболеваемость бронхиальной астмой у детей постоянно растет, делает бронхиальную астму не просто болезнью, а социальной проблемой, на борьбу с которой направляется максимум сил. Несмотря на сложность, бронхиальная астма хорошо поддается лечению, благодаря которому можно добиться стойкой и длительной ремиссии. Постоянный контроль над своим состоянием позволяет пациентам полностью предотвратить наступление приступов удушья, снизить или исключить прием препаратов для купирования приступов, а так же вести активный образ жизни. Это помогает поддержать функции легких и полностью исключить риск осложнений.
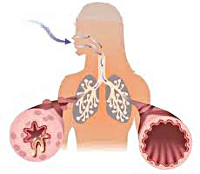
Бронхиальная астма
Причины
Наиболее опасными провоцирующими факторами для развития бронхиальной астмы являются экзогенные аллергены, лабораторные тесты на которые подтверждают высокий уровень чувствительности у больных БА и у лиц, которые входят в группу риска. Самыми распространенными аллергенами являются бытовые аллергены – это домашняя и книжная пыль, корм для аквариумных рыбок и перхоть животных, аллергены растительного происхождения и пищевые аллергены, которые еще называют нутритивными. У 20-40% больных бронхиальной астмой выявляется сходная реакция на лекарственные препараты, а у 2% болезнь получена вследствие работы на вредном производстве или же, например, в парфюмерных магазинах.
Инфекционные факторы тоже являются важным звеном в этиопатогенезе бронхиальной астмы, так как микроорганизмы, продукты их жизнедеятельности могут выступать в качестве аллергенов, вызывая сенсибилизацию организма. Кроме того, постоянный контакт с инфекцией поддерживает воспалительный процесс бронхиального дерева в активной фазе, что повышает чувствительность организма к экзогенным аллергенам. Так называемые гаптенные аллергены, то есть аллергены небелковой структуры, попадая в организм человека и связываясь его белками так же провоцируют аллергические приступы и увеличивают вероятность возникновения БА. Такие факторы, как переохлаждение, отягощенная наследственность и стрессовые состояния тоже занимают одно из важных мест в этиологии бронхиальной астмы.
Патогенез
Хронические воспалительные процессы в органах дыхания ведут к их гиперактивности, в результате которой при контакте с аллергенами или раздражителями, мгновенно развивается обструкция бронхов, что ограничивает скорость потока воздуха и вызывает удушье. Приступы удушья наблюдаются с разной периодичностью, но даже в стадии ремиссии воспалительный процесс в дыхательных путях сохраняется. В основе нарушения проходимости потока воздуха, при бронхиальной астме лежат следующие компоненты: обструкция дыхательных путей из-за спазмов гладкой мускулатуры бронхов или вследствие отека их слизистой оболочки; закупорка бронхов секретом подслизистых желез дыхательных путей из-за их гиперфункции; замещение мышечной ткани бронхов на соединительную при длительном течении заболевания, из-за чего возникают склеротические изменения в стенке бронхов.
В основе изменений бронхов лежит сенсибилизация организма, когда при аллергических реакциях немедленного типа, протекающих в виде анафилаксий, вырабатываются антитела, а при повторной встрече с аллергеном происходит мгновенное высвобождение гистамина, что и приводит к отеку слизистой бронхов и к гиперсекреции желез. Иммунокомплексные аллергические реакции и реакции замедленной чувствительности протекают аналогично, но с менее выраженными симптомами. Повышенное количество ионов кальция в крови человека в последнее время тоже рассматривается как предрасполагающий фактор, так как избыток кальция может провоцировать спазмы, в том числе и спазмы мускулатуры бронхов.
При патологоанатомическом исследовании умерших во время приступа удушья отмечается полная или частичная закупорка бронхов вязкой густой слизью и эмфизематозное расширение легких из-за затрудненного выдоха. Микроскопия тканей чаще всего имеет сходную картину – это утолщенный мышечный слой, гипертрофированные бронхиальные железы, инфильтративные стенки бронхов с десквамацией эпителия.
Классификация
БА подразделяется по этиологии, тяжести течения, уровню контроля и другим параметрам. По происхождению выделяют аллергическую (в т. ч. профессиональную БА), неаллергическую (в т. ч. аспириновую БА), неуточненную, смешанную бронхиальную астму. По степени тяжести различают следующие формы БА:
- Интермиттирующая (эпизодическая). Симптомы возникают реже одного раза в неделю, обострения редкие и короткие.
- Персистирующая (постоянного течения). Делится на 3 степени:
- легкая – симптомы возникают от 1 раза в неделю до 1 раза в месяц
- средняя – частота приступов ежедневная
- тяжелая – симптомы сохраняются практически постоянно.
В течении астмы выделяют обострения и ремиссию (нестабильную или стабильную). По возможности контроля над пристпуами БА может быть контролируемой, частично контролируемой и неконтролируемой. Полный диагноз пациента с бронхиальной астмой включает в себя все вышеперечисленные характеристики. Например, «Бронхиальная астма неаллергического происхождения, интермиттирующая, контролируемая, в стадии стабильной ремиссии».
Симптомы бронхиальной астмы
Приступ удушья при бронхиальной астме делится на три периода: период предвестников, период разгара и период обратного развития. Период предвестников наиболее выражен у пациентов с инфекционно-аллергической природой БА, он проявляется вазомоторными реакциями со стороны органов носоглотки (обильные водянистые выделения, непрекращающееся чихание). Второй период (он может начаться внезапно) характеризуется ощущением стесненности в грудной клетке, которое не позволяет дышать свободно. Вдох становится резким и коротким, а выдох наоборот продолжительным и шумным. Дыхание сопровождается громкими свистящими хрипами, появляется кашель с вязкой, трудно отхаркиваемой мокротой, что делает дыхание аритмичным.
Во время приступа положение пациента вынужденное, обычно он старается принять сидячее положение с наклоненным вперед корпусом, и найти точку опоры или опирается локтями в колени. Лицо становится одутловатым, а во время выдоха шейные вены набухают. В зависимости от тяжести приступа можно наблюдать участие мышц, которые помогают преодолеть сопротивление на выдохе. В периоде обратного развития начинается постепенное отхождение мокроты, количество хрипов уменьшается, и приступ удушья постепенно угасает.
Проявления, при которых можно заподозрить наличие бронхиальной астмы.
- высокотональные свистящие хрипы при выдохе, особенно у детей.
- повторяющиеся эпизоды свистящих хрипов, затрудненного дыхания, чувства стеснения в грудной клетке и кашель, усиливающийся в ночной время.
- сезонность ухудшений самочувствия со стороны органов дыхания
- наличие экземы, аллергических заболеваний в анамнезе.
- ухудшение или возникновение симптоматики при контакте с аллергенами, приеме препаратов, при контакте с дымом, при резких изменениях температуры окружающей среды, ОРЗ, физических нагрузках и эмоциональных напряжениях.
- частые простудные заболевания «спускающиеся» в нижние отделы дыхательных путей.
- улучшение состояние после приема антигистаминных и противоастматических препаратов.
Осложнения
В зависимости от тяжести и интенсивности приступов удушья бронхиальная астма может осложняться эмфиземой легких и последующим присоединением вторичной сердечно-легочной недостаточности. Передозировка бета-адреностимуляторов или быстрое снижение дозировки глюкокортикостероидов, а так же контакт с массивной дозой аллергена могут привести к возникновению астматического статуса, когда приступы удушья идут один за другим и их практически невозможно купировать. Астматический статус может закончиться летальным исходом.
Диагностика
Диагноз обычно ставится клиницистом-пульмонологом на основании жалоб и наличия характерной симптоматики. Все остальные методы исследования направлены на установление степени тяжести и этиологии заболевания. При перкуссии звук ясный коробочный из-за гипервоздушности легких, подвижность легких резко ограничена, а их границы смещены вниз. При аускультации над легкими прослушивается везикулярное дыхание, ослабленное с удлиненным выдохом и с большим количеством сухих свистящих хрипов. Из-за увеличения легких в объеме, точка абсолютной тупости сердца уменьшается, тоны сердца приглушенные с акцентом второго тона над легочной артерией. Из инструментальных исследований проводится:
- Спирометрия. Спирография помогает оценить степень обструкции бронхов, выяснить вариабельность и обратимость обструкции, а так же подтвердить диагноз. При БА форсированный выдох после ингаляции бронхолитиком за 1 секунду увеличивается на 12% (200мл) и более. Но для получения более точной информации спирометрию следует проводить несколько раз.
- Пикфлоуметрия. Измерение пиковой активности выдоха (ПСВ) позволяет проводить мониторинг состояния пациента, сравнивая показатели с полученными ранее. Увеличение ПСВ после ингаляции бронхолитика на 20% и более от ПСВ до ингаляции четко свидетельствует о наличии бронхиальной астмы.
Дополнительная диагностика включает в себя проведение тестов с аллергенами, ЭКГ, бронхоскопию и рентгенографию легких. Лабораторные исследования крови имеют большое значение в подтверждении аллергической природы бронхиальной астмы, а так же для мониторинга эффективности лечения.
- Анализа крови. Изменения в ОАК – эозинофилия и незначительное повышение СОЭ – определяются только в период обострения. Оценка газового состава крови необходима во время приступа для оценки тяжести ДН. Биохимический анализ крови не является основным методом диагностики, так как изменения носят общий характер и подобные исследования назначаются для мониторинга состояния пациента в период обострения.
- Общий анализ мокроты. При микроскопии в мокроте можно обнаружить большое количество эозинофилов, кристаллы Шарко-Лейдена (блестящие прозрачные кристаллы, образующиеся после разрушения эозинофилов и имеющие форму ромбов или октаэдров), спирали Куршмана (образуются из-за мелких спастических сокращений бронхов и выглядят как слепки прозрачной слизи в форме спиралей). Нейтральные лейкоциты можно обнаружить у пациентов с инфекционно-зависимой бронхиальной астмой в стадии активного воспалительного процесса. Так же отмечено выделение телец Креола во время приступа – это округлые образования, состоящие из эпителиальных клеток.
- Исследование иммунного статуса. При бронхиальной астме количество и активность Т-супрессоров резко снижается, а количество иммуноглобулинов в крови увеличивается. Использование тестов для определения количества иммуноглобулинов Е важно в том случае, если нет возможности провести аллергологические тесты.
Лечение бронхиальной астмы
Поскольку бронхиальная астма является хроническим заболеванием вне зависимости от частоты приступов, то основополагающим моментом в терапии является исключение контакта с возможными аллергенами, соблюдение элиминационных диет и рациональное трудоустройство. Если же удается выявить аллерген, то специфическая гипосенсибилизирующая терапия помогает снизить реакцию организма на него.
Для купирования приступов удушья применяют бета-адреномиметики в форме аэрозоля, для того чтобы быстро увеличить просвет бронхов и улучшить отток мокроты. Это фенотерола гидробромид, сальбутамол, орципреналин. Доза в каждом случае подбирается индивидуально. Так же хорошо купируют приступы препараты группы м-холинолитиков – аэрозоли ипратропия бромида и его комбинации с фенотеролом.
Ксантиновые производные пользуются среди больных бронхиальной астмой большой популярностью. Они назначаются для предотвращения приступов удушья в виде таблетированных форм пролонгированного действия. В последние несколько лет препараты, которые препятствуют дегрануляции тучных клеток, дают положительный эффект при лечении бронхиальной астмы. Это кетотифен, кромогликат натрия и антагонисты ионов кальция.
При лечении тяжелых форм БА подключают гормональную терапию, в глюкокортикостероидах нуждается почти четверть пациентов, 15-20 мг Преднизолона принимают в утренние часы вместе с антацидными препаратами, которые защищают слизистую желудка. В условиях стационара гормональные препараты могут быть назначены в виде инъекций. Особенность лечения бронхиальной астмы в том, что нужно использовать лекарственные препараты в минимальной эффективной дозе и добиваться еще большего снижения дозировок. Для лучшего отхождения мокроты показаны отхаркивающие и муколитические препараты.
Прогноз и профилактика
Течение бронхиальной астмы состоит из череды обострений и ремиссий, при своевременном выявлении можно добиться устойчивой и длительной ремиссии, прогноз же зависит в большей степени от того, насколько внимательно пациент относится к своему здоровью и соблюдает предписания врача. Большое значение имеет профилактика бронхиальной астмы, которая заключается в санации очагов хронической инфекции, борьбе с курением, а так же в минимизации контактов с аллергенами. Это особенно важно для людей, которые входят в группу риска или имеют отягощенную наследственность.
Источник

