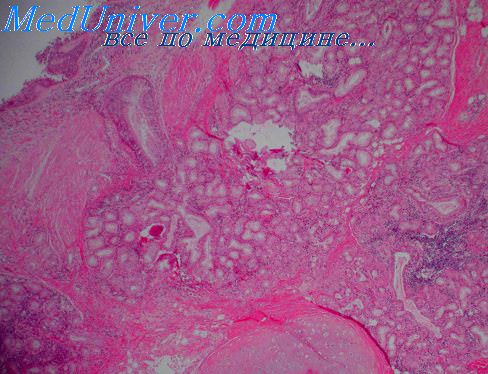
Клетки воспаления при бронхиальной астме

Преимущественно эозинофильные варианты воспаления бронхов при бронхиальной астме.Бронхиальная астма – самое частое заболевание легких, в основе которого лежит эозинофильное воспаление, но принимают участие также другие клетки, причем точное значение каждого типа клеток и медиаторов в его патогенезе неизвестно. При бронхиальной астме отмечается разнообразие воспалительных изменений в бронхах. Принятое в 1993 г. международное соглашение “Global Strategy for Asthma Management” определяет бронхиальную астму как “хроническое воспалительное заболевание дыхательных путей, при котором многие клетки играют определенную роль, включая тучные клетки и эозинофилы”. Только у больны бронхиальной астмой обнаружено интраэпителиальное присутствие эозинофилов и наличие дегранулированных эозинофилов в повышенном количестве под базальной мембраной, вместе с тем найдена корреляция между содержанием дегранулированных эозинофилов, повреждением эпителия бронхов и тяжестью течения бронхиальной астмы. Эозинофилы в содержимом бронхоальвеолярного лаважа сохраняются у больных бронхиальной астмой в межприступный период и выявлена прямая зависимость между уровнем эозинофилов в лаважной жидкости и тяжестью течения бронхиальной астмы. Сохранение воспалительных изменений в бронхах у больных бронхиальной астмой в межприступный период, которое проявляется повышенным содержанием в лаважной жидкости эозинофилов и нейтрофилов, а также перманентным состоянием повышенной реактивности бронхов, способствует тому, что любые внешние и внутренние агенты, играющие роль триггера, могут мобилизировать эти клетки воспаления и вызвать обострение болезни. Повреждение эпителия “большим основным протеином” эозинофилов играет важную роль в развитии неспецифической гиперреактивности бронхов (НГБ) и бронхиальной астмы, которую некоторые авторы даже называют “болезнью эпителия”, поскольку клетки эпителия бронхов выделяют вещества, способные модулировать деятельность гладкой мускулатуры брохов, секретируют производные арахидоновой кислоты, а также содержат чувствительные нервные окончания, раздражение которых ведет через рефлекторные механизмы к выделению нейропептидов, в частности, нейрокинов, вещества П, играющих важную роль в развитии бронхообструкции. “Большой основной протеин” эозинофилов а также эозинофильный катионный белок и эозинофильный нейротоксин вызывают повреждение эпителия, десквамацию и разрушение ресничных клеток, что является типичным при бронхиальной астме. Концентрация эозинофильного катионного белка в мокроте и в периферической крови коррелирует со степенью бронхообструкции . Как правило, имеется прямая зависимость между увеличением количества эозинофилов в содержимом бронхоальвеолярного лаважа и в периферической крови. Количество эозинофилов в периферической крови позволяет судить об общей (системной) аллергизации, и предлагается по степени эозинофилии крови судить о тяжести течения бронхиальной астмы и выраженности обострения болезни. Обнаружено, что НГБ коррелирует с повышением количества эозинофилов в периферической крови даже у лиц без клинических признаков бронхиальной астмы. Иногда бывают отклонения от обычного соответствия количества эозинофилов периферической крови и лаважной жидкости. Это может быть объяснено существованием независимых хемотаксических факторов, действующих в капиллярах большого круга и в альвеолах.
Экспериментальные модели бронхообструктивного синдрома у животных а также ингаляционные провокации различными аллергенами больных бронхиальной астмой показали, что возможно развитие одной или двух фаз патологического процесса: ранняя астматическая реакция, характеризуемая быстрой бронхоконстрикцией с максимумом через 10-30 мин после провокации и постепенным ослаблением в течение последующих 2 часов, и поздняя астматическая реакция, возникающая через 6-8 часов после провокации у 60% больных бронхиальной астмой, с максимумом бронхоконстрикции еще через 2-4 часа. Если основной клеткой, ответственной за развитие ранней астматической реакции, является тучная клетка, то поздняя астматическая реакция связана с привлечением в легкие различных видов клеток, прежде всего эозинофилов, и возникновением хронического воспаления в IgE-опосредованных реакциях. Развитие поздней астматической реакции сопровождается транзиторным снижением количества эозинофилов в периферической крови при повышенном их содержании в бронхиальных смывах, что указывает на избирательное привлечение этих клеток из бронхиальных сосудов и сопровождается повышением НГБ. Впрочем, как сейчас считается, у больных с хроническим персистирующим течением бронхиальной астмы различия между ранней и поздней астматической реакциями не столь явные и тучные клетки и их медиаторы принимают активное участие в развитии хронического воспаления. У больных с поздней астматической реакций не просто изменяется количество эозинофилов, но определяются их качественные изменения: начинают преобладать эозинофилы низкой плотности (плотность меньше 1,095 г/мл), которые более активны, экспрессируют на своей мембране больше рецепторов к IgE и выделяют большее количество БАВ, причем увеличение количества активных эозинофилов коррелирует с тяжестью течения бронхиальной астмы обнаружили в биопсинном материале слизистой бронхов даже у больных с легким течением бронхиальной астмы увеличеннное количество активных эозинофилов, тучных клеток, а также клеток, содержащих фактор некроза опухолей а-цитокина, сходного по своим действиям с интерлеикином-1 и являющимся первичным медиатором воспаления. Некоторые авторы подчеркивают, что эозинофил является мощной эффекторной клеткой, главным образом, в позднюю фазу астматической реакции, проявляющейся аллергическим воспалением преимущественно дистальных отделов бронхов. Возможно, что это особенно справедливо в отношении атонической бронхиальной астмы Привлечение, активация и поддержка длительного существования эозинофилов в слизистом и подслизистом слоях бронхиального дерева вызывается действием многих БАВ, среди которых особенно выделяют интерлейкены 3 и 5, гранулоцитарномакрофагальный колониестимулирующий фактор и фактор некроза опухолей. В настоящее время считается, что одним из ключевых моментов в патогенезе бронхиальной астмы является взаимодействие эозинофила и фактора агрегации тромбоцитов (ФАТ). Дело в том, что эозинофилы – клетки, которые продуцируют ФАТ и в то же время являются объектами его действия: ФАТ вызывает активацию и дегрануляцию эозинофилов и обуславливает их хемотаксис. Показано, что ФАТ вызывает усиление экспрессии Fc-рецепторов для IgC на неактивированных эозинофилах у больных бронхиальной астмой, вовлекая эти клетки в иммунные реакции. ФАТ рассматривается как общая эффекторная субстанция анафилаксии, он также индуцирует агрегацию тромбоцитов с выделением ими серотонина, гистамина, 3 и 4 факторов тромбоцитов, что приводит не только к бронхоспазму, но и нарушениям микроциркуляции. ФАТ может непосредственно повышать проницаемость микрососудов дыхательных путей, что приводит к выходу плазмы, нейтрофилов, моноцитов и эозинофилов. Посредством всех этих механизмов ФАТ вызывает состояние гиперреактивности бронхов по отношению к широкому спектру специфических и неспецифических раздражителей и как модулятор воспалительных реакций вместе с другими воспалительными медиаторами вызывает десенситизацию адренорецепторов у больных БА. Показана роль ФАТ как единственного вещества, вызывающего повышение неспецифической бронхиальной гиперчувствительности и гиперреактивности у здоровых лиц. При атопической бронхиальной астме основными продуцентами ФАТ являются эозинофилы и макрофаги, при инфекционнозависимой бронхиальной астме к этим клеткам присодиняются нейтрофилы. Имеются данные о влиянии ФАТ на пролиферацию В-лимфоцитов и стимуляцию продукции IgE: таким образом, ФАТ выступает как медиатор ГНТ. ФАТ обладает действием эндогенного вазодилататора легочных сосудов и принимает участие в поддержании низкого уровня сосудистого сопротивления в системе легочной артерии, с чем, возможно, связана редкость высокого давления в системе легочной артерии у больных ХНЗЛ (в отличие от больных первичной легочной гипертензией и рецидивирующей тромбоэмболией мелких ветвей легочной артерии). С другой стороны, у некоторых больных бронхиальной астмой при возможном развитии легочного эозинофильного микроваскулита этого протективного вазодилатирующего действия оказывается недостаточно, во всяком случае, показано, что у ряда больных бронхиальной астмой по мере нарастания эозинофилии крови и уровня циркулирующих иммунных комплексов (ЦИК) повышается давление в легочной артерии. Эозинофилы и выделяемые ими БАВ ответственны за структурные изменения эпителия бронхов, базальной мембраны, слизистых желез, гладких мышц бронхов и нервных окончаний, а ФАТ, помимо бронхоконстрикторного действия и влияния на НГБ, способен увеличивать количество мелких сосудов слизистой оболочки бронхов и вызывать ее отек. В литературе имеются указания на нарушение микроциркуляции у больных бронхиальной астмой, причем нарушения реологии крови коррелируют с выраженностью бронхиальной обструкции. Однако уже на ранних этапах развития бронхиальной астмы и даже у некоторых больных с состоянием предастмы выявляются нарушения реологии крови, повышается агрегация тромбоцитов и эритроцитов, и эти изменения нарастают параллельно с нарушением бронхиальной проходимости. Сцинтиграфические исследования, проведенные у больных бронхиальной астмой, показали расстройства в капиллярном кровообращении: у многих больных определялась неравномерность распределения радиофармпрепарата в артериально-капиллярном русле легких, иногда – очаговые расстройства кровообращения вплоть до участков с полным выключением капиллярного кровотока. – Также рекомендуем “Бронхиальная астма и микроциркуляторные нарушения.” Оглавление темы “Бронхиальная астма и воспаление при нем.”: |
Источник
Изменения эпителия бронхов при бронхиальной астме.Своеобразным вариантом эозинофильного воспаления является сочетание эозинофильного или эозинофильно-нейтрофильного воспаления с появлением в бронхиальном смыве измененного эпителия бронхов. Эпителий бронхов – одна из главных мишеней для атаки активных клеток воспаления у больных бронхиальной астмой, и изменения эпителия играют важную роль в патогенезе этого заболевания. Нами с помощью COMOD-технологии выделена группа больных с эозинофильно-нейтрофильным воспалением и наличием измененного эпителия бронхов. В эту группу входили больные бронхиальной астмой средней степени тяжести и тяжелой, у которых выявлялась колонизация бронхов непатогенной и условно-патогенной микрофлорой, вирусная инфекция, иммунные нарушения (определялись в высоком титре циркулирующие иммунные комплексы – ЦИК). Обнаружена достоверная связь между появлением в бронхиальном смыве измененного бронхиального эпителия и показателями, характеризующими преимущественно отечный механизм нарушения бронхиальной проходимости: достоверные изменения ОФВ, после подкожной инъекции 1 мл 0,1% раствора адреналина, но не после ингаляции беротека. Важно также отметить, что у выделенных COMOD-технологией в эту группу больных преобладало нарушение бронхиальной проходимости на уровне дистальных бронхов: преимущественное снижение мгновенных скоростей воздушного потока при выдохе 50% и 75% ЖЕЛ, но не максимальной скорости воздушного потока на выдохе первой четверти ФЖЕЛ. В генезе нарушения проходимости на уровне дистальных бронхов существенную роль может играть отечный механизм. Такой механизм описан недавно, в частности у больных аспириновой бронхиальной астмы. У больных описываемой группы выявлены нарушения обмена ККС, вероятно, связанные с вирусной инфекцией, и также, способствующие отечному механизму бронхообструкции и нарушениям микроциркуляции. У этих же больных найдено повышение уровня свободного серотонина в периферической крови, что может свидетельствовать о нарушении его инактивации эндотелием легочных сосудов и считаться маркером повреждения легочного эндотелия, наряду с таким общеизвестным показателем повреждения сосудистого эндотелия, как повышение активности фактора Виллебранда, нередко выявляемое у больных бронхиальной астмой. Повреждение эндотелия в этой группе больных может быть связано с фиксацией на нем ЦИК, о повышении которых говорилось ранее, и по крайней мере у некоторых больных нельзя исключить иммунный васкулит легочных микрососудов.
Найденные изменения укладываются в предложенные концептуальные модели нарушения микроциркуляции и иммунного васкулита у больных бронхиальной астмой и находятся в русле работ последних лет, в которых состоянию сосудов легких уделяется особое внимание, о чем писалось ранее. Таким образом, выделенная нами группа больных с эозинофильно-нейтрофильным воспалением в сочетании с появлением в бронхиальном смыве измененного эпителия бронхов относится к инфекционно-зависимому и аутоиммунному клинико-патогенетическим вариантам бронхиальной астмы. Не исключается, что выявленная у этих больных колонизация бронхов различной микрофлорой, соответствующая полученным в последнее время данным о высокой чувствительности к бактериальной адгезии вновь растущих покровых клеток, закрывающих повреждения эпителия, является толчком к развитию аутоиммунного процесса, учитывая способность некоторых бактерий и вирусов нарушать толерантность к собственным антигенам хозяина. У некоторых больных бронхиальной астмой выделено эозинофильно-мононуклеарное воспаление: эозинофильно-макрофагальное и эозинофильно-моноцитарное (частота 0,36-0,32 среди эозинофильных вариантов воспаления в зависимости от исходной базы данных). Ранее было указано, что у многих больных бронхиальной астмой выявляется “макрофагальный дефицит”- низкое содержание макрофагов среди клеток бронхиального смыва, что может рассматриваться как проявление снижения местной защитной реакции, исходя их сложных кооперативных функций макрофагов в регуляции иммунного воспаления. Вместе с тем, в условиях патологии, в частности при БА, альвеолярные макрофаги, составляющие 90% всех клеток дыхательных путей (около 500 млн. клеток), могут играть первичную роль в патогенезе болезни, поскольку имеют рецепторы к IgE и выделяют различные медиаторы воспаления. Д,Н. Маянский считает, что аллергическое воспалениек при бронхиальной астме проявляется преимущественно как вариант мононуклеарно-ин-фильтративного воспаления, и ведущую роль в его патогенезе играют фагоциты – эффекторы воспалительной реакции. И.Г. Даниляк указывает на важную патогенетическую роль свободных радикалов, выделяемых фагоцитами, в частности альвеолярными макрофагами, и говорит о существовании “фагоцитарно-свободнорадикального” варианта бронхиальной астмы. Другие авторы подчеркивают, что свободные радикалы после антигенного воздействия выделяют преимущественно макрофаги, а не нейтрофилы. Увеличение содержания в бронхиальвеолярном лаваже мононуклеаров, прежде всего, лимфоцитов, по данным многих авторов, коррелирует с тяжестью течения бронхиальной астмы. Интерлейкины, выделяющиеся в зоне воспаления, и в частности ИЛ-2, связываясь с поверхностными клеточными рецепторами (IL-2R), вызывают клональную экспансию антигенстимулированных Т-лимфоцитов и играют ключевую роль в активации иммунной системы и в трансформации острого иммунного воспаления в хроническое. Л.К. Романова и соавт. выделяет особый лимфоцитар-ный вариант воспаления бронхов при бронхиальной астме. По мнению Г.Б. Федосеева и соавт. лимфоциты характеризуют хронический компонент воспаления при бронхиальной астме. Увеличение количества лимфоцитов в просвете бронхов у больных бронхиальной астмой часто сочетается с увеличением количества эозинофилов, при этом лимфоциты продуцируют провоспалительные кинины и нарушено соотношение Т и В-лимфоцитов, причем количество В-лимфоцитов увеличивается, а Т-лимфоцитов снижается. Мононуклеары, в том числе лимфоциты, впервые появляются через 24 часа после начальной дегрануляции тучных клеток под воздействием аллергена и, следовательно, характеризуют позднюю реакцию при бронхиальной астме. При поздней аллергической реакции особенно важно взаимодействие эозинофилов и лимфоцитов. – Вернуться в оглавление раздела “Пульмонология.” Оглавление темы “Бронхиальная астма и воспаление при нем.”: |
Источник
Активность нейтрофилов при различных видах бронхиальной астмы.Нейтрофилы активно включаются в воспалительный процесс у больных бронхиальной астмой, и это не свидетельствует об инфекционной природе воспаления: активированные аллергеном тучные клетки выделяют высокомолекулярный фактор хемотаксиса нейтрофилов, также активированные макрофаги выделяют фактор, активирующий нейтрофилы и привлекающий их в очаг воспаления из периферической крови. В экспериментальной модели бронхиальной астмы показано, что при развитии только ранней астматической реакции возникает нейтрофильное воспаление, а при развитии как ранней, так и поздней астматической реакции воспаление сразу же носит черты эозинофильно-нейтрофильного. Считается, что в дистальных отделах дыхательных путей у здоровых лиц содержатся лишь единичные полиморфноядерные нейтрофилы, а увеличение их количества является признаком воспалительной реакции и следствием воздействия поллютантов. Известно, что профессиональная бронхиальной астма, вызванная толуеном, ассоциируется с повышением чувствительности бронхов, развитием острого нейтрофильного воспаления со вторичным привлечением эозинофилов. Активированные макрофаги и нейтрофилы вызывают дисбаланс системы протеолиз-ингибиторы протеолиза, выделяя различные протеазы, что приводит у больных бронхиальной астмой к относительному недостатку ингибитора протеаз. Неспецифическая гиперреактивность бронхов, астматический бронхит и БА обнаружены у лиц с генетическим дефицитом ингибитора протеаз, в частности у гетерозиготных носителей гена дефицита ингибитора протеаз. В процессе фагоцитоза клетки, содержащиеся в бронхах, и прежде всего макрофаги и нейтрофилы, выделяют повышенное количество различных активированных метаболитов, высокий уровень которых, либо недостаточная активность антиоксидантных механизмов приводят к “окислительному стрессу”, который играет большую роль в усилении процессов воспаления в бронхолегочной системе и повреждении легочной ткани. В результате действия свободных радикалов окислению подвержены все молекулы, но наибольшую опасность представляет окисление нуклеиновых кислот, ферментов и ненасыщенных липидов – процессы перекисного окисления липидов (ПОЛ). Активация ПОЛ приводит к повышению ригидности мембранных фосфолипидов, снижает их текучесть и может вызвать снижение чувствительности адренорецепторов. У больных бронхиальной астмой выявлен дефицит антиоксидантных систем, в том числе генетически обусловленный, что снижает компенсаторные возможности при свободнорадикальной патологии и в итоге приводит к усилению бронхиальной обструкции за счет бронхоспазма и отека слизистой в условиях стимуляции кининогенеза и повышения сосудистой проницаемости. По мнению Абдусаламова А.Б. и Шафера A.M. активация ПОЛ выявляется практически у всех больных бронхиальной астмой, и этот процесс играет роль в формировании гиперреактивности бронхов. Имеются данные о большем дисбалансе в системе ПОЛ-антиоксиданты у больных инфекционно-зависимой бронхиальной астмой.
Нейтрофилы относятся к клеткам, наиболее интенсивно образующим активные формы кислорода (АФК), и у больных БА в зависимости от степени тяжести и фазы заболевания обнаружено снижение присущего здоровым ингибирующего влияния тромбоцитов, углекислоты и гистамина на выделение АФК. Гистамин модулирует генерацию АФК лейкоцитами, а АФК усиливают выделение гистамина, формируя тем самым “порочный круг”. Снижение ингибирующего действия тромбоцитов на выделение АФК может быть связано с функциональными и морфологическими изменениями тромбоцитов у больных БА: они становятся сферическими, возрастает количество тромбоцитов с псевдоподиями и выявляются нарушения их ультраструктурной организации. В связи со значимой ролью АФК некоторые авторы предлагают выделить самостоятельный свободнорадикальный клинико-патогенетический вариант БА. Тесно связанные с выделением АФК процессы ПОЛ вызывают повреждение клеточных мембран, усиливают их проницаемость, потенцируют воспаление бронхов, вызывают гиперкоагуляцию, вплоть до появления маркеров ДВС-синдрома, что определяет прогрессирование микроциркуляционных нарушений у больных ХНЗЛ. АФК могут играть роль в формировании аутоиммунного процесса, поскольку одна из форм АФК – пероксид водорода – относительно устойчив, способен к длительной диффузии и окислительной модификации эндогенных макромолекул, что вызывает появление тканевых структур со свойствами аутоантигенов. Усиление продукции АФК, особенно в условиях истощения антиоксидантной защиты, что типично для больных ХНЗЛ, связано также с присоединением вирусной и бактериальной инфекции. У больных бронхиальной астмой выявлен так называемый “макрофагальный дефицит”: уменьшение количества макрофагов в бронхиальных смывах, обнаружено снижение количества моноцитов в периферической крови, функциональная неполноценность мононуклеаров,- снижение фагоцитоза, угнетение Fc и СЗ рецепторов на мембранах моноцитов и альвеолярных макрофагов. Все это позволяет рассматривать “макрофагальный дефицит” в лаважной жидкости как маркер нарушения местной защиты бронхов. У 50% больных БА, обследованных нами, было выявлено снижение количества макрофагов в бронхиальных смывах. В связи с этим понятна частота выявления патогенной (пневмококки, гемофильная палочка), условно-патогенной и непатогенной микрофлоры (различные виды кокковой флоры, протей, нейсерии) в материалах бронхиальных смывов и мокроты в диагностически значимых титрах (частота обнаружения патогенной и непатогенной микрофлоры 0,325 и 0,722 соответственно). Обнаружение непатогенной и условно-патогенной микрофлоры означает колонизацию бронхиального дерева микроорганизмами, и нам с помощью COMOD-технологии удалось выявить достоверную связь этого феномена с развитием эозинофильного воспаления, тяжестью приступов удушья и дисбалансом некоторых биологически активных веществ (БАВ) и в частности, компонентов калликреин-кининовой системы (ККС). При этом отсутствовали клинические признаки активного воспалительного процесса и не было связи с фазой заболевания, в отличие от выявления патогенной микрофлоры, связанной с фазой обострения БА, явными клиническими признаками инфекции и чаще обнаруживаемой у курящих мужчин с признаками хронического обструктивного бронхита. – Также рекомендуем “Роль микроорганизмов в развитии бронхиальной астмы.” Оглавление темы “Бронхиальная астма и воспаление при нем.”: |
Источник