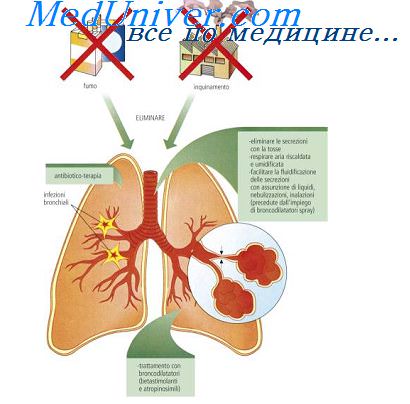
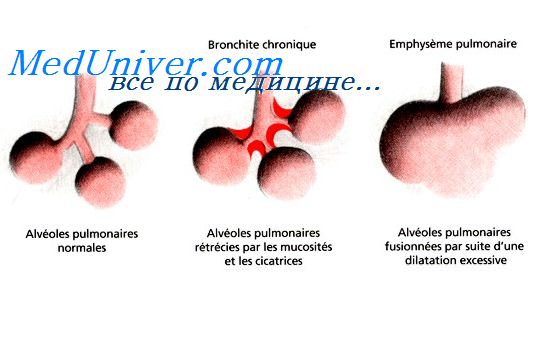
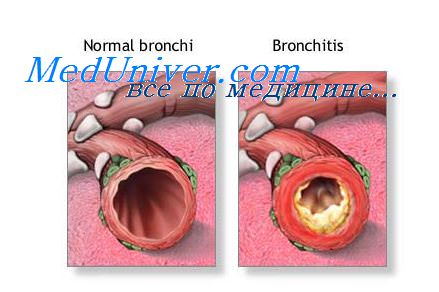
Клеточные изменения при воспалении

Клеточные механизмы защитных реакций организма при воспалении.Основные закономерности развития необратимых патологических изменений в клетках при первичной и вторичной альтерации Рассматривая воспаление как типовой патологический процесс, протекающий в виде последовательно сменяющих друг друга, а в ряде случаев развивающихся параллельно стадий альтерации, экссудации и пролиферации, необходимо отметить, что при определенных условиях течение воспалительных реакций может иметь как преимущественно защитно-приспособительный, так и разрушительный характер. Воздействие на ткани различных по своей природе факторов (химических, физических, бактериальных), как правило, приводит к развитию первичной альтерации. Степень выраженности и распространенность альтеративных изменений определяется интенсивностью действующего фактора, устойчивостью клеток к этому воздействию и способностью клеточных механизмов компенсировать патологические изменения. Повреждение ткани сопровождается выделением биологически активных веществ, способных еще в большей степени увеличивать альтеративные процессы – вызывать вторичную альтерацию. Независимо от особенностей воздействующего фактора, индуцирующего воспалительный процесс, все изменения в клетках можно свести к следующим типам:
Деструктивные процессы в тканях, возникающие в альтернативной стадии (фазе) воспаления, имеют преимущественно патологический характер. Их выраженностью в значительной степени определяется возможная степень неблагоприятного течения воспалительного процесса в целом. При обратимых сублетальных изменениях клетка способна адаптироваться и восстанавливать свою структуру и функцию. В этом случае, как правило, происходит снижение интенсивности метаболических процессов, ограничение потребления кислорода, угнетение процессов окислительного фосфорилирования, активирование гликолиза, уменьшение запасов макроэргических фосфорных соединений, падение уровня активности K-Na-АТФ-азы, ингибирование внутриклеточных ферментов, активирующих анаболические процессы. В процессе необратимого повреждения клетки наблюдается постепенное увеличение объема внутриклеточных структур (расширение эндоплазматической сети, набухание митохондрий, увеличение объема лизосом). Летальные изменения в клетках сопровождаются повреждением наружной и внутриклеточных мембран, в результате чего повышается их пассивная проницаемость для ионов. Одним из кардинальных признаков повреждения клетки является увеличение содержания натрия в цитозоле и выход во внеклеточную среду калия. Тяжелые метаболические расстройства клеточных функций сопровождаются увеличением содержания кальция в цитозоле. В нормальных условиях в цитоплазме регистрируется низкая концентрация кальция, не превышающая 10″‘ моль/л, которая обеспечивается непрерывной работой Са-АТФаз. Основные запасы кальция содержатся в эндоплазматическом ретикулуме, большая часть мембраны которого плотно покрыта белком с молекулярной массой 110 кДа, являющегося Са-насосом. Концентрация кальция в эндоплазматическом ретикулуме в 10 000-100 000 раз выше чем в цитозоле. Деполяризация клеточной мембраны и гидролиз мембранных липидов сопровождаются раскрытием кальциевых каналов, по которым кальций из внутриклеточных депо (цистерн эндоплазматического ретикулума, митохондрий) или интерстициального пространства устремляется в цитозоль. Возникающие в ходе воспаления метаболические нарушения энергообеспечения работы транспортных систем клеток изменяют нормальное протекание процессов реабсорбции кальция, который устремляется из кальцийсодержащих структур и внеклеточной среды в цитозоль по механизмам пассивного транспорта. – Также рекомендуем “Изменения клеток при альтеративной стадии воспаления.” Оглавление темы “Ключевые механизмы воспаления легких.”: |
Источник
Изменения клеток при альтеративной стадии воспаления.Наибольшее увеличение цитозольной фракции кальция наблюдается в условиях деградации клеточных мембран, нарушений структурной целостности мембран митохондрий, повышения проницаемости лизосомальных мембран с лабилизацией лизосомальных ферментов. Все перечисленные изменения влекут за собой увеличение зоны деструкции в очаге воспаления. Принято считать, что появление в плазмолемме дефектов на протяжении более 3-4 нм, а также снижение цитоплазматического рН на 2 единицы и более свидетельствует о необратимом повреждении клетки (Пермяков Н.К., 1986). В развитии летальных клеточных изменений существенную роль играет активирование свободнорадикального окисления мембранных фосфолипидов. Воздействие патогенных факторов, вызывающих альтерацию, приводит к нарушению оптимального для неповрежденной клетки соотношения функциональной активности прооксидантных и антиоксидантных систем, что сопровождается активированием свободнорадикальных процессов. В ходе альтерации наблюдается ухудшение сопряжения окисления и фосфорилирования, приводящее к нарушениям утилизации кислорода. Это создает дополнительные условия для увеличения интенсивности свободнорадикального окисления мембранных фосфолипидов.
Активирование свободнорадикальных процессов влечет за собой повреждение клеточных мембран, в результате чего нарушаются основные их функции (транспортная, каталитическая и рецепторная). Изменения структуры полиненасыщенных жирных кислот, входящих в состав мембранных фосфолипидов, сопровождаются снижением гидрофобности фосфолипидного бислоя, уменьшением молекулярной подвижности фосфолипидов и нарушениями процессов липид-белковых взаимодействий. Это приводит к увеличению пассивной проницаемости клеточных мембран для ионов, изменениям ионных градиентов, нарушениям процессов биоэлектрогенеза, дисбалансу обмена жидкости между клеткой и внеклеточной средой. Свободнорадикальное окисление фосфолипидов мембран митохондрий сопровождается снижением уровня активности мембраносвязанных ферментов, участвующих в процессах окислительного фосфолирирования, в результате чего снижается его интенсивность. Повреждение в ходе альтеративных процессов клеточных мембран сопровождается нарушением их рецепторных свойств. При этом понижается, вплоть до полного угнетения, способность клетки реагировать на физиологические концентрации биологически активных веществ. Результатом альетеративных изменений в клеточных мембранах является ингибирование процессов, протекающих с участием таких внутриклеточных посредников, как цАМФ и цГМФ, а также триггерных белков. Таким образом, альтеративная стадия воспаления, независимо от вида ткани, в которой оно развивается, имеет преимущественно патологический характер, выраженность которого коррелирует с глубиной и тяжестью деструктивных процессов. В ответ на повреждение в клетке происходят защитно-приспособительные изменения: – Также рекомендуем “Эксудация и эксудативные процессы в ходе воспаления.” Оглавление темы “Ключевые механизмы воспаления легких.”: |
Источник
Своеобразие вирусного воспаления на клеточном уровне.Особенности вирусного воспаления на клеточном уровне, также как и на субклеточном, обусловлены морфологическими и функциональными особенностями вирусных частиц. Аналогично воспалению, обусловленному другими инфекционными агентами, возможно развитие двух основных форм воспаления: острого и хронического. Принципиальная схема острого воспаления также сходна: повреждение клеток – выход гидролитических ферментов – нарушение проницаемости сосудистой стенки эндотелия и его базальной мембраны под влиянием продуктов деградации тучных клеток и активированных фагоцитов – диапедез форменных элементов крови и появление экссудата. И все-таки существуют принципиальные различия. Бактерии, за редким исключением (гонококки, менингококки), воздействуют на клетки-мишени извне с помощью различных ферментов и токсинов, которые нередко ведут к полному расплавлению наружнрой мембраны. Вирусы осуществляют процесс воспаления как снаружи, так и изнутри клетки. Основой защитной воспалительной реакции при бактериальной инфекции служат нейтрофилы, заглатывающие и переваривающие их, а также выделяющие ряд высокоактивных веществ. При этом возникает целый ряд кислородозависимых и кислородонезависимых защитных реакций, продукты которых (супероксид О2, Н202, ОН и др.) обладают мощным бактерицидным действием и в то же время способны повреждать собственные клетки хозяина. Кроме того, полиморфноядерные лейкоциты (ПМЛ) выделяют лизосомальные гидролазы, катепсины и эластазу, которая отслаивает эндотелиоциты от базальной мембраны. Биоокислители (02, Н202) разрушают ингибиторы протеаз и провоцируют образование медиаторов проницаемости, которые, наряду с системой комплемента, способствуют фокусированию нейтрофилов в очаге воспаления. Значительные скопления ПМЛ в сочетании с тромбоцитами способствуют не только повышению проницаемости стенок сосудов, но и их разрушению, что, чаще всего, имеет место при аллергических процессах в легких, бронхиальной астме, острых сливных пневмониях и респираторном дистресс-синдроме. Сравнительно недавно участие нейтрофилов в развитии воспалительного процесса при респираторных вирусных инфекциях практически отрицалось. Полагали, что это исключительная прерогатива бактерий. Тем не менее, в последние годы представлены убедительные данные о значительном вкладе нейтрофилов в процессы образования активных форм кислорода (АФК) при гриппе. Доказано, что одним из основных механизмов воспалительного процесса при гриппе является образование свободных радикалов кислорода. С генерированием этих форм связаны мутагенез, протеолитическая активация вируса гриппа, цитопатический эффект вирусной инфекции, деструкция капиллярной сети и стенок капилляров, развитие сливных пневмоний с отеком легких. Установлено также, что липидная пероксидация (ЛП), активируемая вирусом гриппа в клетках легкого, является одним из узловых метаболических процессов наряду с генерацией АФК. Именно эти процессы определяют тяжесть и распространенность воспалительной реакции. При резкой активации АФК и ЛП ферментная защита от них в виде супероксиддисмутазы (СОД), каталазы, глютатион-пероксидазы и аскорбиновой кислоты становится недостаточной. Преимущественная генерация при гриппе гипохлорида, который является мощным неспецифическим окислителем, способным окислять не только липиды, но и белки, безусловно, требует переоценки стратегии антиоксидантной терапии при гриппе, с подключением не только токоферола, ионола, но и более эффективной супероксиддисмутазы.
Несмотря на явное участие нейтрофилов в развитии воспаления при вирусных инфекциях, по мнению многочисленных авторов, основой фагоцитарной защитной реакции при вирусной инвазии являются моноциты и их зрелые формы – макрофаги. В чем сходство и отличие фагоцитоза, осуществляемого нейтрофилами и макрофагами? Сходство в наличии ряда аналогичных по функциональной направленности этапов при взаимодействии с чужеродными агентами: хемотаксис, активация, выброс активных веществ, адсорбция, захват, переваривание. Однако много принципиальных отличий. В противоположность нейтрофилам макрофаги – долгоживущие клетки и рассеяны по всему организму, они входят в состав соединительной ткани, содержатся в базальной мембране кровеносных сосудов. Соответствующую фокусировку макрофагов можно обнаружить как в ткани, так и в полостях и экссудатах. При хронической бронхолегочной патологии альвеолярные макрофаги нередко содержат вирусные антигены. Набор выделяемых активированным макрофагом веществ значительно больше и многообразнее, чем у ПМЛ. Соответственно этому спектр выбрасываемых активных веществ при вирусном воспалении значительно шире. К числу секретируемых им веществ следует отнести гидролазные ферменты (лизоцим, кислые гидролазы, нейтральные протеазы, липазы), ингибиторы протеолитических ферментов, факторы, меняющие клеточную пролиферацию и функцию (интерлейкин 1, фактор созревания тимоцитов, ангиогенный фактор, интерферон и фибронектин), производные липидов (простагландины, лейкотриены, фактор активации тромбоцитов), факторы, меняющие процесс свертывания крови (тромбопластин, активатор плазминогена), вирусоцидные агенты (супероксид – радикал О2, Н202, интерфероны), компоненты комплемента и их ингибиторы. Обилие секретируемых макрофагами веществ определяет и большую сложность и многообразие их функций. Активные МФ из очага воспаления участвуют во всех процессах по обеспечению гомеостаза, являясь главными его эффекторами. В отличие от нейтрофилов макрофаги способны фагоцитировать крупные, более 1 мкм объекты, именно они поглощают фрагменты клеток с содержащимися в них вирусами. В силу многообразия секретируемых веществ и выполняемых функций макрофаг активно вступает в контакт с другими клетками, осуществляющими более высокий уровень клеточной защиты организма. Именно макрофаг представляет Т-хелперам вирусный антиген, который находится на поверхности МФ в комплексе с клеточными маркерами главного комплекса гистосовместимости. Макрофаги запускают и регулируют деятельность всех видов лимфоцитов (В, Т с хелперной и супрессорной активностью). Под влиянием активированных МФ Т-лимфоциты продуцируют разнообразные растворимые факторы – лимфокины, которые, в свою очередь, оказывают активирующее воздействие на макрофаги. Макрофаги в значительно большей степени участвуют в развитии наиболее сложных и актуальных в настоящее время хронических форм воспаления. Причин для возникновения хронического воспаления при активации макрофагов значительно больше в силу их более длительного жизненного цикла, полифункциональности и значительной связи с элементами, контролирующими клеточный иммунитет, который при вирусных инфекциях, в отличие от бактериальных, имеет доминирующее значение. Функциональная недостаточность МФ, в том числе альвеолярных, нередко возникает именно под влиянием респираторных вирусов, встраивающихся в мембрану макрофага, повреждающих их рецепторный аппарат и внутренние структуры. Известно также, что для вирусов характерен незавершенный механизм фагоцитоза, при котором сами фагоциты способствуют диссеминации вирусного агента на значительные расстояния от первичного очага воспаления. – Также рекомендуем “Фагоцитоз при вирусной инфекции. Хроническое вирусное воспаление.” Оглавление темы “Воспаление в легких.”: |
Источник
Клетки, функции которых активируются при воспалении, подразделяют на две группы по месту их пребывания на момент воздействия повреждающего агента: первая — дендритные клетки, макрофаги и тучные клетки, которые содержатся в тканях постоянно (клетки-резиденты), вторая — другие клетки, поступающие в зону воспаления извне (клетки-эмигранты). К ним относятся гранулоциты (ней-трофильные, эозинофильные), моноциты и лимфоциты.
Дендритные клетки вместе с моноцитами-макрофагами относятся к антиген-представляющим, или антигенпрезентирующим, клеткам (АПК), которые способны представлять Т-хелперам на своей цитоплазматической мембране инородные процессированные антигены вместе с молекулами ГКГС II класса. Благодаря наличию разветвленных отростков они образуют важную систему защиты в поверхностных структурах организма (кожа и слизистые оболочки) и органах (лимфатические узлы, селезенка, легкие), расположенных на путях наиболее возможного проникновения флогогенов. Кроме того, активированные АПК продуцируют специфические сигналы — “угрозы”. К этой группе относятся провоспалительные цитокины, такие как ИЛ-1, ИЛ-6, ФНО-α, ФНО-β и γ-ИФ, различные хемокины и др. Роль ИЛ-1 особенно важна. Под его влиянием Т-лимфоцитыхелперы 1-го типа в момент презентации антигена начинают продуцировать ИЛ-2, который активирует пролиферацию и дифференциацию Т-лимфоцитов-киллеров, а также функцию моноцитов-макрофагов и натуральных киллеров.
Макрофаги. “Классически активированные” в начале воспалительного процесса инфекционными факторами и Т-хелиерами 1-го типа макрофаги синтезируют ИЛ-1. Он находит свои мишени — клетки мышечной, костной, нервной тканей, синовиоциты, гепатоциты, лимфоциты. На мембранах этих клеток имеются специфические рецепторы для ИЛ-1. Действие ИЛ-1 стимулирующее и универсальное, т. е. проявляется при любой болезни воспалительной этиологии (инфекционной или неинфекционной), причем на ранних ее этапах. Есть основания считать, что ранние симптомы болезни (головная боль, боль в мышцах и суставах, сонливость, лихорадка, лейкоцитоз, повышение уровня белков, в том числе и иммуноглобулинов) объясняются именно действием ИЛ-1 (рис. 31).

Роль указанных макрофагов не ограничивается продукцией ИЛ-1. Они также синтезируют более 100 биологически активных провоспалительных цитокинов, фосфолипаз, протеиназ, лизосомальных гидролаз, факторов комплемента, эйкозаноидов, активных кислородных радикалов, в том числе NO, и др. Основная функция этих макрофагов — фагоцитоз собственных клеток, инфицированных бактериями, вирусами, простейшими, грибами, и погибших клеток, в том числе нейтрофилов.
“Альтернативно активированные” Т-хелперами 2-го типа макрофаги синтезируют противовоспалительные цитокины, ингибиторы протеиназ, антифосфолипазы, антиоксиданты, ингибиторы комплемента, биогенных аминов, кининов, фибринолиза, факторы роста и компоненты внеклеточного матрикса. Такое изменение функции моноцитов-макрофагов происходит лишь после обезвреживания флогогенного фактора, его переваривания и преобразования антигена в растворимую форму.
Тучные клетки (тканевые базофилы, мастоциты, лаброциты) после повреждения выбрасывают гистамин, гепарин и лейкотриен D4, факторы хемотаксиса нейтрофилов (ФХН) и эозинофилов (ФХЭ), фактор активации тромбоцитов (ФАТ), которые содержатся в их гранулах. Гистамин и гепарин прежде всего действуют на сосуды (гиперемия). Лейкотриен D4 является хемоаттрактантом, а также вызывает спазм неисчерченных мышц бронхиол и кишечника.
Нейтрофильные гранулоциты. Основная функция этих клеток — фагоцитоз грамотрицательных бактерий и некоторых грибов (гноеродная микрофлора). Попав в кровь из костного мозга, они под влиянием хемоаттрактантов мигрируют из сосудов и в большом количестве скапливаются в очаге воспаления. Размножение клеток, миграция, участие в фагоцитозе регулируются БАВ, для которых на поверхностной мембране нейтрофилов существуют специфические рецепторы.
В цитоплазме нейтрофильных гранулоцитов есть два типа гранул: первичные азурофильные (больших размеров) — обычные лизосомы, в состав которых входят кислые гидролазы, лизоцим, миелопероксидаза. Вторичные (специфические) гранулы более мелкие, а главное — они содержат другой набор веществ (ферментативных и неферментативных), щелочную фосфатазу, лизоцим и неферментативные (катионные) белки. Гликопротеид лактоферрин является хелатором железа (связывает 2 моль железа на 1 моль белка), отбирая у бактерий важное для их жизнедеятельности железо. Вместе с тем, снижение благодаря лактоферрину концентрации Fe2+тормозит образование гидроксильного радикала в реакции Фентона, что уменьшает повреждение собственных тканей. Мощнейшим бактерицидным фактором нейтрофилов служат активные кислородные радикалы, особенно гипохлорит, образующийся под влиянием миелопероксидазы.
Эозинофильные гранулоциты. Их роль в воспалении определяется способностью адсорбировать и разрушать свободный гистамин с помощью гидролитического энзима гистаминазы и обезвреживать лейкотриены арилсульфатазой-В. Антихимотрипсин-α1 ингибирует сериновые протеиназы. Важную роль играют эозинофильные цитотоксические белки (основной белок белок эозинофилов), которые способны повреждать гельминты и их личинки и нейтрализовать гепарин. Миграция и активация эозинофильных гранулоцитов происходят под действием фрагментов (С5а) и компонентов (С5, С6, C7) комплемента, пептидов тучных клеток, лейкотриенов и веществ, вырабатываемых гельминтами.
Тромбоциты. Роль тромбоцитов в процессе воспаления заключается большей частью в том, что они принимают непосредственное участие в процессах микроциркуляции. Очевидно, это наиболее постоянные и универсальные клетки воспаления. В них содержатся вещества, влияющие на проницаемость сосудистой стенки, ее тонус и адгезивные свойства, на рост и размножение клеток, а главное — на способность крови свертываться.
Лимфоциты принимают участие в любом воспалении, особенно иммунной этиологии. Иммунный ответ, как и эффекторная фаза иммунных реакций, регулируется растворимыми медиаторами (интерлейкинами). Основными продуцентами интерлейкинов являются T-лимфоциты, моноциты и тканевые макрофаги.
Фибробласты пролиферируют и активируются в последней стадии воспаления, накапливаясь в очаге воспаления, где они синтезируют коллаген, эластин и гликозаминогликаны. Обобщенные данные о клетках воспаления приведены в табл. 11.


Медиаторы воспаления — это БАВ, являющиеся центральным звеном патогенеза воспаления, поскольку оказывают непосредственное регуляторное влияние на воспалительный процесс, как правило, в пределах очага воспаления (табл. 12). Различают гуморальные и клеточные медиаторы воспаления.
Медиаторы, на момент повреждения находящиеся в плазме крови, называются гуморальными медиаторами. Они представляют собой систему протеиназ плазмы крови, которые синтезируются преимущественно в макрофагах и гепатоцитах и попадают в кровь в неактивном состоянии. Клеточные медиаторы либо синтезируются заново в процессе воспаления уже в активном состоянии (эйкозаноиды и АКР), либо депонируются в гранулах и везикулах клеток и при воспалении активируются и секретируются (биогенные амины, лизосомальные ферменты, катионные белки). Основной причиной образования и/или высвобождения медиаторов клеточного происхождения является альтерация. Именно в результате повреждения клеток выделяются и активируются лизосомальные ферменты, которые в свою очередь активируют другие ферменты, в том числе и пропротеиназы плазмы крови. При этом протеолитические ферменты расщепляют белки не до конца (ограниченный протеолиз), вследствие чего образуются протеиназы и другие специфические активные вещества, дающие определенный патофизиологический эффект Одни из них действуют преимущественно на сосуды, усиливая проницаемость их стенки, другие — на миграцию лейкоцитов, а некоторые — на размножение клеток.
Первым, кто увидел в воспалении определенный “порядок”, закономерность, был В. Менкин. В воспалительном экссудате он выявил химические вещества и установил их влияние на некоторые характерные для воспаления реакции: гиперемию, экссудацию, лейкоцитоз, хемотаксис. С той поры в фактическом материале многое изменилось, однако это направление (химия воспаления) успешно развивается.
Клеточные медиаторы воспаления представлены биогенными аминами, лизосомальными ферментами, неферментативными катионными белками, эозинофильными цитотоксическими белками, активными кислородными радикалами (см. выше), эйкозаноидами, фактором активации тромбоцитов, цитокинами.
Биогенные амины главным образом депонируются в гранулах тучных клеток (гистамин) и тромбоцитах (серотонин, адреналин и норадреналин). Дегрануляция и выброс этих медиаторов происходит под влиянием флогогенных факторов, цитокинов, лизосомальных ферментов, катионных белков, АКР, а также комплексов антигенов с IgE и IgG4, фиксированных на Fc-рецепторах тучных клеток в процессе анафилактической реакции. Адреналин и норадреналин вызывают быстрый и кратковременный спазм сосудов, а гистамин — расширение артериол, повышение проницаемости сосудов микроциркуляторного русла с развитием отека, спазм гладкомышечных клеток, раздражение болевых рецепторов. Серотонин в очаге воспаления действует на мелкие сосуды подобно гистамину, но спазмирует более крупные.
Лизосомальные ферменты нейтрофилов и макрофагов вместе с АКР, катионными белками и мембранатакующим комплексом комплемента являются основным средством защиты от микроорганизмов, убивая и переваривая их в фаголизосомах. В то же время эластаза, коллагеназа и другие нейтральные протеиназы обусловливают разрушение базальных мембран и других матриксных белков, усиливая вторичную альтерацию и повышая проницаемость сосудистой стенки.
Катионные белки адсорбируются на негативно заряженной мембране бактерий и других клеток благодаря своему положительному заряду. Встраивание этих неферментативных белков в мембрану клеток вызывает образование нерегулируемых ионных каналов, через которые в клетки проникают кальций, натрий и вода, что ведет к их набуханию, активации протеиназ и фосфолипаз, разрушению и гибели клеток.
Эозинофильные цитотоксические белки фиксируются преимущественно на наружной оболочке гельминтов, опсонизированной IgE, что приводит к ее повреждению. Это делает эозинофилы главным средством борьбы с гельминтами и одновременно фактором воспаления при гельминтозе.
Эйкозаноиды, как и АКР, образуются заново в процессе воспалительной реакции из ПНЖК, входящих в состав клеточных мембран. Преобладание в рационе, а следовательно, и в клеточных мембранах ω-6-ПНЖК (арахидоновой и линолевой) обусловливает избыточное образование при повреждении тканей сильных провоспалительных факторов — лейкотриена B4 и тромбоксана A2, а также проста-гландинов ПГЕ2, ПГF2α. В то же время достаточное количество в рационе ω-3-ПНЖК способствует образованию ПГI3, оказывающего выраженное противовоспалительное действие, лейкотриена B5 и тромбоксана A3 — слабых провоспалительных факторов.
Фактор активации тромбоцитов является 1-алкил-2-ацетилглицерил-3-фосфорилхолином, образующимся из ацетил-лизофосфатидилхолина мембран нейтрофилов, моноцитов, эндотелиоцитов, тучных клеток и тромбоцитов под влиянием эндотоксина бактерий, тромбина, ангиотензина II, гистамина, брадикинина, ИЛ-1, ФНО-α. ФАТ в свою очередь стимулирует синтез цитокинов, кининов, NO. Он акгивирует фосфолипазу С, что приводит к образованию диацилглицерола, который посредством дегрануляции тромбоцитов стимулирует их адгезию и агрегацию, активирует гранулоциты, способствует продукции АКР и повреждению клеточных мембран, что усиливает приток в цитоплазму Са2+. Диацилглицерол и Ca2+ активируют фосфолипазу A2, в результате чего из фосфолипидов мембран высвобождается арахидоновая кислота с образованием провоспалительных эйкозаноидов. При этом тромбоксан A2 суживает и тромбирует сосуды, в том числе и венечные, лейкотриен B4 вызывает бронхоспазм и эмиграцию нейтрофилов, а ПГI2 может обусловить вазодилатацию. ФАТ в 100—10 000 раз сильнее, чем гистамин, повышает проницаемость сосудов микроциркуляторного русла и является самым мощным активатором тромбоцитов и нейтрофилов.
Цитокины — низкомолекулярные белки или гликопептиды, секретируемые клетками крови, стромы и иммунной системы. Они оказывают паракринное и аутокринное регулирующее воздействие на рост, развитие и функцию клеток-мишеней посредством специфических рецепторов, экспрессию которых клетки в определенной степени могут контролировать. Важнейшими цитокинами являются факторы некроза опухолей, интерлейкины, хемокины, интерфероны и факторы роста.
ФИО-α (кахексия) продуцируется различными типами клеток, в том числе моноцитами-макрофагами, лимфоцитами, опухолевыми клетками и адипоцитами. В низких концентрациях он стимулирует синтез и экспрессию молекул клеточной адгезии на эндотелиоцитах, что обеспечивает адгезию к ним нейтрофилов. ФНО-α повышает фагоцитарную активность нейтрофилов и макрофагов, усиливает синтез лимфокинов хелперными T-лимфоцитами и стимулирует пролиферацию В-лимфоцитов. В высоких концентрациях ФНО-α вызывает внутри-сосудистый тромбоз и некроз опухолевой ткани, усиливает продукцию ИЛ-1, ИЛ-6, простагландинов, что может привести к развитию шока, блокирует тирозинкиназную активность инсулиновых рецепторов мышечных и печеночных клеток, обусловливая их инсулинорезистентность.
ФИО-β (лимфотоксин) вырабатывается акгивированными T-лимфоцитами. Главная его функция — индукция апоптоза клеток-мишеней.
Интерлейкины, хемокины и интерфероны рассматриваются далее при изложении эмиграции лейкоцитов и фагоцитоза, а значение факторов роста анализируется при рассмотрении процессов пролиферации и репарации.
Гуморальные медиаторы воспаления представлены в основном кининами и системой комплемента.
Кинины — группа вазоактивных полипептидов, образующихся в результате каскада биохимических реакций, которые начинаются с активации сериновой протеиназы — фактора Xaгeмана (XII фактор свертывающей системы крови). Столкновение с поврежденной поверхностью или изменение внутренней среды (температуры, pH) приводит к тому, что этот фактор становится активным и действует на прекалликреин, являющийся неактивной протеиназой, которая содержится в плазме крови, превращая его в активный фермент калликреин. Последний в свою очередь действует на α2-глобулины (кининоген), отщепляя от них полипептидную цепь, состоящую из 9 (брадикинин) или 10 (каллидин) аминокислотных остатков. Кинины плазмы крови оказывают непосредственное влияние на тонус и проницаемость сосудистой стенки, обусловливая расширение артериол и повышая проницаемость стенки капилляров. Кроме того, они вызывают типичные для воспаления зуд и боль. Медиаторы калликреин-кининовой системы при воспалении влияют на реологические свойства крови, ее способность к свертыванию и фибринолизу. На схеме 9 показано, как активированный фактор Хагемана инициирует процессы кининобразования, гемокоагуляции и фибринолиза. Выпадение нитей фибрина и образование тромбов в очаге воспаления определенным образом связаны с состоянием калликреин-кининовой системы.

Еще один важный медиатор воспаления гуморального происхождения — комплемент, представляющий собой каскадную систему протеиназ. Известно, что комплемент является защитным фактором организма, однако вместе с тем он может вызывать повреждение собственных тканей, наблюдающееся при воспалении, особенно иммунном. Это объясняется тем, что фрагменты комплемента С3а и С5а активируют выброс медиаторов из тучных клеток и образование лейкоцитами АКР, которые повреждают как микроорганизмы, так и собственные клетки. Фрагмент С5b способен фиксироваться на сенсибилизированных и несенсибили-зированных антителами клетках, образовывать мембранатакующий комплекс С5b6789, который разрушает мембраны и осуществляет лизис поврежденных клеток. Фрагмент С5а усиливает хемотаксис нейтрофилов и повышает проницаемость сосудистой стенки. Наконец, микроорганизмы, мембрана которых покрыта (опсонизирована) фрагментом комплемента С3b, экспрессируют на фагоцитах рецептор комплемента 1-го типа (CRl) и становятся объектом активного фагоцитоза. Опсонизации бактерий фрагментом С3b способствует предыдущее связывание фосфатидилхолина их мембран с белком острой фазы — С-реактивным протеином.
Медиаторы воспаления осуществляют свое влияние преимущественно местно, т. е. в очаге воспаления: оно описывается при характеристике течения воспалительного процес?