Механизм воспаления соединительной ткани
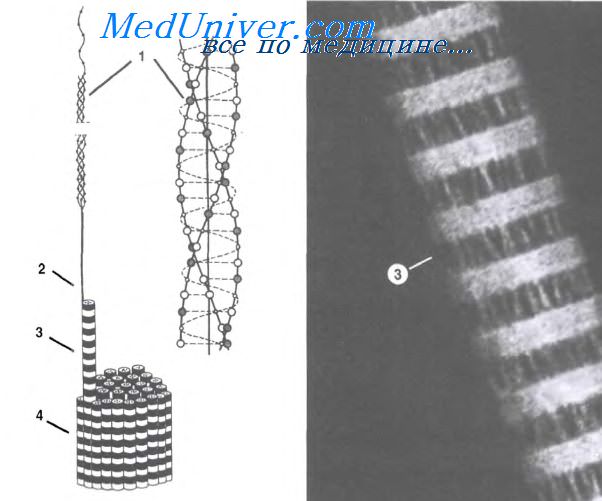
Воспаление в соединительной ткани. Процессы воспаления в соединительной ткани.
Рыхлая соединительная ткань — это система многих клеточных дифферонов, или гистогенетических рядов — дивергентных линий клеточной дифференцировки. Несмотря на большое разнообразие клеточных форм, все они составляют единую систему, выполняющую защитную и трофическую функции. Между кровью и соединительной тканью существуют тесные взаимосвязи и постоянный обмен клеточными элементами.
Структурно-функциональной единицей соединительной ткани считается гистион. Он включает участок микроциркуляторного русла с окружающими его клетками и межклеточными структурами. Рыхлая соединительная ткань находится в динамических взаимодействиях с другими тканями, в частности, с эпителиальными, ретикулярной, эндотелиальной, жировой, пигментной, плотными волокнистыми соединительными тканями.
Воспаление и регенерация. При действии повреждающих агентов (механических, химических, бактериальных и других) в рыхлой соединительной ткани развивается сложная сосудисто-тканевая защитно-приспособительная реакция — воспаление. При воспалении наблюдаются как общие, так и местные изменения. Местные проявления реакции организма в очаге воспаления включают несколько взаимосвязанных фаз: 1) альтерация (повреждение) тканей; 2) высвобождение физиологически активных веществ — так называемых медиаторов воспаления; 3) сосудистая реакция с экссудацией, включающая изменение кровотока в микроциркуляторном русле, повышение проницаемости сосудов; 4) резорбция продуктов распада тканей; 5) пролиферация клеток с образованием “грануляционной ткани” и последующей регенерацией тканей. Завершается воспаление образованием зрелой волокнистой соединительной ткани.

При описании воспаления обычно выделяют три фазы: лейкоцитарную, с преобладанием в очаге воспаления нейтрофильных гранулоцитов; макрофагическую, когда продукты распада активно резорбируются макрофагами; фибробластическую, на протяжении которой на месте повреждения разрастается соединительная ткань.
Лейкоцитарная фаза воспаления характеризуется передвижением нейтрофильных гранулоцитов в очаг распада ткани на месте ее повреждения. Пусковым механизмом воспаления является выброс медиаторов и цитокинов (гистамина, серотонина, лизосомных гидролаз и других биологически активных веществ). Источником выделения медиаторов являются тканевые базофилы (тучные клетки), лейкоциты, кровяные пластинки, макрофаги и лимфоциты. При этом развивается комплекс сосудистых изменений, включающий повышение проницаемости микроциркуляторного русла, экссудацию жидких составных частей плазмы, эмиграцию клеток крови. Уже через 6 ч от начала воспаления образуется лейкоцитарный инфильтрат. Нейтрофильные гранулоциты проявляют высокую фагоцитарную активность, поглощая главным образом микроорганизмы (отсюда их название — микрофаги). Часть нейтрофилов при этом распадается, выделяя большое количество лизосомных гидролаз. Это способствует очищению очага воспаления от поврежденных тканей.
Макрофагическая фаза воспаления протекает при явлениях активизации макрофагов как гематогенных (возникающих из моноцитов крови), так и гистиогенных (оседлых макрофагов — гистиоцитов). Макрофаги энергично фагоцитируют продукты тканевого распада. Вместе с тем они вырабатывают вещества — стимуляторы восстановительных процессов в очаге воспаления.
Фибробластическая фаза является завершающей фазой воспаления. Она характеризуется пролиферацией (размножением) клеток фибробластического ряда и их передвижением к воспалительному очагу. Поскольку к этому времени заканчивается в основном очищение места повреждения от продуктов тканевого распада, фибробласты заполняют бывший дефект ткани. Они интенсивно вырабатывают межклеточное вещество. При этом образуются вначале тонкие аргирофильные, а позднее и коллагеновые волокна. Вместе с клетками эти волокна отграничивают воспалительный очаг от неповрежденной ткани. Развитие фибробластов постепенно приводит к замещению воспалительного очага соединительной тканью. При значительном дефекте ткани на месте очага воспаления формируется рубец. При наличии инородного тела вокруг него образуется соединительнотканная капсула, отчетливо выраженная на 5-7-е сутки от начала воспаления. Относительно источников развития фибробластов в очаге повреждения существуют разные гипотезы. Так различают две субпопуляции фибробластов, имеющие разные источники и отличающиеся неодинаковой продолжительностью жизни (коротко- и долгоживущие фибробласты).
Фибробласты, которые развиваются из стволовых кроветворных клеток — это короткоживущая популяция фибробластов защитно-трофического типа, участвующая в процессах воспаления, заживления ран и т. д. Другие фибробласты происходят от стволовых стромальных клеток (механоцитов) костного мозга. Это популяция долгоживущих фибробластов опорного типа с преимущественно механическими функциями. Кроме того, существуют специализированные формы фибробластов — фиброкласты и миофибробласты, развивающиеся из адвентициальных клеток. Фиб-рокласты обеспечивают перестройку соединительной ткани путем разрушения межклеточного вещества. В цитоплазме клеток обнаруживается хорошо развитый аппарат лизиса коллагеновых фибрилл. Клетки выявляются преимущественно в области формирования рубцовой ткани после повреждения органов. Миофибробласты отличаются от фибробластов большим содержанием сократительных филаментов (актина гладкомышечного типа). Они также участвуют в регенерации путем контракции краев раны.
– Также рекомендуем “Ткани с опорно-механической функцией. Плотные волокнистые соединительные ткани.”
Оглавление темы “Костные ткани. Мышечные ткани.”:
1. Воспаление в соединительной ткани. Процессы воспаления в соединительной ткани.
2. Ткани с опорно-механической функцией. Плотные волокнистые соединительные ткани.
3. Костные ткани. Остеогистогенез.
4. Развитие костной ткани на месте хряща. Остеокласты. Пластинчатая костная ткань.
5. Ткани с двигательной функцией. Скелетная мышечная ткань. Гистогенез скелетной мышечной ткани.
6. Строение скелетной мышечной ткани. Регенерация скелетной мышечной ткани.
7. Сердечная мышечная ткань. Строение сердечной мышечной ткани.
8. Гладкая мышечная ткань. Строение гладкой мышечной ткани.
9. Мионевральная ткань. Миоидные клетки.
10. Ткани нервной системы. Гистогенез нервной системы.
Источник
Иммунообусловленный системный воспалительный процесс составляет общий и главный стержень, на основе которого объединяются диффузные болезни соединительной ткани. Несмотря на очевидное клиническое и патогенетическое своеобразие каждой из этих болезней, существуют общие законы развития иммунных нарушений и воспаления, которые имеют важнейшее значение для понимания механизмов возникновения, динамики и терапии рассматриваемых заболеваний.
Этим общим закономерностям посвящена настоящая глава. Нам представлялось методологически более удобным проанализировать вначале основные черты воспалительного процесса (клинически наиболее очевидного, ответственного за непосредственные проявления болезни и поэтому более близкого врачу-лечебнику), а затем — структуру и функцию иммунной системы, которой принадлежит серьезная (хотя и гораздо менее очевидная) роль в патогенезе воспалительных ревматических заболеваний.
Воспалительный процесс
Воспаление лежит в основе главных клинических проявлений диффузных болезней соединительной ткани и служит важнейшим объектом антиревматической терапии. Несмотря на многообразие причин, вызывающих воспалительный процесс (в том числе и при различных ревматических заболеваниях), всякое воспаление, будучи биологически целесообразной и филогенетически закрепленной реакцией, характеризуется рядом общих проявлений.
Оно сопровождается также мобилизацией некоторых биологических систем, обеспечивающих защитноприспособительные реакции организма, но в то же время вызывающих и активно поддерживающих воспалительный процесс (последний в принципе также является защитно-приспособительной реакцией в общебиологическом смысле, хотя с точки зрения индивидуально-клинической может рассматриваться как процесс патологический). Наиболее крупным достижением в исследовании воспаления в целом является, расшифровка многих биохимических процессов, определяющих его возникновение и динамику. Установлен ряд эндогенных химических веществ, которые ответственны за проявление конкретных биологических реакций, составляющих в своей совокупности общую клинико–морфологическую картину воспалительного процесса независимо от его причины.
Среди подобных химических медиаторов воспаления, обеспечивающих местное расширение сосудов (вслед за первоначальным кратковременным спазмом) в первые минуты после тканевого повреждения особое значение имеют гистамин и серотонин, выделяющиеся из разрушающихся в очаге воспаления тучных клеток, идентичных им базофилов крови и из тромбоцитов. Несколько позже вазодилатация становится еще более стойкой и выраженной вследствие увеличения синтеза простагландинов и лейкотриенов. Длительное время считалось, что неврогенные влияния на тонус и просвет сосудов в зоне воспаления осуществляются только по принципу аксон-рефлекса.
Сравнительно недавно установлено, что в нервных окончаниях под влиянием различных раздражителей способны вырабатываться, провоспалительные субстанции (в частности, вещество Р), поддерживающие воспалительный процесс. Возможно, что именно продукция медиаторов воспаления нервными окончаниями объясняет симметричность суставных поражений, столь свойственную ряду ревматических заболеваний и прежде всего ревматоидному артриту, а также менее выраженные воспалительные изменения суставов на стороне сопутствующей гемиплегии.
Воспаление не может рассматриваться как некоторое стабильное состояние ткани или целого организма; условно также понятие «воспалительный процесс». Оно всегда представляет собой очень сложную и во многом нерасшифрованную совокупность взаимозависимых местных и общих процессов, которые для большей демонстративности целесообразно рассмотреть раздельно.
Местные проявления воспалительного процесса
Первое непосредственное повреждающее действие на ткань вызывает очень кратковременное сокращение гладкомышечных волокон в стенке артериол и вследствие этого сужение последних. Однако вскоре эта реакция под влиянием химических и неврогенных факторов сменяется стойкой вазодилатацией, которая сохраняется в течение всей активной фазы воспаления.
Вазодилатация лишь в начальный период вызывает усиление капиллярной циркуляции. Буквально через несколько минут замедляется местный кровоток, а в ряде капилляров возникает стаз, сопровождающийся скоплениями эритроцитов в виде «монетных столбиков» и развитием истинных микротромбозов. Замедлению микроциркуляции способствуют также повышенная вязкость крови из-за экссудации плазмы из сосудов и нарастание экстраваскулярного давления, вызванного этим процессом. В отличие от нормального ламинарного кровотока, при котором форменные элементы занимают центральную часть потока, а плазма — периферическую, в зоне воспаления возникает турбулентное течение, при котором клетки и плазма перемешиваются.
В связи с этим возможность контакта клеток с эндотелием значительно увеличивается. Лейкоциты как бы «катятся» по внутренней поверхности эндотелия и часто «прилипают» к нему, что особенно характерно для кровотока в венулах воспаленной ткани. В норме подобных феноменов не наблюдается. Усиленный выход плазмы из кровеносных сосудов и вызванное этим повышение внутритканевого давления приводят к резкому нарастанию оттока лимфы из очагов воспаления.
При этом по лимфатическим сосудам в регионарные лимфатические узлы поступают частицы распадающихся клеток и другие корпускулярные остатки тканевого распада. В результате в лимфатических узлах возникает реактивная гиперплазия их клеточных элементов с образованием новых зародышевых центров и повышенной макрофагальной реакцией.
Образование экссудата, типичное для начального периода воспаления, определяется несколькими механизмами. Прежде всего расширение артериол приводит к их повышенному кровенаполнению и нарастанию гидростатического давления. Это вызывает увеличенный выход через эндотелий артериол, капилляров и венул воды, электролитов и (в меньшей степени) белка в ткани.
По-видимому, не меньшее значение имеет образование между эндотелиальными клетками промежутков шириной около 1 мкм, через которые не могут выйти клетки, но легко проходят белки плазмы, повышающие в околососудистых пространствах онкотическое давление и тем самым препятствующие возвращению воды в кровяное русло. Указанные межклеточные промежутки возникают благодаря активному сокращению микрофибриллярной системы в клетках эндотелия. Вследствие такого сокращения клетки округляются и как бы «оттягиваются» друг от друга, образуя промежутки между собой. Этот механизм свойствен преимущественно венулам, эндотелий которых наиболее богат микрофибриллами и особенно чувствителен к влиянию химических медиаторов, вызывающих сокращение микрофибрилл.
Неотъемлемой чертой воспалительного процесса является клеточная реакция в очаге воспаления. При наиболее простом — легком травматическом — воспалении через 30 мин после повреждения в очаг начинают поступать нейтрофилы. Их количество достигает максимума через 4—6 ч, а в течение следующих 2 сут эти клетки постепенно исчезают. Макрофаги появляются в экссудате позднее — через 6 ч; максимальная концентрация наблюдается через 36 ч, практическое исчезновение — через 3—5 сут.
Естественно, что при воспалительных процессах у больных ревматическими заболеваниями клеточные реакции более сложны и длительны; однако в общем виде отмеченная закономерность сохраняется — преобладание нейтрофилов на первом этапе воспаления или его обострения, а макрофагов — на последующих этапах и особенно — при хроническом воспалении. Клетки поступают из крови в воспаленную ткань путем активных амебоидных движений через сосудистую стенку под влиянием хемотаксических влияний различных веществ, возникающих в очагах воспаления (продукты распада тканей и т. д.). Своеобразно, что выход клеток происходит не через рассмотренные выше межэндотелиальные промежутки, возникшие в процессе, а через нормальные соединения между клетками эндотелия.
Клеточный инфильтрат в зоне воспаления оказывает существенное влияние на развитие воспалительного процесса в целом. При распаде этих клеток и в процессе их жизнедеятельности выделяются химические и физические медиаторы воспаления (лизосомные ферменты, серотонин, простагландины, кислородные радикалы и др.). Моноциты способны пролиферировать непосредственно в воспалительном очаге, увеличивая тем самым количество активных макрофагов. Лимфоидные клетки могут участвовать в местных иммунных реакциях (в частности, осуществлять преимущественно локальный синтез антител), поддерживающих воспаление. Более подробно роль клеток в воспалительном процессе рассматривается ниже.
По мере развития воспаления при его достаточной выраженности может происходить более или менее заметное вовлечение в процесс устойчивых биологических адаптивных систем организма, сущность функционирования которых заключается, в частности, в генерировании или поддержании воспалительных реакций. К ним относятся главным образом 3 системы: система медиаторов тучных клеток, кининобразующая система и система комплемента. Все эти системы имеют определенное значение (хотя и неодинаковое) в развитии ревматических заболеваний. В то же время их компоненты оказываются объектом воздействия антивоспалительных препаратов. Выяснение конкретных путей такого воздействия позволяет уточнить ряд важных механизмов патогенеза болезней и противовоспалительной терапии.
Сигидин Я.А.
Опубликовал Константин Моканов
Источник
Соединительная ткань встречается в организме буквально на каждом шагу. Кости, хрящи, сухожилия и связки — это всё соединительная ткань. Она образует каркас, «арматуру» для внутренних органов, защищает их, участвует в их питании, «склеивает», как цемент, разные виды тканей между собой.
Соединительная ткань есть в суставах, мышцах, глазах, сердце, коже, легких, почках, органах пищеварительной и мочеполовой системы, в стенке кровеносных сосудов.
На данный момент ученым известно более 200 заболеваний, при которых страдает соединительная ткань. А так как она разбросана по всему организму, то и симптомы обычно возникают не в каком-то одном органе, а сразу в нескольких — то есть, выражаясь врачебным языком, носят системный характер. Именно поэтому заболевания соединительной ткани называют системными. Иногда используют более научный синоним — «диффузные». Иногда говорят просто — «коллагенозы».
Что общего между всеми системными заболеваниями соединительной ткани?
Все болезни из этой группы обладают некоторыми общими чертами:
- Они возникают в результате нарушения работы иммунитета. Иммунные клетки перестают различать «своих» и «чужих», и начинают атаковать собственную соединительную ткань организма.
- Эти заболевания протекают хронически. Вслед за очередным обострением наступает период улучшения состояния, а после него — снова обострение.
- Обострение возникает в результате действия некоторых общих факторов. Чаще всего его провоцируют инфекции, пребывание под солнечными лучами или в солярии, введение вакцин.
- Страдают многие органы. Чаще всего: кожа, сердце, легкие, суставы, почки, плевра и брюшина (две последние — это тонкие пленки из соединительной ткани, которые покрывают внутренние органы и выстилают изнутри, соответственно, грудную и брюшную полость).
- Улучшить состояние помогают лекарства, которые подавляют иммунную систему. Например, глюкокортикостероиды (препараты гормонов коры надпочечников),цитостатики.
Несмотря на общие признаки, каждое из более чем 200 заболеваний имеет собственные симптомы. Правда, установить правильный диагноз иногда бывает очень сложно. Диагностикой и лечением занимается врач-ревматолог.
Некоторые представители
Типичный представитель группы системных заболеваний соединительной ткани — ревматизм. После инфекции, вызванной особой разновидностью бактерий-стрептококков, иммунная система начинает атаковать собственную соединительную ткань. Это может приводить к воспалению в стенках сердца с последующим формированием пороков сердечных клапанов, в суставах, нервной системе, коже и других органах.
«Визитная карточка» другого заболевания из этой группы — системной красной волчанки — характерная сыпь на коже лица в виде «бабочки». Также может развиваться воспаление в суставах, коже, внутренних органах.
Дерматомиозит и полимиозит — заболевания, которые, соответственно, сопровождаются воспалительными процессами в коже и мышцах. Их возможные симптомы: мышечная слабость, повышенная утомляемость, нарушение дыхания и глотания, лихорадка, снижение веса.
При ревматоидном артрите иммунная система атакует суставы (преимущественно мелкие — кистей и стоп),со временем они деформируются, в них нарушается подвижность, вплоть до полной утраты движений.
Системная склеродермия — заболевание, при котором уплотняется соединительная ткань, входящая в состав кожи и внутренних органов, нарушается кровообращение в мелких сосудах.
При синдроме Шегрена иммунная система атакует железы, в основном слюнные и слезные. Больных беспокоит сухость глаз и во рту, повышенная утомляемость, боли в суставах. Болезнь может привести к проблемам с почками, легкими, пищеварительной и нервной системой, сосудами, повышает риск лимфомы.
Системные васкулиты — группа, включающая около 20-ти заболеваний, при которых развивается воспаление в стенках сосудов, в итоге нарушается работа внутренних органов. Наиболее распространенные васкулиты: узелковый периартериит, неспецифический аортоартериит, гранулематоз Вегенера, геморрагический васкулит.
Проявления системных заболеваний соединительной ткани бывают очень разными, и даже опытный врач-терапевт не всегда может правильно заподозрить заболевание. В медицинском центре «Медицина 24/7» вы можете получить консультацию ревматолога, пройти все необходимые исследования, сдать анализы. При любых симптомах, которые беспокоят достаточно долго, нужно посетить врача. Вовремя установленный диагноз и эффективное лечение помогут избежать возможных осложнений и свести к минимуму риски. Звоните: +7 (495) 230-00-01
Источник
