Особенности обмена веществ в очаге воспаления
На начальном этапе воспаления в ткани
(не только зоны первичной, но и вторичной
альтерации) преобладают реакции
катаболизма, затем — при развитии
артериальной гиперемии и активации
процессов пролиферации, как правило,
начинают доминировать анаболические
реакции.
Углеводный обмен: в очаге воспаления
метаболизм углеводов претерпевает
характерные изменения, выражающиеся в
преобладании гликолиза и развитии
ацидоза.
Проявления
увеличение поглощения тканью кислорода
при одновременном снижении эффективности
окисления глюкозы в процессе тканевого
дыхания;активация гликогенолиза и гликолиза;
уменьшение уровня АТФ в ткани;
накопление избытка лактата и пирувата.
Липидный обмен: обмен липидов в
очаге воспаления характеризуется
доминированием липолиза над реакциями
их синтеза.
Проявления
активация процессов липолиза и накопление
продуктов липолизаторможение реакций синтеза липидов
активация перекисного окисления липидов
и накопление перекисей и гидроперекисей
липидов
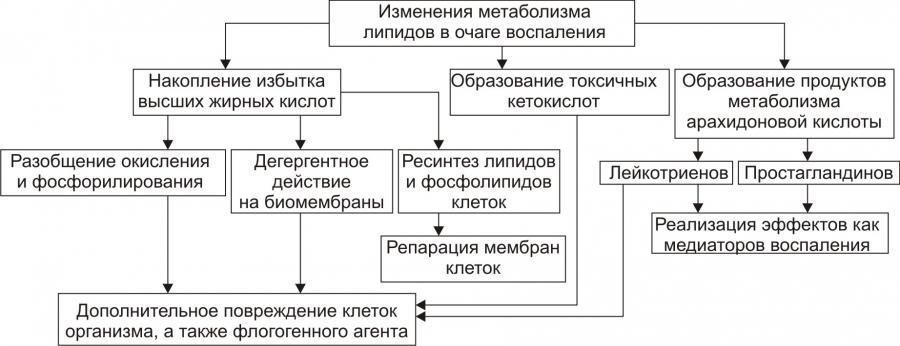
Рис. 7. — Изменения
метаболизма липидов в очаге воспаления
(по П.Ф. Литвицкому,
2002)
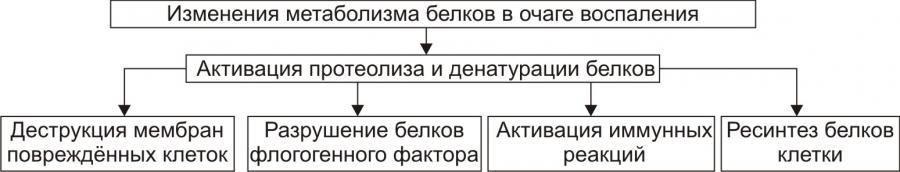
Белковый обменхарактеризуется
преобладанием протеолиза над процессами
протеосинтеза.
Проявления
активация процессов протеолиза и
накопление продуктов протеолиза.торможение реакций протеосинтеза.
денатурация молекул белка (образование
аутоантигенов).

Рис. 8. — Изменения
метаболизма белков в очаге воспаления
(по П.Ф. Литвицкому,
2002)
Обмен ионов и воды
Для ионов и воды характерен трансмембранный
дисбаланс ионов, увеличение внутриклеточного
содержания Na+иCa2+и внеклеточного содержанияK+и Mg2+, гипергидратация клеток и
отёк ткани в очаге воспаления.
Проявления
нарушения распределения ионов по обе
стороны плазмолеммы; происходит потеря
клеткой K+,Mg2+,
микроэлементов и накопление их в
межклеточной жидкости. В клетку же
поступаютNa+,Ca2+и некоторые другие ионы.нарушения соотношения между отдельными
ионами как в клетке, так и вне клетки в
результате расстройства механизмов
трансмембранного переноса ионов.гипергидратация ткани в очаге воспаления
в связи с высокой гидрофильностью
накапливающихся в нём Na+иCa2+, а также
продуктов гидролиза органических
соединений.высвобождение дополнительного количества
катионов (K+,Na+,Ca2+, железа, цинка)
при гидролизе солей, распаде гликогена,
белков и др. органических соединений,
а также клеточных мембран.выход большого количества Ca2+из повреждённых внутриклеточных депо
(митохондрий и цистерн эндоплазматической
сети и митохондрий).
Медиаторы воспаления
В ходе первичной и вторичной альтерации
высвобождаются большие количества
разнообразных медиаторов и модуляторов
воспаления.
Медиаторы воспаления — БАВ, образующиеся
при воспалении, обеспечивающие
закономерный характер его развития и
исходов, формирование местных и общих
признаков. По происхождению делятся на
гуморальные (образующиеся в жидких
средах — плазме крови и тканевой
жидкости) иклеточные. Всегуморальные
медиаторы являются предсуществующими,
т.е. имеются в виде предшественников
до активации последних (производные
комплемента, кинины и факторы свертывающей
системы крови).Среди клеточных
медиаторов выделяют предсуществующие
(депонированные в клетках в неактивном
состоянии) — вазоактивные амины,
лизосомальные ферменты, нейропептиды,
ивновь образующиеся (т.е. продуцируемые
клетками при стимуляции) — эйкозаноиды,
цитокины, лимфокины, активные метаболиты
кислорода (таб. 2–4).
Таблица 2. Клеточные предшествующие
медиаторы воспаления
Основные | Основные | Основные | Основные |
Вазоактивные | Гистамин | Базофилы Тучные клетки Тромбоциты | Вазодилятация Повышение Спазм |
Серотонин | Тромбоциты | Зуд Угнетение Стимуляция | |
Лизосомальные | Протеиназы | Гранулоциты | Тканевая Усиление эмиграции Пролиферация |
Неферментные | Гранулоциты | Микробицидность Повышение Дегрануляция Адгезия | |
Нейропептиды | Вещество | С-волокна | Вазодилятация Повышение Дегрануляция Спазм |
Нейромедиаторы | Ацетилхолин | Холинергические | Вазодилятация Спазм гладкой Стимуляция |
Таблица 3. Клеточные, вновь образующиеся,
медиаторы воспаления
Основные | Основные | Основные | Основные эффекты |
Производные (эйкозаноиды) | Простагландины | Моноциты-макрофаги | Активация Вазодилятация Боль |
Тромбоксаны | Моноциты | Агрегация Спазм гладкой Активация | |
Лейкотриены Гидроокси- и Липоксины | Моноциты-макрофаги | Активация Повышение Вазодилятация Спазм | |
Фосфолипиды | Фактор, | Гранулоциты | Спазм гладкой Повышение Активация Агрегация |
Монокины | Интерлейкин-1 Фактор | Моноциты-макрофаги | Активация Пролиферация и Усиление фагоцитоз Стимуляция Стимуляция |
Лимфокины | Фактор, | Т-лимфоциты | Активация и Активация |
Активные | Супероксид-анион Гипохлорид | Гранулоциты | Тканевая деструкция Активация Стимуляция Угнетение |
Другие | Окись | Моноциты-макрофаги | Тканевая деструкция Активация |
Таблица 4. Гуморальные медиаторы
воспаления
Основные | Основные | Основные | Основные эффекты |
Производные | С5b-С9 С5а des С5аС3а | Плазма Тканевая жидкость | Тканевая деструкция Активация Повышение Дегрануляция Спазм гладкой |
Кинины | Брадикинин Каллидин | Плазма Тканевая | Вазодилятация Повышение Спазм гладкой Угнетение Стимуляция Боль |
Факторы | Фибринопеп-тиды Продукты деградации | Плазма | Активация Усиление фагоцитоза |
Источник
В случае воспаления метаболизм тканей имеет как количественные, так и качественные особенности.
Количественные особенности обмена веществ при воспалении
Количественные особенности особенно заметны в начале воспаления – это усиление обмена веществ, которое Саде назвал «метаболическим огнем». В этот период сильно усиливаются процессы гидролиза (гликолиз, протеолиз, липолиз) и окислительные процессы (из-за артериальной гиперемии). В воспаленных тканях увеличивается утилизация кислорода.
По мере прогрессирования нарушений периферического кровообращения (венозная гиперемия, застой) интенсивность окислительных процессов снижается, и в воспалительных тканях начинают проявляться качественные изменения обмена веществ.особенности – процессы окисления не проходят полностью, не заканчиваются выделением СО2. Процессы гидролиза преобладают над процессами окисления.
Основные причины этих метаболических нарушений – повреждение митохондрий – цикл Кребса, биологическое окисление и связанные с ним нарушения окислительного фосфорилирования – и лизосомное повреждение (лизосомы выделяют около 40 гидролитических ферментов).
Схема цикла Кребса
Также вызывают метаболические нарушения остатки бактерий и ферменты. Например, многие бактерии продуцируют гиалуронидазу, которая деполимеризует гиалуроновую кислоту, разжижает соединительную ткань и увеличивает проницаемость сосудов. Коллагеназа приводит к разрушению волокон соединительной ткани. Стрептококковая дезоксирибонуклеаза и рибонуклеаза расщепляют нуклеиновые кислоты и активируют протеолитические ферменты.
Из-за венозной гиперемии, застоя и повреждения митохондрий в тканях остается мало кислорода. В отсутствие кислорода активность ферментов цикла Кребса снижается, и во время этого цикла (особенно в центре воспалительных очагов) образуется недостаточно CO2, но промежуточные продукты метаболизма (пировиноградная кислота, α-кетоглутаровая кислота, яблочная кислота, янтарная кислота) накапливаются из пировиноградной кислоты.
Если в присутствии монойодацетата ферменты гликолиза подавлены, воспаление слабое. Белковый обмен усиливают протеолитические процессы. Они активируются при повреждении лизосом и ядер нейтрофилов крови, макрофагов и воспаленных паренхиматозных клеток, а также дезоксирибонуклеазами и рибонуклеазами. Усиленный протеолиз приводит к пролиферации нуклеотидов, полипептидов и аминокислот.
В воспалительных условиях, когда в тканях не хватает кислорода, дезаминирование (нормальный путь окисления аминокислот) снижается, а декарбоксилирование усиливается. В этих условиях, а также в результате дегрануляции тучных клеток в тканях накапливается гистамин.
Для жирового обмена характерно усиление липолиза. В результате увеличивается количество жирных кислот и продуктов их переваривания. Поскольку интенсивность цикла Кребса уменьшается, молекулы ацетил-СоА начинают конденсироваться и взаимодействуют друг с другом с образованием ацетилуксусный-КоА, который, в свою очередь, дает кетон вещество уксусной кислоты (5-оксимасляной кислоты и ацетона).
Из – за высокого потребления O2 (особенно в артериальной гиперемии), но количество выделяемого СО2 намного меньше, тогда частота дыхания также уменьшается.
Описанные процессы диссимиляции (катаболизма) преобладают в остром периоде воспаления. В это время некоторые продукты патологически измененного обмена веществ (медиаторы воспаления) сами влияют на развитие процесса.
В более поздний период воспаления, когда тенденции к восстановлению тканей уже проявляются, на первый план выходят процессы синтеза, а именно анаболические – увеличивается синтез ДНК и РНК. Эти процессы особенно активны в гистиоцитах и фибробластах.
В этих клетках возрастает активность окислительно-восстановительных ферментов, активно происходит биологическое окисление и окислительное фосфорилирование. В результате увеличивается образование макроэргических соединений и обеспечивается повышенная функциональная активность гистиоцитов и фибробластов.
Биологически активные вещества
Биологически активные вещества играют очень важную роль в патогенезе воспаления, поэтому кратко опишем основные из них.
Гистамин образуется декарбоксилазой из гистидина. Много гистидина и гистамина находятся в коже, легких, симпатических нервных волокнах.
- Гистамин расщепляется метилтрансферазой. Этот фермент в изобилии присутствует в органах, на которые действует гистамин (легкие, кожа, желудочно-кишечный тракт).
- Второй путь расщепления гистамина – это окислительное дезаминирование гистамином (диаминоксидазой), которое обнаруживается в основном в кишечнике, печени и почках.
В клетках (лейкоцитах, тромбоцитах, тучных клетках и эндотелиальных клетках) гистамин присутствует в больших количествах в связанной форме. В тучных клетках всегда с гепарином.
Гистамин является биологически очень активным веществом. Понижает тонус прекапиллярных сфинктеров, расширяет сосуды в зоне микроциркуляции, сужает крупные сосуды. В то же время гистамин сокращает сократительные вещества эндотелиальных клеток и увеличивает поры между этими клетками. Таким образом, гистамин увеличивает проницаемость стенки кровеносных сосудов, и белковые жидкости могут выходить в интерстициальное пространство (IST). Больше всего увеличивается проницаемость стенки мелких вен. Гистамин также вызывает сокращение гладких мышц.
Серотонин (5-окситриптамин) образуется из триптофана специфической гидроксилазой. Серотонин расщепляется неспецифической моноаминоксидазой. Образуется индоксиуксусная кислота, которая способствует пролиферации клеток. Серотонин содержится в тучных клетках и тромбоцитах (из которых гистамин высвобождается в процессе свертывания крови).
Как и адреналин, серотонин повышает кровяное давление, но мало влияет на периферическое сопротивление. В отличие от адреналина серотонин вызывает бронхоспазм. В тканях серотонин выделяется алкалоидом резерпином. Серотонин также увеличивает проницаемость сосудов, но он делает отек в 200 раз более активным, чем гистамин.
Гранулы тучных клеток содержат гистамин, гепарин и серотонин. Гистамин и гепарин связаны с ферментом химазой. Кроме того, гепарин является ингибитором этого фермента и защищает гранулы от автолиза. Гистамин относительно слабо связан в этом комплексе и может высвобождаться так называемыми освободителями гистамина, веществами, которые более тесно связаны с гепарином, чем гистамином (натрий, кальций, водород и другие ионы). Следовательно, в условиях гипоксии и ацидоза количество гистамина увеличивается и его действие становится более выраженным.
Дегрануляция тучных клеток может быть вызвана воздействием тепла, ультрафиолетового и ионизирующего излучения, солевых растворов, кислот, катионных белков, синтетических полимеров и мономеров, поверхностно-активных веществ.
Дегрануляция тучных клеток
Дегрануляция всегда происходит за счет взаимодействия антигена и антител. Выброшенные гранулы фагоцитируются макрофагами или растворяются в межслитковой жидкости, а вазоактивные вещества переносятся лимфой или кровотоком в организм. Гистамин и серотонин расширяют кровеносные сосуды и увеличивают проницаемость их стенок, в то время как гепарин увеличивает проницаемость капилляров, препятствуя образованию фибрина.
Гипотензивные полипептиды – хинины
Хининовая система или так называемые гипотензивные полипептиды также называют местными (тканевыми) гормонами, потому что они не вырабатываются эндокринными железами и действуют в основном локально. Хинины обнаружены в крови, лимфе, моче, поджелудочной железе, слюнных железах, головном мозге, тонком кишечнике и т. д. Два хинина: калидин и брадикинин были изучены на людях.
Хинины в плазме крови и тканях образуются из неактивных α2-глобулинов (кининогенов) ферментом каликреином. Каликреины тканей (калидиногеназы) и каликреины плазмы (брадикининогеназы) происходят из прекалликреинов. Их переход в каликреины облегчается реакциями антиген-антитело, температурами выше 45 ° C, кислыми изменениями pH, лизосомальными ферментами, катепсинами, трипсином, фактором свертывания XII (фактор Хагемана), фибринолизином (плазмин).
Хининогены сначала образуют калидин. После расщепления аминопептидазы образуется брадикинин. Брадикинин – сильнейшее сосудорасширяющее средство, увеличивающее проницаемость капилляров в 10-15 раз сильнее, чем гистамин. Брадикинин стимулирует сокращение миокарда и, таким образом, увеличивает частоту сердечных сокращений, сердечный выброс и коронарное кровообращение, а также усиливает почечную клубочковую фильтрацию и выведение ионов натрия и калия.
Хинины расслабляют гладкие мышцы артериол и венозных стенок, тем самым расширяя эти кровеносные сосуды и снижая скорость их кровотока. В то же время они значительно увеличивают проницаемость стенки сосуда и способствуют эмиграции лейкоцитов из кровеносных сосудов.
Как и другие медиаторы, хинины вызывают воспаление, различные типы шока, аллергические реакции, артрит, инфаркт миокарда, инсульт, острый панкреатит и другие заболевания. Действуя на местном уровне,
Хинины вместе с системами тромбина и плазмина (фибринолизина) образуют так называемую систему факторов Хагемана, которая активируется при повреждении тканей. Свертывание крови и фибринолиз являются результатом системы факторов Хагемана.
Тромбоксан А2 и тромбоксан В2
Тромбоксан А2 и тромбоксан В2 – высоко биологически активные вещества. Тромбоксан А2 был выделен из тромбоцитов с очень короткой продолжительностью действия (период полураспада 32 с). Это вещество активно участвует в удалении медиаторов из тромбоцитов и других клеток, а также в агрегации тромбоцитов.
Система комплемента
Система комплемента состоит из 9 различных белков, обозначенных Ci, C2 и т. д. Она активируется комплексом антиген-антитело, а также эндотоксинами, и образуются продукты, которые активно участвуют в патогенезе воспаления. Наиболее активные компоненты системы комплемента – C3a (анафилатоксин I), C5a (анафилатоксин II) и C5,6, C3a – гемотаксический фактор, который увеличивает проницаемость сосудистой стенки и способствует дегрануляции тучных клеток. У Csa такое же и даже более сильное действие.
Также присутствуют в тканях ингибиторы C3a и Csa. Если дефицит этих ингибиторов передается по наследству или приобретается, активность системы комплемента может значительно возрасти, и воспалительный процесс может стать тяжелым. Было показано, что ингибиторы комплемента подавляют эмиграцию лейкоцитов.
Система комплемента также участвует в фагоцитозе и высвобождении лизосомальных ферментов и в конечном итоге вызывает иммунологический лизис клеток – смерть. Система комплемента вместе с ионами магния является частью системы пропердина, вызывающей микробный лизис в крови.
Таким образом, в случае воспаления активируются тесно связанные системы хинина, комплемента, свертывания крови, фибринолиза и другие.
Простагландины
Простагландины (PG) были обнаружены примерно в 1930 году в семенниках и сперме различных животных. Первоначально считалось, что эти биологически активные вещества происходят из простаты, поэтому их назвали простагландинами.
Теперь известно, что они являются высокоактивными фосфолипидами, образованными в клеточных мембранах из арахидоновой кислоты под действием простагландинсинтетазы. Ферменты циклооксигеназа и липоксигеназа зависят от образования PG или лейкотриенов из арахидоновой кислоты. PG присутствует во всех органах.
Простагландины
Различают несколько типов простагландинов (Ei, E2, F, I, D, A, G). У людей было обнаружено 13 простагландинов, наиболее активными из которых являются простагландины E, F и G. Действие PGE и PGF часто противоположно.
Простагландины контролируют диффузию веществ через клеточную мембрану (часть простагландина активирует аденилатциклазу и увеличивает количество цАМФ), а также регулируют активность гладких мышц и процессы секреции.
Простагландины действуют в основном локально, потому что ферментные системы мешают их общей функции. Общая эффективность наблюдается, если деградация PG ингибируется или накоплено слишком много PG. Простагландины обладают моделирующим действием – они стимулируют слабые и подавляют избыточные функции.
При воспалении особенно повышены уровни PGE2, PGE и PGI2. Эти простагландины сильно способствуют расширению сосудов, а также увеличивают проницаемость сосудистой стенки и лизосомальной мембраны, тем самым способствуя воспалению. Эти простагландины также стимулируют синтез ДНК и пролиферацию тканевых лимфоцитов. Лимфоток стимулируется в меньшей степени. С другой стороны, также наблюдалась защитная противоязвенная активность клеток простагландинов (PGE2).
Медиаторы воспаления
Помимо простагландинов, липоксигеназа арахидоновой кислоты также продуцирует лейкотриены, такие как медленно действующее вещество анафилаксии (медиатор аллергического воспаления). В случае аллергического воспаления из тканей выделяется вещество Р (проницаемость), которое увеличивает проницаемость стенки сосуда.
Медиаторы воспаления
Система адениловой кислоты содержит производные аденина (аденозин, AMF, ADF), и их количество в воспаленных тканях значительно увеличено. Эти вещества способствуют лейкоцитозу, эмиграции лейкоцитов и фагоцитозу, а также, среди прочего, увеличивают проницаемость сосудистой стенки.
Фермент клеточной мембраны аденилилциклаза катализирует переход АТФ в аденозин-3′-5 ‘- (циклический) монофосфат (цАМФ) и пирофосфат. Обычно клетки и биологические жидкости содержат очень мало cAMF. Он участвует в гуморальной регуляции – это промежуточный член между гуморальным рецептором клетки и внутриклеточными процессами.
В случае повреждения клетки увеличивается активность аденилциклазы и снижается ресинтез АТФ, поэтому количество цАМФ в поврежденной клетке увеличивается и стимулируются процессы регенерации. Печень играет ключевую роль в эвакуации и гидролизе цАМФ из плазмы крови. При заболевании печени эти функции снижены.
АМФ подавляет дегрануляцию лизосом и высвобождение лизосомальных медиаторов, тем самым подавляя дальнейшее развитие воспаления. Адреналин и норадреналин оказывают ингибирующее действие на воспаление через цАМФ.
К эндогенным медиаторам воспаления также относятся лизосомальные компоненты (катионные белки, кислотные и нейтральные протеазы) и продукты активности лимфоцитов – фактор, препятствующий миграции лейкоцитов, гемотаксический фактор, митогенный фактор и т. д. Большинство лизосомальных медиаторов высвобождаются из нейтрофилов и макрофагов.
В зависимости от места их образования, воспалительные посредники делятся на две группы:
- медиаторы, образующиеся в клетках;
- «плавающие» медиаторы, образованные в жидкостях организма, главным образом, в крови.
В первую группу входят вазоактивные амины (гистамин, серотонин), лизосомальные ферменты, катионные белки и др. Гистамин и серотонин присутствуют в клеточных гранулах, поэтому в случае повреждения клеток (тучных клеток, базофилов, тромбоцитов) они появляются первыми (в течение нескольких минут) в месте воспаления.
Однако запас вазоактивных аминов быстро истощается, поскольку эти вещества расщепляются, и вазоактивные амины исчезают из очага воспаления. Поэтому вазоактивные амины называют медиаторами короткого действия. Позже, когда активируется система калихреин-хинин, образуются калидин и брадикинин, а еще позже – простагландины. Они являются медиаторами пролонгированного действия и требуют образования ферментных систем.
Ко второй группе («плавающих») медиаторов относятся фактор Хагемана, система комплемента и тромбоксана, фибринопептиды и др.
Помимо медиаторов воспаления, вызывающих воспалительные реакции, различают и модуляторы воспаления (повреждения). Они не вызывают напрямую воспалительных реакций, но способны усиливать или уменьшать их. Такие эффекты проявляются, например, в системах простагландинов, тромбоксана и адениловой кислоты.
Продолжение статьи
- Часть 1. Этиология и патогенез воспаления. Классификация.
- Часть 2. Особенности обмена веществ при воспалении.
- Часть 3. Физико – химические изменения. Роль нервной и эндокринной систем в развитии воспаления.
- Часть 4. Изменения в периферическом кровообращении при воспалении.
- Часть 5. Экссудация. Экссудат и транссудат.
- Часть 6. Эмиграция лейкоцитов. Хемотаксис.
- Часть 7. Фагоцитоз. Асептическое и острое воспаление.
- Часть 8. Распространение. Последствия. Принципы лечения воспаления.
Поделиться ссылкой:
Источник
