Прокаин в очагах воспаления

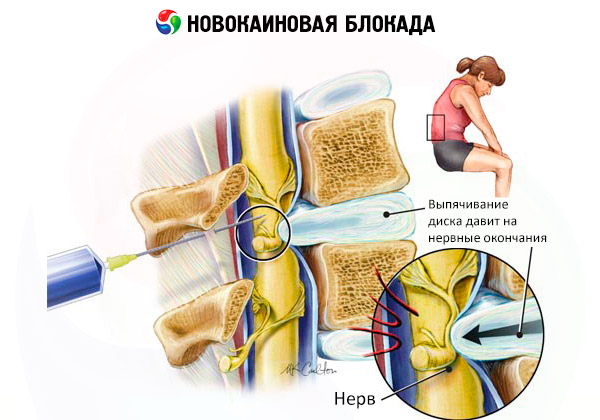
Новокаиновая блокада. Механизм действия новокаиновой блокадыА.В.Вишневский, сводя сущность влияния новокаиновой блокады к замене сильного раздражителя нервной системы слабым, утверждал, что сильные раздражения способствуют ухудшению трофической иннервации и приводят к явлениям нейро-дистрофии и преобладанию разрушительного компонента воспаления над регенеративно-восстановительным, что проявляется в виде гиперергической воспалительной реакции, ухудшающей течение болезни. Замена сильного раздражения нервной системы слабым приводит к нормализации трофической иннервации, уменьшению или полному снижению нейродистрофии. В результате этого в очаге воспаления начинает преобладать регенеративно-восстановительный компонент над разрушительным, и болезнь приобретает благоприятное течение. Это положение А. В. Вишневского остается незыблемым. Накопленные научные и клинические данные лишь уточняют и дополняют его. Необходимо, однако, учитывать, что терапевтический эффект новокаиновой блокады определяется исходным состоянием соматической и вегетативной нервной системы, т. е. зависит от степени их перераздражения (фазы парабиоза). А. В. Вишневский подчеркивал, что при очень тяжелых патологических процессах, сопровождающихся чрезмерно сильным раздражением нервной системы, новокаиновая блокада как добавочное раздражение нервов может дать на периферии отрицательный эффект вплоть до некроза тканей.
Учитывая, что парасимпатикус и симпатикус находятся между собой в реципрокных отношениях, следует иметь в виду, что новокаиновая блокада каждого из них дает физиологически не одинаковый эффект, точно так же, как и новокаиновая блокада рефлексогенных зон, где оба отдела образуют нервные сплетения, например солнечное, и др. В данном случае эффект новокаиновой блокады может быть различным в зависимости от функционального преобладания парасимпатикуса или симпатикуса. Поэтому более четкий и дифференцированный эффект можно ожидать от новокаиновой блокады каждого из упомянутых отделов вегетативной нервной системы. Установлено, что новокаиновая блокада отдельных звеньев симпатического отдела вегетативной нервной системы приводит к более выраженному улучшению трофики тканей и усилению регенеративных процессов. Под влиянием новокаиновой блокады соматических и тем более вегетативных проводящих путей и ганглиев понижается или полностью снимается перераздражение нервных центров, возникшее под влиянием сильных или монотонных, длительно действующих раздражителей, идущих с периферии или внутренних органов. Этот эффект новокаиновой блокады обусловлен прежде всего прекращением потока сильных раздражений в подкорковые центры и кору головного мозга и длительным воздействием новокаина на периферические нервные окончания зоны блокады, а также длительным контактом его с различными отделами центральной нервной системы. Е. Н. Воротынцева установила на кроликах с помощью меченого новокаина по С , что после парентеральной новокаиновой блокады или внутривенного введения новокаина он обнаруживается во всех тканях организма, и в том числе в промежуточном мозге через 4 ч после введения. Максимальное содержание его в спинном мозге и особенно в коре головного мозга установлено через 48 ч, затем количество его постепенно снижается. При этом больше всего он задерживается в коре головного мозга — до 72 ч. Изложенное дает основание считать, что длительное воздействие новокаина на нервные центры и, в частности, кору головного мозга способствует снижению или ликвидации очагов ее возбуждения. На этом фоне улучшаются циркуляция крови, внутриклеточный и общий обмены, уменьшается проницаемость капилляров, особенно в зоне патологического очага; активируются фагоцитоз и другие иммунологические реакции; снижаются явления нейродистрофии, нарастают регенеративно-восстановительные процессы; нормализуется функция внутренних органов и улучшается общее состояние. – Вернуться в оглавление раздела “Биология” Оглавление темы “Шок в ветеринарии. Лечение травм”: |
Источник
Имейте в виду, что новокаиновая блокада в домашних условиях не проводится: это стерильная процедура, которая обычно выполняется в амбулаторных условиях квалифицированным специалистом – хирургом-травматологом, ортопедом, неврологом с дополнительной квалификацией в области анестезиологии (а не любой манипуляционной медсестрой, делающей обычные уколы).
Техника проведения новокаиновой блокады по любой методике отработана на уровне пошаговых действий – на основе хирургической анатомии и топографии периферической иннервации человеческого тела и зон нервных сплетений: продвижение иглы постоянного контролируется и корректируется по анатомическим ориентирам. И только врач, владеющий этими методиками и имеющий достаточный опыт, допускается к выполнению таких манипуляций.
Так что по описания, которые приводят многие интернет-ресурсы медицинской тематики, не помогут пациенту освоить технику проведения новокаиновой блокады…
Подготовка к процедуре заключается в предварительном (за сутки-двое до проведения блокады) определении чувствительности пациента к новокаину – путем введения небольшой дозы под кожу.
В набор для новокаиновой блокады входят: раствор новокаина (0,25-0,5%), стерильные шприцы (на 20 мл), специальные длинные и короткие иглы. В соответствии с видом манипуляции игла может быть разного размера (18-26G) – с менее острым концом или измененной формой его среза.
Учитывая то, что блокада проводится при болевом синдроме, вид внушительного размера игл у пациентов вызывает логичный вопрос: больно ли делать новокаиновую блокаду? При низком болевом пороге любая манипуляция кажется очень болезненной, но анальгезирующая блокада, действительно может сопровождаться временным усиление болевого синдрома. Хотя для снижения болезненности процедуры перед введением новокаина длинной иглой в кожу на места инъекции тонкой иглой вкалывается небольшая доза менее концентрированного новокаинового раствора – до образования зоны нечувствительности к боли.
Основные виды новокаиновых блокад
До сих пор виды новокаиновых блокад не имеют строгой классификации на основе единых принципов, поэтому отмечается синонимичность определений – в зависимости от места очага боли и топографии анатомической области введения новокаина. Кроме того, наличие целого ряда авторских методик, которые нашли отражение в названиях, также приводит к терминологическому дублированию.
Новокаин может вводиться интрадермально (внутрикожно), подкожно, внутримышечно и внутрикостно. Периневральное введение новокаина (в область периневральной фиброзной оболочки нервного ствола) или параневральное (в окружающие нерв ткани) – это, по сути, новокаиновая блокада нерва или проводниковая новокаиновая блокада, суть которой заключается в прекращении проведения нервных импульсов. А если проводятся новокаиновые блокады суставов, то инъекции делаются либо периартикулярно (около сустава), либо интрапериартикулярно (внутрь сустава и в окружающие его ткани).
Также существует футлярная периваскулярная или футлярная новокаиновая блокада по Вишневскому, которая проводится путем введения анестезирующего раствора в соединительнотканные оболочки (футляры) мышц. Делается она при переломе бедра и других трубчатых костей, а также пациентам с трофическими язвами нижних конечностей. Практически в тех же случаях используется блокада поперечного сечения или циркулярная новокаиновая блокада – когда создание анальгезирующего блока достигается несколькими внутрикожными инъекциями в одной плоскости по окружности конечности.
Эту манипуляцию также разделяют на виды по месту введения и подпадающим под действие новокаина анатомическим областям. Так, околопозвоночная – паравертебральная новокаиновая блокада – отличается введением анестетика в мышцы рядом с позвоночником, то есть вблизи паравертебральных ганглиев симпатического нервного ствола позвоночника. В некоторых медицинских источниках выделяется корешковая (фуникулярная) новокаиновая блокада позвоночника. Но в любом случае показаниями к ее применению являются боли в позвоночнике, когда назначается новокаиновая блокада при грыже или протрузии межпозвоночных дисков, новокаиновая блокада при радикулите, травмах позвоночного столба, поясничном остеохондрозе и т.п.
Введение новокаина в жировые ткани около почки – паранефральная новокаиновая блокада по Вишневскому (с добавлением в раствор глюкозы) или поясничная новокаиновая блокада (по Роману) – оказывает действие на все пространство за брюшиной и способствует купированию интенсивных спастических болей у пациентов с почечной коликой, острым воспалением желчного пузыря или поджелудочной железы, непроходимостью кишечника.
Если анестезирующий раствор вводится в область передне-боковой поверхности шеи (ближе к позвоночнику), то есть туда, где находится шейный отдел вагосимпатического ствола (а рядом проходят блуждающий нерв и сонная артерия), значит, проводится вагосимпатическая новокаиновая блокада – шейная вагосимпатическая блокада или шейная. При этом происходит блокирование блуждающего нерва и звездчатого ганглия в области шеи. Применяется она при шейном остеохондрозе, заднем шейном симпатическом синдроме, а также повреждениях, локализованных в области грудной клетки.
Болевой синдром при острых формах холецистита и панкреатита может снять предбрюшинная новокаиновая блокада или иначе – новокаиновая блокада круглой связки печени, продольно проходящей по левой борозде в нижней части поверхности печени (влево от пупка) и содержащей нервные волокна.
В травматологии при любых переломах тазовых костей, вызывающих нестерпимые боли, обязательной процедурой является одно или двусторонняя внутритазовая новокаиновая блокада по Школьникову-Селиванову – с введением обезболивающего (с передней стороны туловища) глубоко (до 12 см) в область подвздошной кости, вблизи переднего верхнего костного выступа. Поскольку в зоне действие новокаина находится и мочеточник, данный вид новокаиновой блокады можно применять при почечной колике, связанной с нефролитиазом.
Пресакральная новокаиновая блокада проводится в область plexus sacralis – крестцового нервного сплетения или через крестцово-копчиковую связку в нижней части крестца (в промежность между крестцом и анусом); она оказывает действие на бедренно-половой нерв и копчиковое сплетение. Проктологи могут прибегать к такому методу снятия острой и хронической анальной боли, при ущемлении геморроидальных узлов, проктите. Данная блокада облегчает состояние пациентов при загибе матки, патологиях маточно-крестцовых связок, язвенном колите, после хирургических вмешательств на промежности, области анального отверстия и гениталиях.
При интенсивных болях из-за ишиаса – воспаления седалищного нерва, тянущегося от поясницы до ступни, или в случаях его защемления назначается новокаиновая блокада седалищного нерва (часто с кортикостероидами): параневрально в область седалищного нерва тремя возможными доступами – задним, боковым или передним.
Неврологи отмечают, что ишиалгию может провоцировать сдавливание седалищного нерва воспаленной грушевидной мышцей (расположенной под ягодичной и обеспечивающей подвижность крестцово-подвздошного сочленения). Кроме того, боли в области ягодиц с отдачей в пах бедро и даже голень – явные признаки туннельного болевого синдрома грушевидной мышцы, часто возникающего при пояснично-крестцовом радикулите со сдавливанием спинномозговых корешков. В таких случаях и назначается новокаиновая блокада грушевидной мышцы – в область седалищного нерва или путем паравертебральной блокады в поясничной области (как при радикулите).
Обязательна новокаиновая блокада в паховую область (в зону паховой связки) при повреждениях мошонки, тестикул и их канальцев, которые могут приводить к болевому шоку, а также в случае перекрута яичка.
Новокаиновая блокада семенного канатика, который находится в паховом канале у мужчин и по которому проходят нервные волокна – то же, что и новокаиновая блокада по Лорину-Эпштейну. Подобная манипуляция проводится только мужчинам – при остром воспалении придатка семенника (эпидидимите) или семенного канатика (фуникулите), а также острой форме орхита (воспаления яичек).
Ретробульбарная новокаиновая блокада с введением препарата в находящий в глазнице слой ткани проводится офтальмологами при неврите глазного нерва, кератите, травмах роговицы.
А в отоларингологии изредка – при тяжело протекающем вазомоторном рините или синусите – могут применяться новокаиновые блокады в нос (точнее в стенку носовых раковин) с добавление кортикостероидов, быстро снимающих отечность носовых проходов и околоносовых пазух.
Кроме того, в абдоминальной хирургии применяется новокаиновая блокада корня брыжейки тонкой кишки в ходе лапаротомического вмешательства при острой кишечной непроходимости. И ревизию брюшной полости во время операций по поводу повреждения ее органов также предваряют инъекции новокаина в корни брыжеек тонкой, поперечно-ободочной и сигмовидной кишок.
Новокаиновая блокада в ветеринарии
Благодаря эффективности данная анальгезирующее-терапевтическая манипуляция нашла применение и в лечении животных, для чего в ветеринарии были модифицированы имеющиеся или разработаны собственные методики.
Например, надплевральная новокаиновая блокада по Мосину применяется для обезболивания органов, расположенных в брюшной полости и области таза, а по методике Шакурова – при плеврите и пневмонии.
Коровам и козам при воспалении или абсцессе вымени производится новокаиновая блокада по Логвинову, таким же методом делается и процедура собаке при мастите.
Новокаиновая блокада по Фатееву блокирует тазовые нервные сплетения у коров, и делается это как в случае острого мастита, так и при проблемах с маткой во время и после отела. А при воспалениях и травмах роговицы глаза ветеринары проводят используемую у людей ретробульбарную блокаду.
Источник

Анестетики разделяют на:
- Местные
- Общие:
а) ингаляционные – летучие жидкости и газы
б) неингаляционные (внутривенные)
Таблица 1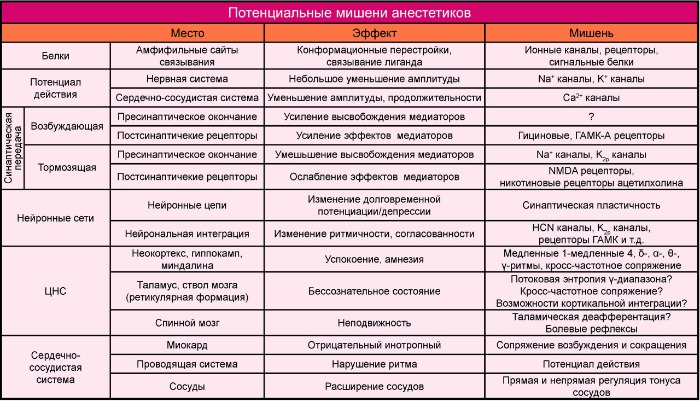
1. Местные анестетики
Местные анестетики обратимо снижают возбудимость чувствительных нервных окончаний и блокируют проведение афферентных импульсов в нервных стволах в зоне непосредственного применения, используются для устранения боли.
Первый препарат этой группы — кокаин, был выделен в 1860 г. Альбертом Ньюманом из листьев южноамериканского кустарника Erythroxylon coca. Ньюман, как многие химики прошлого, попробовал новое вещество на вкус и отметил онемение языка. Профессор Военно-медицинской академии Санкт-Петербурга Василий Константинович Анреп в 1879г. подтвердил способность кокаина вызывать анестезию. В экспериментах на лягушках он обнаружил, что кокаин влияет «парализующим образом» на окончания чувствительных нервов. В. К. Анреп исследовал действие кокаина на себе: инъекция кокаина в дозе 1 — 5 мг под кожу сопровождалась полной анестезией — укол булавкой, прижигание тлеющей спичкой не вызывали боли. Аналогичный эффект наблюдался при закапывании раствора кокаина в глаз и нанесении его на слизистую оболочку языка.
Местные анестетики классифицируют на сложные эфиры (анестезин, дикаин, новокаин) и замещенные амиды (лидокаин, тримекаин, бупивакаин). Местные анестетики — сложные эфиры подвергаются гидролизу псевдохолинэстеразой крови и действуют в течение 30 — 60 мин. Их эффект пролонгируют антихолинэстеразные средства (прозерин). Продукт гидролиза — n-амино-бензойная кислота ослабляет бактериостатическое влияние сульфаниламидов. Замещенные амиды кислот инактивируются монооксигеназной системой печени в течение 2 — 3 ч. Бупивакин вызывает местную анестезию продолжительностью 3 — 6 ч, после ее прекращения длительно сохраняется анальгетический эффект.
С точки зрения практического применения анестетики подразделяют на следующие группы:
- Средства, применяемые для поверхностной (терминальной) анестезии: Кокаин, Дикаин, Анестезин, Пиромекаин
- Средства, применяемые преимущественно для инфильтрационной и проводниковой анестезии: Новокаин, Бупивакаин
- Средства, применяемые для всех видов анестезии: Лидокаин, Тримекаин
Механизм действия
Местные анестетики представляют собой третичные азотистые основания. Они состоят из гидрофильной и липофильной частей, соединенных эфирной или амидной связями. Механизм действия определяет липофильная часть, имеющая ароматическую структуру. Для нанесения на слизистые оболочки и кожу и парентерального введения применяют водные растворы хлористоводородных солей местных анестетиков. В слабощелочной среде тканей (рН=7,4) соли гидролизуются с освобождением оснований. Основания местных анестетиков растворяются в липидах мембран нервных окончаний и стволов, проникают к внутренней поверхности мембраны, где превращаются в ионизированную катионную форму.
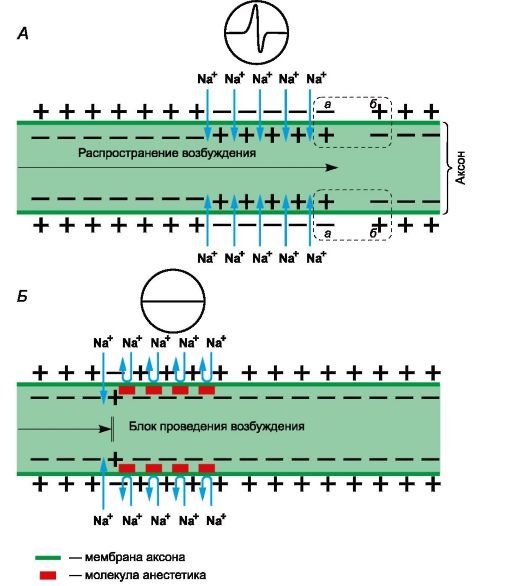 Рисунок 1 | Механизм действия местных анестетиков
Рисунок 1 | Механизм действия местных анестетиков
Рецепторы для местных анестетиков локализованы в S6-сегменте IV домена внутриклеточной части натриевых каналов. Связываясь с рецепторами, катионы местных анестетиков пролонгируют инактивированное состояние натриевых каналов, что задерживает развитие следующего потенциала действия. Местные анестетики не взаимодействуют с закрытыми каналами в период потенциала покоя. Таким образом, в зоне нанесения местных анестетиков не развиваются потенциалы действия, что сопровождается блоком проведения нервных импульсов. Избирательное влияние местных анестетиков на чувствительные афферентные нервы обусловлено генерацией в них длительных (более 5 мс) потенциалов действия с высокой частотой.
В первую очередь местные анестетики блокируют безмиелиновые С и миелиновые Аδ и Аβ волокна (афферентные пути, проводящие болевые и температурные раздражения; вегетативные нервы). На волокна, окруженные миелиновой оболочкой, местные анестетики действуют в области перехватов Ранвье. Толстые миелиновые волокна (афферентные пути, проводящие тактильные раздражения; двигательные нервы) слабее реагируют на местные анестетики. Кроме того, устойчивость двигательных нервов к анестезии обусловлена низкочастотными короткими (менее 5 мс) потенциалами действия. В очаге воспаления в условиях ацидоза нарушаются диссоциация хлористоводородных солей местных анестетиков и образование их свободных липидорастворимых оснований, поэтому обезболивающее влияние утрачивается. Например, местная анестезия может оказаться неэффективной при удалении зуба в случае тяжелого периодонтита.
2. Общие анестетики
2.1. Ингаляционные анестетики
2.1.1 Летучие жидкости
Теории механизма действия общих анестетиков
Эффекты ингаляционных анестетиков не могут быть объяснены одним молекулярным механизмом. Скорее всего многокомпонентное действие каждого анестетика реализуется через множество мишеней. Тем не менее, эти эффекты сходятся на ограниченном числе изменений, лежащих в основе физиологических эффектов. На данный момент существуют липидная и белковая теории анестезии, но ни одна из них пока не описывает последовательность событий, происходящих от взаимодействия молекулы анестетика и ее мишеней до физиологических эффектов.
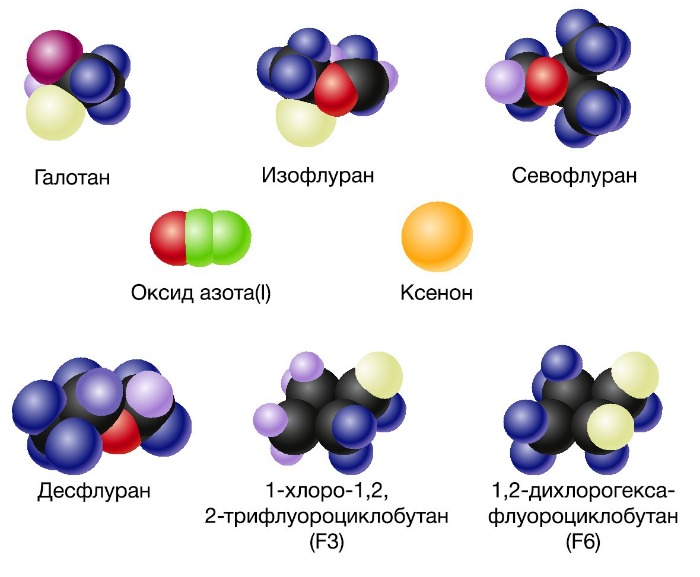 Рисунок 2 | Ингаляционные анестетики
Рисунок 2 | Ингаляционные анестетики
Активность ингаляционных анестетиков оценивают по минимальной альвеолярной концентрации (МАК). Доза, создающая 1 МАК, предотвращает у половины пациентов движения в ответ на хирургическое вмешательство. Сила общих анестетиков коррелирует с их растворимостью в жирах, что говорит о важности взаимодействия с гидрофильными мишенями. В частности, обнаружение связи между силой анестетика и его липофильностью (правило Мейер-Овертона) дало начало липидной теории механизма действия анестетиков. Липидная теория анестезии утверждает, что анестетики растворяются в двойном липидном слое биологических мембран и вызывают анестезию, достигая критической концентрации в мембране. Наиболее усложненные версии липидной теории требуют, чтобы молекулы анестетиков вызывали пертурбацию (изменение свойств) мембраны.
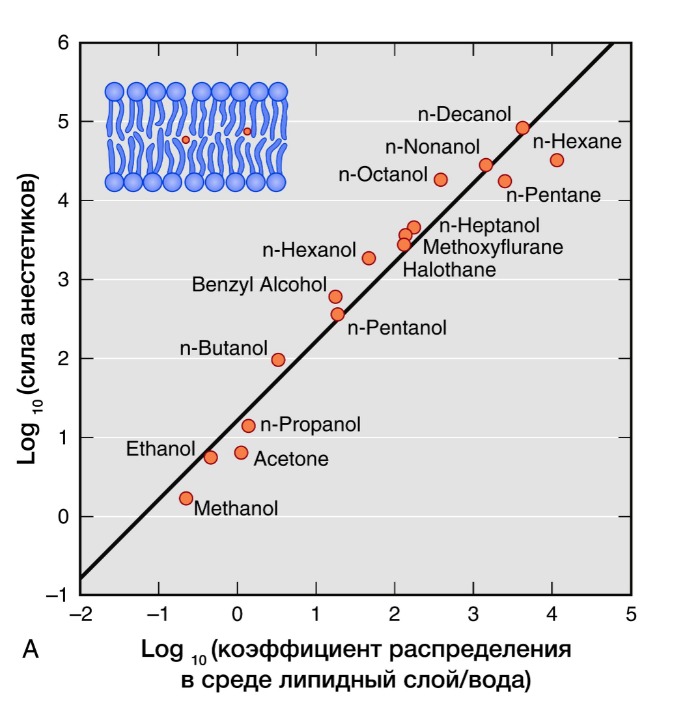 Рисунок 3 | Правило Мейер-Овертона
Рисунок 3 | Правило Мейер-Овертона
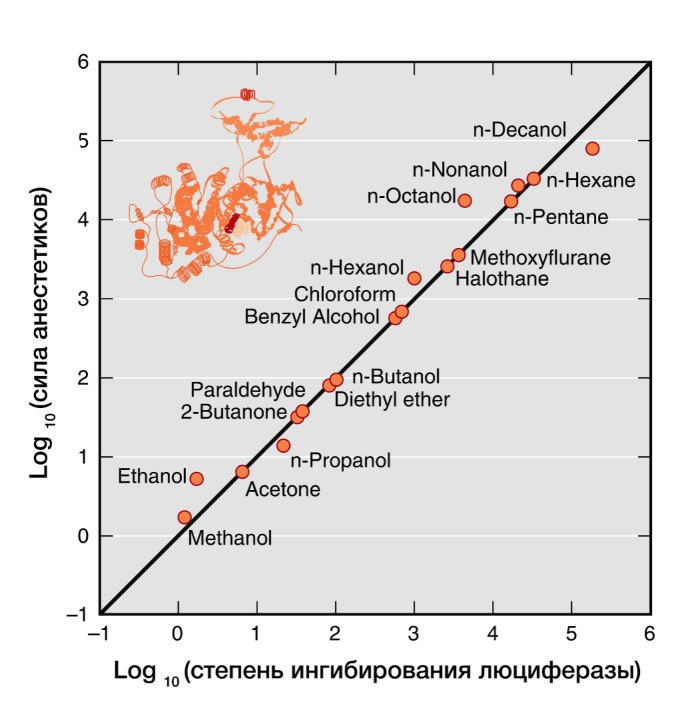 Рисунок 4 | В 20 веке было показано, что сила общих анестетиков коррелируют с их способностью ингибировать активность растворимого фермента люциферазы, который физиологически не является мишенью анестетиков, но служит в качестве безлипидной модели белковой молекулы для связывания анестетика.
Рисунок 4 | В 20 веке было показано, что сила общих анестетиков коррелируют с их способностью ингибировать активность растворимого фермента люциферазы, который физиологически не является мишенью анестетиков, но служит в качестве безлипидной модели белковой молекулы для связывания анестетика.
Современные факты позволяют утверждать, что белки в большей степени, чем липиды, являются молекулярными мишенями для действия анестетиков. Взаимодействие анестетиков с гидрофобными участками белков также объясняет правило Мейер-Овертона. Прямое взаимодействие молекул анестетиков с белками позволяет объяснить исключения из этого правила, так как любые участки связи с белком определяются как размером и формой молекулы, так и растворимостью. Многочисленные физические методы (рентгенодифракция, ЯМР-спектроскопия) подтверждают, что общие анестетики действуют путем непосредственного связывания с амфифильными полостями белковых молекул, а размер связанного участка объясняет эффект «обрубания» свойства (более длинные спирты теряют свойства анестетика).
Механизм действия
Таким образом, общие анестетики изменяют физико-химические свойства липидов мембран нейронов и нарушают взаимодействие липидов с белками ионных каналов. При этом уменьшается транспорт в нейроны ионов натрия, сохраняется выход менее гидратированных ионов калия, в 1,5 раза возрастает проницаемость хлорных каналов, управляемых ГАМК-А рецепторами. Итогом этих эффектов становится гиперполяризация с усилением процессов торможения. Общие анестетики подавляют вход в нейроны ионов кальция, блокируя Н-холинорецепторы и NMDA-рецепторы глутаминовой кислоты; снижают подвижность Са2+ в мембране, поэтому препятствуют кальций-зависимому выделению возбуждающих нейромедиаторов. Наиболее чувствительны к действию общих анестетиков полисинаптические системы ЦНС — кора больших полушарий (1013 – 1014 синапсов), таламус, ретикулярная формация, спинной мозг. К наркозу устойчивы дыхательный и сосудодвигательный центры продолговатого мозга.
Летучие ингаляционные анестетики:
- постсинаптически усиливают тормозящую передачу путем потенциирования лиганд-управляемых ионных каналов, активируемых ГАМК и глицином;
- экстрасинаптиески путем усиления ГАМК-рецепторов и ионных токов утечки;
- пресинаптически за счет повышения базального высвобождения ГАМК.
Ингаляционные анестетики подавляют возбуждающую синаптическую передачу путем снижения высвобождения глутамата и постсинаптически путем ингибирования ионотропных глутаматных рецепторов. Парализующий эффект местных анестетиков включает действие на спинной мозг, в то время как седация/наркоз и амнезия включают супраспинальные механизмы памяти, сна и сознания.
2.1.2. Газовый наркоз
В анестезиологии широко применяют ингаляционный газовый анестетик азота закись (N2O). В конце 1980-х гг. в зарубежную анестезиологическую практику вошел инертный газ ксенон.
Азота закись представляет собой бесцветный газ характерного запаха, хранится в металлических баллонах под давлением 50 атм в жидком состоянии, не горит, но поддерживает горение. Ее смеси с анестетиками группы летучих жидкостей в определенных концентрациях взрывоопасны. В субнаркотических концентрациях (20 — 30 %) азота закись вызывает эйфорию (веселящий газ) и сильную анальгезию. В концентрации 20 % обеспечивает обезболивание в такой же степени, как 15 мг морфина. Закись азота на ГАМК-А рецепторы не влияет. Используется только в комбинациях, так как МАК составляет 104 %.
Инертный газ ксенон считают лучшей альтернативой азота закиси, так как он обладает более выраженным наркозным действием, индифферентностью и экологической безопасностью. Способность ксенона вызвать наркоз была открыта в связи с практикой глубоководных погружений и развитием гипербарической физиологии. Ксенон бесцветен, не горит и не обладает запахом, при соприкосновении со слизистой оболочкой рта создает на языке ощущение горьковатого металлического вкуса. Отличается низкой вязкостью и высокой растворимостью в липидах, выводится легкими в неизмененном виде. Разработана технология ксенонсберегающей анестезии с включением минимального потока и системы рециклинга для повторного многократного использования газа. Такая технология успешно решает важную в практическом отношении проблему дефицита и дороговизны ксенона. В механизме наркозного эффекта ксенона имеют значение блокада циторецепторов возбуждающих нейромедиаторов — Н-холинорецепторов, NMDA-рецепторов глутаминовой кислоты, а также активация рецепторов тормозящего нейромедиатора глицина. При взаимодействии с циторецепторами ксенон выступает как протонсвязывающий кластер и образует комплексы с катионами НСО+, NH2+, HNCH+. Ксенон проявляет свойства антиоксиданта и иммуностимулятора, снижает выделение гидрокортизона и адреналина из надпочечников.
2.2. Неингаляционные (внутривенные) наркозные средства подразделяют на три группы:
Препараты короткого действия (3 — 5 мин)
- пропанидин (эпонтол, сомбревин)
- пропофол (диприван, рекофол)
Препараты средней продолжительности действия (20 — 30 мин)
- кетамин (калипсол, кеталар, кетанест)
- мидазолам (дормикум, флормидал)
- гексенал (гексобарбитал-натрий)
- тиопентал-натрий (пентотал)
Препараты длительного действия (0,5 — 2 ч)
- натрия оксибутират
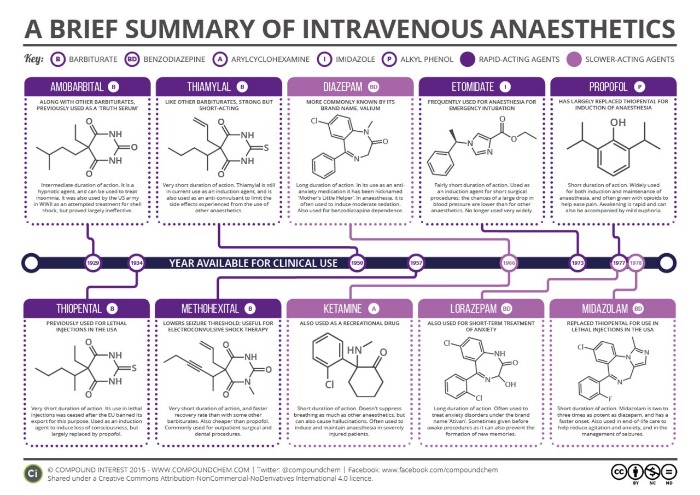 Рисунок 5 | Общие анестетики для внутривенного введения
Рисунок 5 | Общие анестетики для внутривенного введения
Механизм действия
Наиболее широко используемым внутривенный анестетиком является пропофол. Его механизм действия связан с увеличение хлорной проводимости ГАМК рецепторов.
Метогекситал по скорости наступления и выхода из наркоза близок к пропофолу.
Барбитураты использовались для анестезии до введения в практику пропофола. Тиопентал вызывает быстрое наступление и быстрый выход из наркоза при разовом введении, но он быстро накапливается при повторном или пролонгированном введении и таким образом замедляет выход из анестезии. Барбитураты являются лигандами барбитуратных рецепторов. В малых дозах они аллостерически усиливают действие ГАМК на ГАМК А-рецепторы . При этом удлиняется открытое состояние хлорных каналов, возрастает вход в нейроны анионов хлора, развиваются гиперполяризация и торможение. В больших дозах барбитураты прямо повышают хлорную проницаемость мембран нейронов. Кроме того, они тормозят высвобождение возбуждающих медиаторов ЦНС — ацетилхолина и глутаминовой кислоты, блокируют АМРА-рецепторы (квисквалатные рецепторы ) глутаминовой кислоты. Барбитураты обладают церебропротективными свойствами и могут быть использованы с такой целью.
Бензодиазепины используются в основном как анксиолитики и для седации с сохранением сознания.Все бензодиазепиновые рецепторы аллостерически усиливают кооперацию ГАМК с ГАМК А-рецепторами, что сопровождается повышением хлорной проводимости нейронов, развитием гиперполяризации и торможения. Реакция с бензодиазепиновыми рецепторами происходит только в присутствии ГАМК. Ремимазолам – самый молодой бензодиазепин, имеет очень короткое время действия из-за быстрой нейтрализации эстеразами плазмы.
Кетамин химически является производным фенциклидина. Синаптические механизмы действия кетамина многообразны. Он является неконкурентным антагонистом возбуждающих медиаторов головного мозга глутаминовой и аспарагиновой кислот в отношении NMDA-рецепторов. Эти рецепторы активируют натриевые, калиевые и кальциевые каналы мембран нейронов. При блокаде рецепторов нарушается деполяризация. Кроме того, кетамин стимулирует освобождение энкефалинов и β-эндорфина; тормозит нейрональный захват серотонина и норадреналина. Последний эффект проявляется тахикардией, ростом АД и внутричерепного давления. Кетамин расширяет бронхи. При выходе из кетаминового наркоза возможны бред, галлюцинации, двигательное возбуждение (эти нежелательные явления предупреждают введением дроперидола или транквилизаторов).Важным терапевтическим эффектом кетамина является нейропротективный. Как известно, в первые минуты гипоксии мозга происходит выброс возбуждающих медиаторов — глутаминовой и аспарагиновой кислот. Последующая активация NMDA-рецепторов, увеличивая во внутриклеточной среде концентрацию ионов натрия и кальция и осмотическое давление, вызывает набухание и гибель нейронов. Кетамин как антагонист NMDA-рецепторов устраняет перегрузку нейронов ионами и связанный с этим неврологический дефицит.
Самым новым внутривенным анестетиком является дексмедетомидин. Это высокоселективный агонист а2-адренорецепторов с седативными, симпатолитическими, снотворными и анальгетическими эффектами. Его основное действие – в качестве агониста на а2 рецепторы в голубом пятне.
Источники:
- Теории механизма действия – https://en.wikipedia.org/wiki/Theories_of_general_anaesthetic_action и https://www.esus.ru/php/content.php?id=744
- Венгеровский А.И., Лекции по фармакологии для врачей и провизоров 2007
- Харкевич, Фармакология изд. 10
- Miller’s anesthesia / [edited by] Ronald D. Miller ; associate editors, Neal H. Cohen, Lars I. Eriksson, Lee A. Fleisher, Jeanine P. Wiener-Kronish, William L. Young. — Eighth edition. 2015
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.
Источник

