Роль лизосом в воспалении
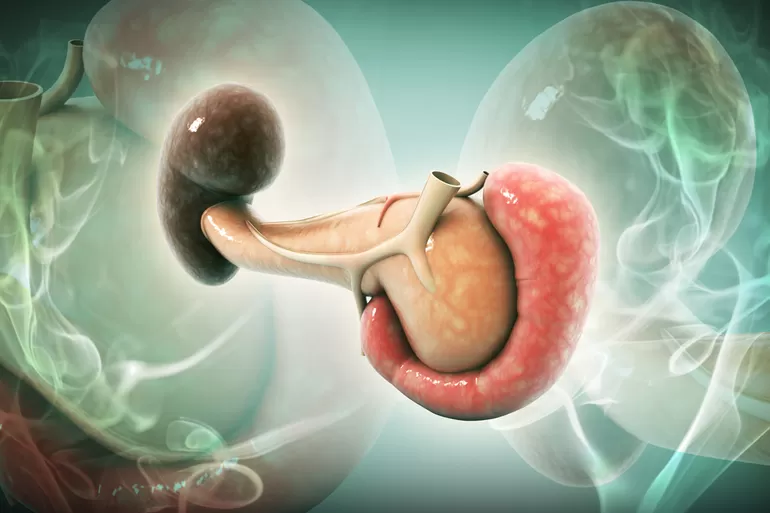
Значение лизосом в патологии столь многогранно и существенно, что в настоящее время трудно представить патологический процесс, в который не был бы вовлечен лизосомальный аппарат клетки. Следует выделить два аспекта этой проблемы. Во-первых, вовлечение лизосом в развитие таких общих патологических процессов, как воспаление и некроз и в этом случае участие лизосом является одним из проявлений их нормальной защитной функции организма в ответ на возникновение очага инфекции. Однако развитие ряда патологий связано с нарушением структуры и функции самих лизосом. Нарушения в лизосомах являются первичным, пусковым звеном в развитии двух типов патологических процессов. Для первого из них характерно повреждение лизосомальных мембран. Каковы же обстоятельства, способствующие возникновению патологической дестабилизации лизосомальной мембраны, ведущей к выходу в клеточный матрикс кислых гидролаз? Установлено, что проницаемость лизосомальных мембран значительно увеличивается при гипоксии (недостаток кислорода), изменении кислотно-щелочного равновесия, после травм и хирургических вмешательств, голодании, при заболеваниях суставов и инфекционных заболеваниях, воздействии ионизирующей радиации и некоторых химических агентов. Последнее нашло практическое применение, в частности направленное повреждающее воздействие некоторых фармакологических агентов и ионизирующей радиации на мембраны лизосом опухолевых клеток используется при лекарственной и радиотерапии онкологических заболеваний. Из патологических состояний, связанных с повреждением лизосомальных мембран и высвобождением гидролаз, наиболее изучены болезни суставов – острый и ревматоидный артриты, подагра. При этих заболеваниях, в результате воздействия лизосомальных ферментов, наблюдается эрозия хрящей и деструкция суставов Показано, что аналогичные изменения могут быть получены у экспериментальных животных при введении в область сустава, веществ, обладающих дестабилизирующим действием на лизосомальные мембраны, например стрептолизина S. Наоборот, вещества, стабилизирующие лизосомальные мембраны (к ним относятся многие противовоспалительные препараты, например, глюкокортикостероид – кортизон), значительно уменьшают воспалительную реакцию.
К другой, сравнительно редкой группе заболеваний обусловленных нарушением функции лизосом, относят врожденные генетические нарушения в системе синтеза лизосомальных ферментов. Эти нарушения приводит к развитию так называемых лизосомальных болезней накопления. Такие болезни вызываются, главным образом, мутацией в гене, кодирующем ту или иную гидролазу, что выражается либо в полном подавлении синтеза ферментного белка, либо в синтезе белковых молекул обладающих резко сниженной биокаталитической активностью. Кроме этого генетически обусловленными могут быть нарушения при которых ферментный белок синтезируется без сигнальных участков и по этой причине не распознается транспортной системой. В результате блокируется его доставка из аппарата Гольджи в лизосомы. Нерасщепленный субстрат такой гидролазы накапливается в лизосомах, что приводит к переполнению клеток разбухшими лизосомами, клетки приобретают пенистый вид (пенистые клетки), утрачивают вследствие этого свои функциональные свойства и в конечном результате погибают, что ведет к развитию тяжелых заболеваний (напр. болезнь Тей-Сакса, Гоше, Нимана-Пика и др.), заканчивающихся во многих случаях смертельным исходом в детском возрасте.
Источник
Значение лизосом в патологии столь многогранно и существенно, что в настоящее время трудно представить патологический процесс, в который не был бы вовлечен лизосомальный аппарат клетки. Следует выделить два аспекта этой проблемы. Во-первых, вовлечение лизосом в развитие таких общих патологических процессов, как воспаление и некроз и в этом случае участие лизосом является одним из проявлений их нормальной защитной функции организма в ответ на возникновение очага инфекции. Однако развитие ряда болезней связано с нарушением структуры и функции самих лизосом. Например, некоторые внутриклеточные инфекции (туберкулез) вызываются микробами выделяющими фактор, препятствующий слиянию фагосомы с эндолизосомой.
Нарушения в лизосомах являются первичным, пусковым звеном в развитии двух типов патологических процессов. Для первого из них характерно повреждение лизосомальных мембран. Каковы же обстоятельства, способствующие возникновению патологической дестабилизации лизосомальной мембраны, ведущей к выходу в клеточный матрикс кислых гидролаз? Установлено, что проницаемость лизосомальных мембран значительно увеличивается при гипоксии (недостаток кислорода), изменении кислотно-щелочного равновесия, после травм и хирургических вмешательств, голодании, при заболеваниях суставов и инфекционных заболеваниях, воздействии ионизирующей радиации и некоторых химических агентов. Последнее нашло практическое применение, в частности направленное повреждающее воздействие некоторых фармакологических агентов и ионизирующей радиации на мембраны лизосом опухолевых клеток используется при лекарственной и радиотерапии онкологических заболеваний. Из патологических состояний, связанных с повреждением лизосомальных мембран и высвобождением гидролаз, наиболее изучены болезни суставов – острый и ревматоидный артриты, подагра. При этих заболеваниях, в результате воздействия лизосомальных ферментов, наблюдается эрозия хрящей и деструкция суставов Показано, что аналогичные изменения могут быть получены у экспериментальных животных при введении в область сустава, веществ, обладающих дестабилизирующим действием на лизосомальные мембраны, например стрептолизина S. Наоборот, вещества, стабилизирующие лизосомальные мембраны (к ним относятся многие противовоспалительные препараты, например, глюкокортикостероид – кортизон), значительно уменьшают воспалительную реакцию.
К другой, сравнительно редкой группе заболеваний обусловленных нарушением функции лизосом, относят врожденные генетические нарушения в системе синтеза лизосомальных ферментов. Эти нарушения приводит к развитию так называемых лизосомальных болезней накопления. Такие болезни вызываются, главным образом, мутацией в гене, кодирующем ту или иную гидролазу, что выражается либо в полном подавлении синтеза ферментного белка, либо в синтезе белковых молекул обладающих резко сниженной биокаталитической активностью. Кроме этого генетически обусловленными могут быть нарушения при которых ферментный белок синтезируется без сигнальных участков и по этой причине не распознается транспортной системой. В результате блокируется его доставка из аппарата Гольджи в лизосомы. Нерасщепленный субстрат такой гидролазы накапливается в лизосомах, что приводит к переполнению клеток разбухшими лизосомами, клетки приобретают пенистый вид (пенистые клетки), утрачивают вследствие этого свои функциональные свойства и в конечном результате погибают, что ведет к развитию тяжелых заболеваний заканчивающихся во многих случаях смертельным исходом в детском возрасте.
болезнь Тей-Сакса вызывается мутацией гена, ответственного за фермент гексозоаминидазу, принимающего участие в метаболизме ганглиозидов, которые накапливаются в нервных клетках, нарушая их работу. В основном поражает евреев-ашкенази. Проявляется вскоре после рождения. К признакам относятся слепота, глухота, прогрессирующее слабоумие, судороги, паралич. Смерть наступает в возрасте до 3 лет.
Болезнь Нимана-Пика развивается из-за дефицита фермента сфингомиелиназы (сфингомиелинфосфодиэстеразы), катализирующего гидролиз сфингомиелина с образованием фосфорилхолина и церамидных остатков. при этом происходит накопление и отложение сфингомиелина в мозге.и др.), характеризуется увеличением печени и селезёнки (гепатоспленомегалия) и прогрессивным поражением нервной системы. При этом дети не переживают раннего детского периода. Наиболее частая встречаемость этого типа болезни Ниманна-Пика наблюдается у евреев-ашкенази (выходцев из Центральной и Восточной Европы) — примерно 1 случай на 40 тысяч.
Хампердинг и Кочран утверждают, что именно эти болезни ответственны за более высокий умственный потенциал евреев, поскольку они приводят, в частности, к увеличению дендритов на нейронах мозга.
Болезнь Гоше В основе заболевания лежит наследственно обусловленный дефицит фермента – глюкозилцерамидазы, вследствие чего происходит накопление неметаболизированных липидов в макрофагальных клетках, скопления которых ведут к поражению тканей печени, костного мозга, легких увеличение селезенки вплот до разрывов. Больные могут доживать до взрослого возраста Наиболее часто встречается среди ашкеназских евреев.
Синдром Фабри обусловлен недостаточностью фермента альфа-галактозидазы,способной отщеплять терминальные остатки α-D-галактозы от α-D-галактозидов, в том числе от галактоолигосахаридов, галактоманнанов и галактолипидов. При дефиците данного фермента в лизосомах накапливается субстрат реакции – церамид-тригексозид. Смерть наиболее часто наступает от сосудистых поражений сердца и головного мозга на 4-м десятилетии жизни.
Клеточное ядро и геном
Рекомендуемые страницы:
Источник
Форма простейших
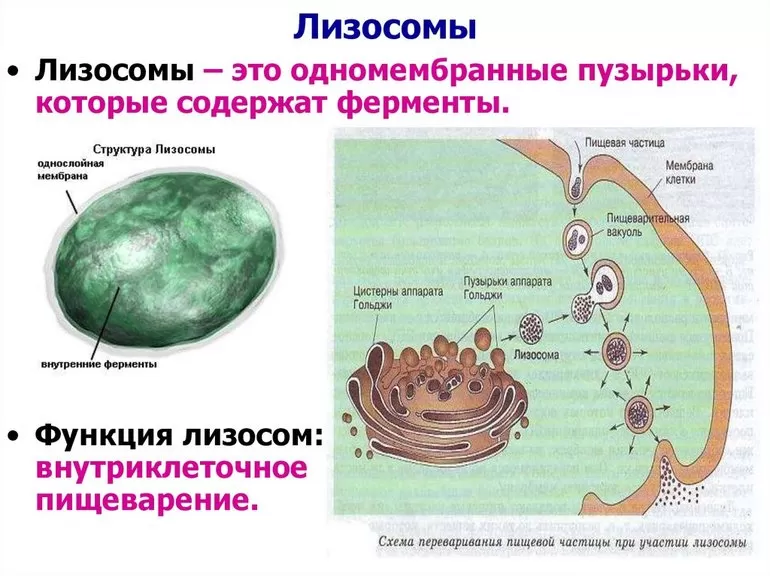
В своей форме лизосомы визуализируют в виде плотных шаровидных вакуоли, но они могут показывать значительные отличия размера, в зависимости от материалов, которые были приняты для пищеварения (см.рисунок).
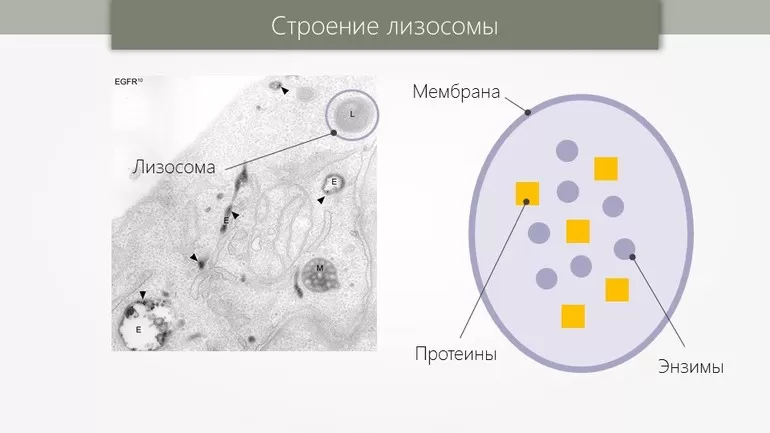
Из таблицы строения и функций лизосом видно, что они обычно сферической формы, с диаметром от 0,05 до 0,5 мкм. На электронных микрофотографиях они имеют форму равномерно-зернистых, электронно-плотных структур (см. схему). Таким образом, особенности строения лизосом в том, что они представляют собой морфологически разнообразные органеллы, проводят определение общей функции деградации внутриклеточного материала.
Это цитоплазматические внутриорганические органеллы, принадлежащие к эндомембранной системе, содержащей ферменты (кислотные гидролазы), которые разрушают многие биологические молекулы. Они встречаются во всех клетках, но чаще — в ответственных за защиту организма: макрофагах, нейтрофильных полинуклеарных или очень специализированных клетках, таких как остеокласты. Первичный видимый в оптической и электронной микроскопии гетерогенный вид лизосом обнаруживается гистоэнзимологической окраской кислой фосфатазы.
Ферменты вида
Лизосомы содержат около 50 различных разлагающих комплексов ферментов, которые могут гидролизовать белки, ДНК, РНК, полисахариды и липиды. Мутации в генах, что кодируют эти ферменты, ответственны за более чем 30 различных генетических заболеваний человека, которые называются лизосомальными заболеваниями хранения, потому что необработанный материал накапливается. Большинство из этих остаточных заболеваний является результатом дефицита отдельных химических лизосомальных ферментов. Например:

- Болезнь под названием Гоше (наиболее распространённое из этих расстройств) является результатом мутации в гене, который кодирует лизосомальный фермент, необходимый для расщепления гликолипидов.
- Клеточное заболевание, которое вызвано дефицитом фермента, катализирующего первый этап мечения лизосомальных ферментов маннозой-6-фосфатом в аппарате Гольджи.
Это всё результат общей неспособности лизосомальных ферментов, которые должны быть включены в органеллах.
Все лизосомальные ферменты являются гидролазами, что активны при рН (около 5), который поддерживается в лизосомах, но не при нейтральном показателе (около 7,2), характерном для остальной цитоплазмы. Требование этих лизосомальных гидролаз для кислотного рН обеспечивает двойную защиту против неконтролируемого пищеварения содержания цитозоля. Даже если лизосомальная мембрана опущена, выпущенные кисловочные гидролазы были бы неактивны на нейтральном рН цитозоля.
Для поддержания кислотного внутреннего рН лизосомы должны активно концентрировать ионы H+ (протоны). Это достигается протонным насосом в лизосомальной мембране, который активно транспортирует протоны в лизосому из цитозоля. Эта перекачка требует затрат энергии в виде гидролиза АТФ, так как она поддерживает примерно в сто раз более высокую концентрацию H+ внутри лизосомы. Органоиды содержат различные кислотные гидролазы, которые активны при кислотном рН, поддерживаемом в органелле, но не при нейтральном рН цитозоля.
Образование органелл
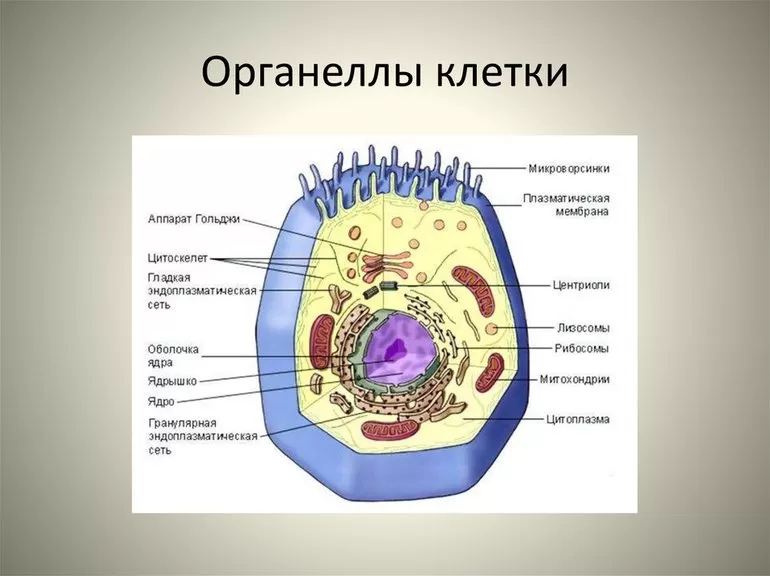
Одной из основных функций лизосом является переваривание материала, взятого извне клетки эндоцитозом. Однако роль органелл в переваривании материала, принимаемого эндоцитозом, связана не только с функцией органелл, но и с их образованием. В частности, лизосомы образуются путём слияния транспортных везикул, почковавшихся из транс-Гольджи сети с эндосомами, которые содержат молекулы, принятые эндоцитозом на плазматической мембране.
Нужно выяснить, где формируются лизосомы и в чём их отличие в биологии. Появление органелл представляет собой пересечение секреторных путей (через них обрабатываются лизосомальные белки) и эндоцитозного пути, через которые молекулы внеклеточного занимают место на поверхности клетки. Материал извне клетки берётся в покрытых клатрином эндоцитарных везикулах, которые распускаются из плазматической мембраны и затем сливаются с ранними эндосомами.
Компоненты затем рециркулируются в плазматическую мембрану и ранние эндосомы постепенно созревают в поздние, которые являются предшественниками лизосом. Одним из важных изменений во время созревания эндосомы является снижение внутреннего рН примерно до 5,5, что играет ключевую роль в доставке лизосомальных кислотных гидролаз из сети транс-гольджи.
Эндоцитоз и образование
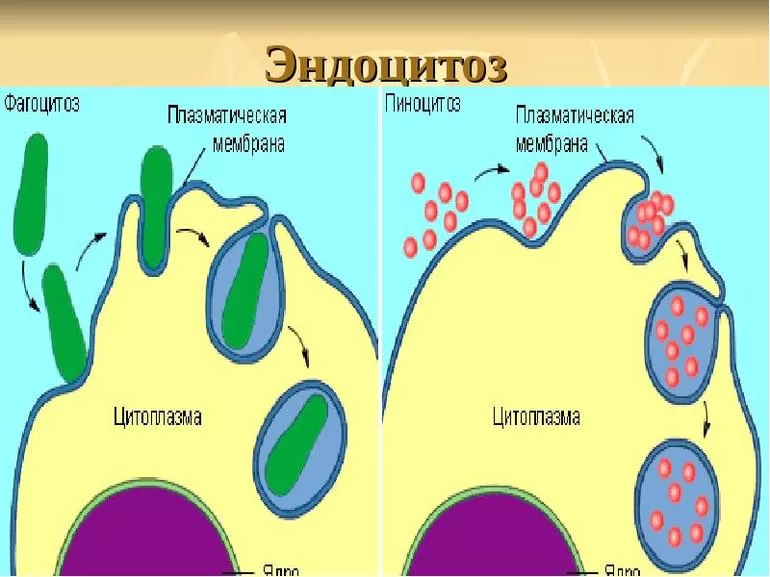
Молекулы берутся извне клетки в эндоцитарных везикулах, которые сливаются с ранними эндосомами. Мембранные компоненты перерабатываются по мере созревания ранних эндосом в поздние.
Кислотные гидролазы нацелены на лизосомы остатками манноза-6-фосфата, которые распознаются рецепторами манноза-6-фосфата в сети транс-Гольджи и упаковываются в клатрин-покрытые везикулы. После удаления слоя клатрина эти транспортные везикулы сливаются с поздними эндосомами, а кислотный внутренний рН приводит к диссоциации гидролаз с рецептором манноза-6-фосфата.
Таким образом, гидролазы высвобождаются в просвет эндосомы, в то время как рецепторы остаются в мембране и в итоге рециркулируются в Гольджи. Поздние эндосомы затем созревают в лизосомы, поскольку они приобретают полный набор кислотных гидролаз, которые переваривают молекулы, первоначально принятые эндоцитозом.
Фагоцитоз и аутофагия
Помимо деградирующих молекул, поглощаемых эндоцитозом, лизосомы переваривают материал, полученный двумя другими путями — фагоцитозом и аутофагией. При фагоцитозе специализированные клетки, такие как макрофаги, поглощают и разрушают крупные частицы, включая бактерии, клеточный мусор и старые клетки, которые необходимо удалить из организма.
Такие крупные частицы попадают в фагоцитарные вакуоли (фагосомы), которые затем сливаются с лизосомами, в результате чего происходит переваривание их содержимого. Образующиеся таким образом лизосомы (фаголизосомы) могут быть довольно крупными и неоднородными, так как их размер и форма определяются содержанием перевариваемого материала.
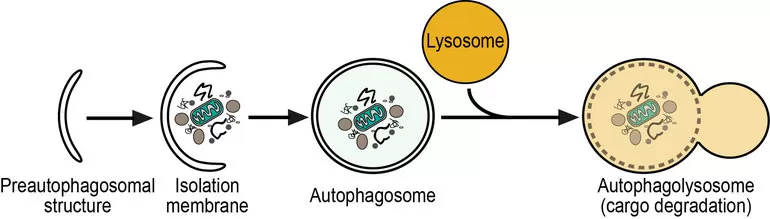
При фагоцитозе крупные частицы, например, бактерии, попадают в фагоцитарные вакуоли или фагосомы. В аутофагии внутренние органеллы, например, митохондрии, заключены в мембранные фрагменты из ER.
Лизосомы также отвечают за аутофагию — постепенный оборот собственных компонентов клетки. Первым шагом аутофагии, по-видимому, является включение органеллы (например, митохондрии) в мембрану, полученную из ER. Образовавшийся пузырёк затем сливается с лизосомой, его содержимое переваривается.
Патофизиологическая роль
У многих примитивных одноклеточных и беспозвоночных микроорганизмов роль лизосом, в первую очередь, питательная. Гетерофагия используется для захвата и переваривания экзогенных продуктов, аутофагия — для контролируемого использования чистых клеточных компонентов в случае нехватки пищи. Эта функция потеряла значение у высших животных, где она действует только для некоторых конкретных питательных веществ, таких как холестерин. С другой стороны, лизосомальное пищеварение подходит для многих специализированных функций.
Таким образом, в зависимости от клеточного типа, гетерофагический механизм служит:
- для защиты от захватчиков;
- очистки альвеол лёгких;
- реабсорбции почек;
- перестановки костей;
- катаболизма белков плазмы;
- регуляции гормональных эффектов;
- синтеза гормонов щитовидной железы и многих других физиологических процессов.
Аутофагия играет очень общую роль в многочисленных аутолитических явлениях, которые происходят в обновлении клеточных составляющих, а также в адаптации, дифференциации и развитии растительных компонентов.
Лизосомы часто могут находиться и участвовать в формировании генеза патологических состояний. Гидролазы, которые они размещают, могут повредить цитоплазму, когда они высвобождаются внутри клетки или внеклеточные структуры, если они сбрасываются снаружи. Кроме того, перегрузка лизосом непереваренными материалами и последующее расширение могут поставить под угрозу нормальную клеточную функцию. Благодаря выяснению этих механизмов, многие заболевания оказались проявлениями клеточной пищеварительной патологии:
- внутриклеточные выделения лизосомального содержимого (клеточные структуры повреждаются и часто клетки погибают) ;
- силикозы, воспаления, интоксикации лизосомотропными веществами.
Функциональные механизмы
Лизосомы играют важную роль во внутриклеточном пищеварении. Этот процесс происходит в вакуолях, ограниченных мембраной, вторичными лизосомами, в пределах которых кислотный рН в диапазоне от 4,5 до 5,0, соответствующий требованиям лизосомиальных гидролаз, активно поддерживается протонным насосом, расположенным в мембране.
Эта кислотность объясняет «лизосомотропизм» очень многих слабо основных соединений: они концентрируются в лизосомах с протонацией и приводят к таким явлениям, как жизненная окраска (например, нейтральный красный, оранжевый акридин), вакуолизация осмотическим вызовом воды, например, хлорохин, и различные фармакологические эффекты.
Исключительно гидролазы и лизосомиальная кислотность сбрасываются во внеклеточную полость, где они выполняют своё пищеварительное действие. Субстраты лизосомального пищеварения поступают извне или изнутри клетки. В первом случае (гетерофагия) захват материалов осуществляется фагоцитозом, пиноцитозом или любой другой формой эндоцитоза, т. е. процессом, включающим инвагинацию плазматической мембраны, которая закрывается вокруг захваченного материала и отделяется в цитоплазме в виде герметичной вакуоли, содержащей этот материал.
Объекты и молекулы, охватываемые таким образом, часто фиксируются специфическими рецепторами, расположенными на плазматической мембране (эндоцитоз интерпозированным рецептором). Это явление позволяет клеткам выбирать определённые питательные вещества в их окружающей среде, например, липопротеины низкой плотности, несущие холестерин. Это даёт им, кроме того, способ ограничивать действие гормонов и других активных агентов.
Источник
