Роль воспаления при атерогенезе
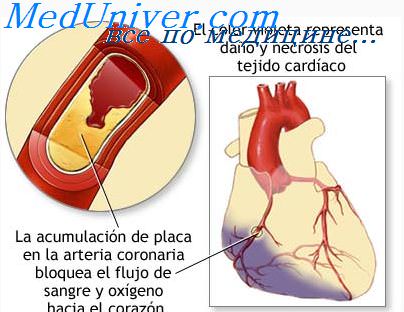
Атерогенез. Этапы развития атеросклероза. Местные причины атеросклероза.Задолго до клинических проявлений атеросклероза в интиме и подслизистом слое артерий запускается сложный патогенетический механизм формирования бляшки. Ее развитие представляет условный стадийный процесс: начальные поражения (рост проницаемости эндотелия, адгезия и миграция моноцитов, появление отдельных пенистых клеток, миграция ГМК) -> липидные полоски и пятна (не возвышающиеся над поверхностью) -> «перламутровые» бляшки, возвышающиеся над поверхностью интимы (атерома со сформировавшимся липидным ядром) -> фиброатерома (имеет липидное ядро и «покрышку») -> фиброз и кальциноз бляшек (отложение большого количества солей кальция) -> ослабление и разрывы бляшки с изъязвлением, наложением и ростом тромботических масс (интрамуральные тромбозы, приводящие к различной степени нарушениям кровотока в артериях) и последующая утрата эластичности и сократимости артерий. На начальных этапах атеросклероза формируются атерогенная гиперлипопротеинемия под действием ФР и ряда этиологических причин (нарушение функции печени, кишечника, эндокринных желез) и внеклеточное накоплениелипидов (и их модификация) в интиме артерий (инфильтрация модифицированными ЛП сосудистой стенки). Атерогенные ХСЛПНП проникают в интиму артерий вследствие дисфункции эндотелия — повышения его проницаемости и адгезивности, нарушения удаления ХС из интимы артерий, активации ПОЛ и включения иммунных механизмов за счет образования антител к атерогенным ХСЛПНП. При атеросклерозе также возникает поломка транспорта ХС, рецепторов и эндотелия артерий. Если отмечается избыток липидов в клетке, то активируются процессы ПОЛ и ХС становится чужеродным для клетки.
В начале формирования атеросклероза выделяют следующие важные местные механизмы атерогенеза: Под действием классических ФР (курения, гиперхолестеринемии, воспаления, АГ, СД, старения, менопаузы и др ) формируется дезорганизация эндотелиальных клеток артерий (нарушается барьерная функция эндотелия), в результате чего снижается синтез и выделение N0, повышаются экспрессия на поверхности эндотелия веществ, притягивающих воспалительные клетки, и проницаемость сосудистой стенки Все это приводит к притоку и инфильтрации субэндотелиального слоя стенок артерий воспалительными клетками крови (лимфоциты, макрофаги) и белками плазмы (СРП и др). Последнее благоприятствует изменению функциональных свойств эндотелия повышению проницаемости интимы, росту клеточной инфильтрации стенки артерии Причины дисфункции эндотелия артерий• высокие гемодинамические нагрузки крови на стенку артерии, ее «износ» вследствие гидродинамических ударов крови по эндотелию в участках разветвления артерий либо их высокой кривизны (появляется вихревой или турбулентный кровоток), Число дефектов эндотелия с возрастом увеличивается (это «расплата» за АГ, курение и другие ФР), что приводит к нарушению релаксации и локальной выработки N0, а в последующем — к повышению агрегация тромбоцитов и их адгезии в эту зону (тромбоциты прилипают к субэндотелиальному коллагену) Повреждение эндотелия — общий механизм формирования АГ и атеросклероза – Также рекомендуем “Фазы атеросклероза. Стадии развития атеросклероза.” Оглавление темы “Механизмы развития атеросклероза. Клиника атеросклероза.”: |
Источник
В статье представлены основные теории развития атеросклероза и современные взгляды на роль воспаления в атерогенезе. Проведен обзор исследований по изучению роли эндотелиальных местных факторов, таких как накопление гладких мышечных клеток, Т и В лимфоцитов, макрофагов, матриксной металлопротеиназы (ММП), высокочувствительного С реактивного белка (СРБ). Показано, что низкий окислительный стресс модулирует эндотелиальную экспрессию гена, индуцирующего атерогенный фактор, который формирует раннюю атеросклеротическую бляшку (АБ). СРБ и окисленные липопротеиды низкой плотности (ОЛНП) непосредственно связаны с воспалительным повреждением артерий при ишемической болезни сердца (ИБС). Моноциты, активизированные в участках воспаления моноцит хемоаттрактантным белком (MХБ 1) и ММП 1, играют главную роль в разрыве АБ. СРБ и ОЛНП увеличивают синтез MMП, alpha фактора некроза опухоли (ФНО alpha) и гранулоцитарно макрофагального колониестимулирующего фактора (ГМ КСФ). Кроме того, дополнение экзогенного MХБ 1 или простагландина Е2 повышает синтез моноцитами MMП 1, ФНО alpha и ГМ КСФ. Апоптоз гладких мышечных клеток фиброзной покрышки дополняется разрушением ММП 1 внеклеточных матричных белков, приводящих в к разрыву АБ.
История изучения. История изучения атеросклероза полна как открытий, так и разочарований, как догм, тормозивших прогресс в познании причин болезни, так и революционных прорывов в выяснении механизмов ее формирования. Но еще больше в ней гипотез и вопросов, оставленных предыдущими поколениями исследователей, подтвердить которые было нелегко. Использование культур клеток, изучение липидного обмена на молекулярном уровне, мутации и экспрессии генов, иммуноферментный анализ, оценка состояния рецепторов клеток, изучение системы цитокинов и многие другие современные методы исследования позволили раскрыть сущность целого ряда механизмов возникновения атеросклероза, показали сложный характер этого процесса [1].
По определению экспертов ВОЗ, атеросклероз — это изменение интимы артерий (в отличие от артериол) с очаговым накоплением липидов, сложных углеводов и развитием соединительной ткани, кальциевых отложений и изменений в медии (Бюллетень ВОЗ, 1985). Атеросклероз — основная причина смерти в развитых странах. Это прогрессирующий патологический процесс, который начинается в детстве и дает клинические проявления в середине взрослой жизни [2]. Стенокардия как клиническое проявление атеросклероза может встречаться у лиц старше 20 лет, но чаще у мужчин в возрасте 50—60 лет и у женщин старше 60 лет. Если два десятилетия назад атеросклероз считали дегенеративным процессом с накоплением липидов и некротических отложений, то теперь ученые полагают, что это многофакторный процесс, ведущий к обширному накоплению гладких мышечных клеток (ГМК) в интиме вовлеченной в процесс артерии. Форму и содержание прогрессирующих повреждений при атеросклерозе демонстрируют результаты 3 фундаментальных биологических процессов: 1) накопление макрофагов, Т-лимфоцитов и ГМК в интиме; 2) формирование накопленными ГМК большого количества матрицы соединительной ткани, включающей коллаген, эластин и протеогликаны; 3) накопление липидов, преимущественно в форме свободного холестерина и его эфиров как в клетках, так и в окружающей соединительной ткани.
Большой интерес вызвала так называемая мутагенная моноклональная теория, выдвинутая E.P. Benditt и J.M. Benditt (1976) [3]. Ученые исходили из того, что ГМК фиброзных бляшек всегда гомозиготны и гомогенны по своему составу и, очевидно, происходят из одного клона клеток, а возможно, из одной единственной ГМК и являются моноклональными (подтверждено, что 80% ГМК являются моноклональными). В связи с этим очевидно предположение, что под влиянием каких-либо повреждений происходит мутация одной ГМК и начинается пролиферативный процесс, приводящий к формированию фиброзной бляшки. Здесь авторы проводят аналогию между опухолями доброкачественной природы, такими как лейомиома, и фиброзной бляшкой, считая, что их гипотеза может объяснить многие неясные вопросы атеросклероза, в частности, несовпадения в локализации липидных пятен и фиброзных бляшек, позволяет также рассматривать некоторые факторы риска с точки зрения их мутагенного воздействия.
Согласно мембранной теории, эфиры холестерина, в отличие от их неэстерифицированных форм, не включаются в двойной фосфолипидный слой мембраны и рассматриваются как защитный фактор клетки [4].
Согласно аутоиммунной теории патогенеза атеросклероза, предложенной А. Климовым и соавт., запуск атеросклеротического процесса вызывают не столько липопротеины, сколько аутоиммунные комплексы, содержащие липопротеины в качестве антигена [5, 6]. Существует в настоящее время и вирусная гипотеза происхождения атеросклероза [7].
Теории о роли воспаления.В настоящее время мы знаем, что в патофизиологии атеросклероза решающую роль играет субклиническое хроническое воспаление. Концепция о роли воспаления в патогенезе атеросклероза и его осложнений обеспечила новую гипотезу связи факторов риска с клеточными и молекулярными изменениями, лежащими в основе этой болезни. Согласно ей, фундаментальная роль воспаления в развитии атеросклероза может привести к новым терапевтическим подходам, избирательно воздействующим на воспалительный процесс, медленно «тлеющий» в атероме [8]. Мишенью воспаления обычно служат так называемые уязвимые атеросклеротические бляшки (АБ) со значительным липидным ядром, обилием макрофагов и тонкой фиброзной покрышкой [9, 10]. Воспаление является филогенетически старейшим типом защитной реакции организма на различные повреждения и внедрение чужеродных агентов. Гипотезу о том, что в основе возникновения и прогрессирования атеросклероза может лежать воспалительный процесс, никак нельзя назвать новой. Такое предположение R. Virchow выдвинул еще в 1856 г. [11]. R. Ross и соавт. подчеркивают значительное сходство воспаления и атеросклероза [12]. В.И. Мазуров и соавт. указывают на воспалительный характер поражения сосудов при атеросклерозе, свидетельством которого являются результаты морфологических исследований, а также обнаружение в периферической крови маркеров воспаления [13]. Воспаление играет главную роль на всех стадиях атеросклероза.
Если устойчивые АБ характеризуются хроническим воспалительным инфильтратом, то уязвимые и разорванные АБ отличаются активным воспалением, вовлекающим тонкую волокнистую покрышку. Существование многократных типов уязвимых АБ наводит на мысль, что атеросклероз — диффузный воспалительный процесс. Идентификация морфологических и молекулярных маркеров, способных отличить устойчивые бляшки от уязвимых, позволяет своевременно выделять группу пациентов с высоким риском развития острых сердечно-сосудистых и мозговых сосудистых осложнений до появления клинических симптомов [14].
Внимание исследователей привлекает возможность использования изображений атеросклероза, получаемых с помощью позитронной эмиссионной томографии на молекулярном и метаболическом уровнях. Этот метод имеет определенные преимущества перед плоскостной сцинтиграфией и однофотонной эмиссионной компьютерной томографией вследствие более высокой разрешающей способности и большей возможности маркировать различные биохимические и метаболические процессы, особенно с использованием меток 11С и 18F. Для этого была предложена меченая фтордиоксиглюкоза (18F-ФДГ), применяемая для получения изображений метаболически активных клеток в миокарде, головном мозге и злокачественных новообразованиях. Эта способность данного радиофармпрепарата позволила исследовать изображения макрофагов в АБ. Результаты исследований на экспериментальных моделях у кроликов, находящихся на холестериновой диете, свидетельствуют об активном включении 18F-ФДГ в области атеросклероза с большим количеством макрофагов. В данных работах была показана возможность визуализировать воспаление АБ in vivoс помощью 18F-ФДГ [15].
Процесс атерогенеза имеет сходство с обычным воспалением. Оба процесса состоят из одних и тех же функциональных реакций, где главным действующим компонентом являются клетки рыхлой соединительной ткани: эндотелиальные, ГМК, моноциты, макрофаги, нейтрофилы, тромбоциты, Т- и В-лимфоциты. Признаки локального неспецифического воспалительного процесса при атеросклерозе выявляются на начальных стадиях развития патологии артерий, а также в фазу дестабилизации и повреждения АБ. В большей степени изучена роль воспаления в процессе дестабилизации АБ и доказано, что липиды не причастны к механизму разрушения АБ [16].
Несмотря на то что коронарное русло на всем протяжении подвергается атерогенному эффекту системных факторов риска, атеросклеротическое повреждение возникает в участках эндотелия артериальной стенки. Низкий окислительный стресс модулирует экспрессию в эндотелии гена, индуцирующего атерогенный фактор, и формирует раннюю АБ. Индивидуальная природа прогресса, стабилизации или регресса каждой бляшки зависит не только от формирования и течения атеросклероза, но и от сосудистого ответа, т.е. ремоделирования атеросклеротически измененной стенки сосуда. Механизмы, вовлеченные в ремоделирование подверженной атеросклерозу артериальной стенки, не полностью понятны. Однако изучение динамического взаимодействия между низким эндотелиальным окислительным стрессом и биологией сосудистой стенки представляется очень важным. При этом необходимо учитывать, что АБ с чрезмерным экспансивным ремоделированием можно считать бляшкой высокого риска. Это обусловлено низким эндотелиальным окислительным стрессом, который ведет к непрерывному накапливанию липидов, вызывает воспаление, окислительный стресс, разрушение матрикса и, в конечном счете, дальнейшее прогрессирование экспансивного ремоделирования локальной сосудистой стенки. Углубление знаний в области патобиологии атеросклероза и ремоделирования сосудов могло бы идентифицировать коронарный тромбоз бляшки высокого риска и способствовать применению инновационных диагностических и/или терапевтических стратегий в лечении больных ИБС и предотвращении острых коронарных синдромов (ОКС) [17]. L.G. Spagnoli и соавт. на основании собственных наблюдений делают вывод, что развитие атеросклероза сосредоточено на молекулярных механизмах, затрагивающих прогрессирование бляшки. Что же касается воспалительных маркеров в сыворотке крови, то они отражают воспаление АБ [18].
С-реактивный белок (СРБ) в периферической крови является важным предиктором сердечно-сосудистых заболеваний (ССЗ), и хроническое воспаление может быть механизмом, через который стресс воздействует как фактор риска развития ССЗ [19].
Внутрисосудистое воспаление является ответом на повреждающее воздействие перекисного окисления липидов и, возможно, инфекции [20]. Различные факторы риска, включая артериальную гипертонию, сахарный диабет и курение, усиливаются вредными эффектами окисленных липопро- теидов низкой плотности (ОЛНП) и вызывают хроническую воспалительную реакцию, результат которой — уязвимая бляшка, склонная к разрыву и тромбозу. Результаты эпидемиологических и клинических исследований указывают на высокую корреляцию между маркерами воспаления и риском развития сердечно-сосудистых осложнений.
В настоящее время наиболее надежным и доступным для клинического использования считается высокочувствительный СРБ. С воспалительным повреждением артерий при ИБС непосредственно связаны СРБ и ОЛНП. При этом моноциты и матриксные металлопротеиназы (ММП) могут играть главную роль в разрыве АБ. Моноциты активизируются в участках воспаления моноцит-хемоаттрактантным белком-1 (МХБ-1). При сравнении индивидуального и сочетанного действия СРБ и ОЛНП на MMП-1, изучаемых на моноците, было выявлено, что СРБ и ОЛНП не активизируют MMП-1 в контрольных моноцитах, хотя и увеличивают синтез MMП-1, α-фактора некроза опухоли (ФНО-α), гранулоцитарно-макрофагального колониестимулирующего фактора (ГМ-КСФ). Кроме того, дополнение экзогенного MХБ-1 или простагландина Е2 (ПГЕ2) повышает синтез моноцитами MMП-1, ФНО-αи ГМ-КСФ. Следовательно, комбинация СРБ и ОЛНП может обусловливать усиление роли моноцитов при воспалении. Первый, увеличивая МХБ-1, привлекает больше моноцитов и непосредственно с помощью активизированных моноцитов увеличивает синтез MMП-1. Второй, увеличивая синтез ПГЕ2, также повышает уровень MMП-1 [21].
В атеросклеротически измененных артериях воспалительный ответ вовлекает не только соответствующие клетки стенки артерии, но также циркулирующие лейкоциты. Лимфоциты, как и макрофаги, обязательно участвуют в этом процессе [22]. При активации иммунной системы хрупкий баланс между воспалительным и противовоспалительным состоянием поддерживается врожденной (неспецифической) и адаптивной иммунными системами. Адаптивная иммунная система характеризуется способностью изменять экспрессию рецепторов на новые аутосомные или чужеродные тела. Ее функция заключается в поддержании клеточного и гуморального иммунитета и в регулировании иммунного ответа. Клетки адаптивной иммунной системы включают Т-хелперы (CD4+), цитотоксические T-киллеры (CD8+) и B-лимфоциты. После активации антигеном T-клетки CD4+ могут быть дифференцированы по крайней мере на 3 группы: 1) Th1, который вовлекается в клеточный иммунитет и секретирует провоспалительные цитокины типа γ-интерферона (ИФН-γ); 2) интерлейкин-2 (ИЛ-2), лимфотоксин, Th2, поддерживающие гуморальную устойчивость и секретирующие противовоспалительные цитокины типа ИЛ-4 и ИЛ-10; 3) регулирующие T-клетки (CD4+CD25 +), которые секретируют трансформирующий β-фактор роста (ТФР-β) и ИЛ-10. Лимфоциты вносят вклад в ускорение формирования АБ.
Клетки CD4+CD28 — редко встречающаяся форма лимфоцитов, являются долгожителями. Они секретируют высокие уровни цитотоксичного ИФН-γ. Эти клетки чаще встречаются в нестабильной бляшке и увеличивают лизис эндотелиальных клеток у больных с ОКС [23].
Достаточно доказательств в пользу концепции, что защитная волокнистая покрышка не всегда стабильна и фактически может подвергаться непрерывному и динамическому ремоделированию, проявляя при этом значительную метаболическую активность. Фибриллы интерстициального коллагена придают биомеханическую силу волокнистой покрышке. Баланс между процессами синтеза и деградации, тесно управляемый воспалительными медиаторами, регулируется уровнем коллагена. Как было указано выше, лимфокин ИФН-γ может заблокировать de novoсинтез ГМК промежуточного коллагена — главного источника этого внеклеточного матричного белка в стенке артерии. Провоспалительные цитокины индуцируют экспрессию ферментов, расплавляющих артериальную внеклеточную матрицу. В частности, ММП, включая промежуточные коллагеназы и желатиназы, могут разрушить коллагеновые волокна, придающие силу и упругость волокнистой покрышке бляшки [24]. Недавно выявлено, что некоторые эластолитические катепсины, также регулируемые провоспали- тельными медиаторами и экспрессируемые в атероме, могут ослабить эластин — другой важный компонент внеклеточной матрицы артерий. Примеры включают сульфгидрилзависимые протеиназы катепсинов S и K [25, 26].
Популяция ГМК бляшки также влияет на уровень внеклеточной матрицы. В участках фатального тромбоза механически ослабленные и типично разорванные бляшки имеют немного ГМК [27]. Гибель этих клеток в атеросклеротических повреждениях является источником внеклеточных матричных макромолекул стенок артерий. Апоптоз ГМК в фиброзной покрышке АБ дополняет разрушение внеклеточных матричных белков ММП, приводящих к разрыву АБ. ОЛНП способствуют накоплению липидов, вызывают воспаление и апоптоз, что играет важную роль в патогенезе атеросклероза и разрыва АБ [28, 29]. Клетки апоптоза всегда присутствуют в атеросклеротически измененной сосудистой стенке [30]. В механизме проапоптоза и апоптоза определенную роль играют ОЛНП и их поверхностно-клеточные рецепторы [31].
Отсутствие ГМК приводит к нарушению целостности волокнистой покрышки, потому что эти клетки восстанавливают и поддерживают ее коллагеновую матрицу. Действительно, разорванные бляшки имеют тонкую и рыхлую волокнистую покрышку из-за недостатка коллагена [32, 33]. Редко наблюдаются случаи фатального тромбоза коронарных артерий как результат поверхностной эрозии интимы без открытого разрыва волокнистой покрышки АБ [34]. Воспаление также вносит вклад в механизм коронаротромбоза и в ответ на провоспалительное воздействие медиаторов; эндотелиальные клетки, подобно ГМК, также подвергаются апоптозу. Потеря эндотелиальных клеток обнажает субэндотелиальную матрицу и таким образом способствует образованию сначала локального пристеночного, а затем и окклюзирующего внутрисосудистого тромба [35].
Итак, представленные данные свидетельствуют о роли воспаления как детерминанты биологии, лежащей в основе осложнений атеросклероза. Установлена тесная взаимосвязь между показателями воспаления, тяжестью, распространенностью и осложнениями атеросклероза. В комплексе функционально-диагностических исследований, проводимых у больных ИБС, СРБ является высокочувствительным и легко доступным маркером локального воспаления атеросклеротической бляшки.
Источник
