Системные изменения организма при воспалении
Ответ
острой фазы – это комплекс последовательных
реакций, инициируемых физическими,
химическими, биологическими повреждающими
воздействиями или опухолевым процессом.
Принято
считать, что через 3-15
часов
после первичной альтерации на фоне
нейтрофилии повышается количество и
активность моноцитов, а затем и лимфоцитов
(возникает первичный иммунный ответ),
что и является началом ООФ, достигающего
максимума через 1-2
суток,
затем медленно ослабевающего и
заканчивающегося (в зависимости от
характера и выраженности как первичной,
так и вторичной альтерации) через 1-3
недели.
Субъективными
проявлениями ответа острой фазы являются:
сонливость, потеря аппетита (анорексия),
безразличие к окружающему (апатия), боли
в мышцах (миалгии), боли в суставах
(артралгии).
Объективные
проявления ответа острой фазы:
1.Изменения
со стороны крови:
1.1.нейтрофильный
лейкоцитоз с регенеративным сдвигом
влево
1.2.
увеличение СОЭ за счет снижения
поверхностного заряда эритроцитов,
который снижается из-за оседания
глобулинов и фибриногена на поверхности
эритроцитов, а также Н+
нейтрализуют отрицательный заряд
эритроцитов, происходит их агрегация,
снижение СОЭ.
1.3.Диспротеинемия:
гипоальбуминемия, гипергаммаглобулинемия,
появление в крови белков ответа острой
фазы (БОФ),
1.4.
снижение содержания железа (гипосидеремия),
цинка и увеличение концентрации меди
в сыворотке крови
1.5.
активация системы комплемента, активация
системы свертывания крови
2.лихорадка,
3.Развитие
общего адаптационного синдрома
4.активация
клеток иммунной системы
С биологических позиций ООФ следует
рассматривать как естественную
эволюционно сформированную реакцию
организма, цель которой заключается в
предотвращении тканевого повреждения,
изоляции и разрушении повреждающего
агента, а также в активации репаративных
процессов, необходимых для восстановления
нормальных жизненных функций. В ответ
на первичную альтерацию в развитии
воспалительного процесса наиболее
быстро (уже в течение 1-2 ч) активизируются
и эмигрируют из крови в очаг воспаления
нейтрофилы. Они осуществляют выраженное
местное защитное действие, проявляющееся
в пиноцитозе веществ, фагоцитозе
микроорганизмов, продуктов распада
тканей, токсинов, а также в высвобождении
и активации гидролаз, свободных радикалов
кислорода, перекисей, катионных белков
и других антимикробных и антитоксических
веществ. Через 3-15 ч после первичной
альтерации в очаге воспаления на фоне
нейтрофилии сначала повышается количество
и активность моноцитов, а затем и
лимфоцитов (раньше Т-, позже В-лимфоцитов),
т.е. возникает так называемый первичный
иммунный ответ. Фактически это и есть
начало ответа ООФ, достигающего максимума
через 1-2 сут, затем медленно ослабевающего
и заканчивающегося (в зависимости от
характера и выраженности как первичной,
так и вторичной альтерации) через 1-3
нед. Через выделение различных цитокинов
сначала нейтрофилы, а позже эндотелиоциты,
моноциты, гистиоциты, лимфоциты и
фибробласты начинают участвовать не
только в местных, но и в системных
реакциях, в том числе в активизации
различных звеньев и всей системы
иммунитета, а также гипофиза, надпочечников
и других различных как регуляторных,
так и исполнительных систем.
При
воспалении в крови изменяется содержание
белков ответа острой фазы (БОФ). Выделяют
две группы БОФ:
1) негативная
группа – концентрация БОФ снижается
(альбумин,трансферрин);
2) позитивная
группа – концентрация БОФ нарастает в
2-10 раз (альфа-1-антитрипсин, альфа-1-
антихимотрипсин, фибриноген, гаптаглобин);
менее чем в 2 раза (церулоплазмин, Сз
компонент комплемента, инактиватор
С1компонента
комплемента) и более, чем в 1000 раз (С –
реактивный белок (СРБ),сывороточный
амилоидный протеин А(САП-А)).
Белки
ООФ при остром экссудативно-деструктивном
воспалении (Д.Н.
Маянский, 2008)
Тип | Функции |
С1, | Опсонизация, |
Калликреин | Повышение |
Плазминоген | Активация |
С-реактивный | Регуляция |
Церулоплазмин | Нейтрализация |
а1-кислый | Регуляция |
а1- | Тормозит |
а | Тормозит |
а | Тормозит |
Гаптоглобин | |
Сывороточный |
СРБ
– наиболее популярен из всех БОФ, однако
интерпретация титров этого белка сложна,
так как его количество может не отражать
интенсивности воспалительного процесса.
В норме концентрация его составляет от
0,1 до 8,0 мг/л. Уровень СРБ достигает
максимума на 2-3-й день воспалительного
процесса и постепенно возвращается к
исходному значению на 12-15-е сутки.
При
затяжном и хроническом воспалении
содержание СРБ сохраняется на высоком
уровне.
К
наиболее чувствительным БОФ относятся
САП-А. Затем, по убыванию располагаются
СРБ, а-1-химотрипсин, церулоплазмин,
а-1-кислый гликопротеид. Определение
гаптаглобина или фибриногена
малоинформативно. При тяжелых формах
воспаления, особенно гепатитах, синтез
БОФ снижается. В этом случае их титр не
будет соответствовать активности
воспалительного процесса.
В
учебниках и руководствах по патологии
подробно рассматривается структурные,
метаболические и функциональные
изменения в очаге воспаления и мало
уделяется внимания на причины и патогенез
системных изменений.
Патогенез
системной реакции организма при
воспалении (по
Ю.С. Свердлову, 2000)
Повреждение
тканей (инфекция,
травма, распад опухоли, некроз, комплекс
антиген-антитело и др.)
Воспаление
(освобождение
ИЛ –
1, ИЛ
–
6, ИЛ
–
8, ФНО
-а, ИНФ-у)
Системные
реакции
Нервная
Эндокринная Печень
Костный
Активация
система система мозг лимфоцитов
(активация
Гипоталамус
Гипофиз БОФ Лейкоцитоз,
иммунитета)
ретикулоцитоз
Лихорадка
АКТГ
В
настоящее время принято считать, что
реализацию системных изменений в
организме при воспалении осуществляют:
интерлейкин-1, интерлейкин-6, интерлейкин-8,
фактор некроза опухолей, интерфероны,
фактор ингибирования лейкемии, онкостатин
М, цилиарный нейтрофический фактор,
трансформирующий фактор роста в, а так
же глюкокортикоиды.
В
настоящее время показано, что инсулин
действует как ингибитор цитокиновой
индукции некоторых БОФ.
Интерлейкин-1
представлен двумя полипептидами ИЛ-1-а
и ИЛ-1-в, последний у человека преобладает.
Стимуляторами выделения ИЛ-1 являются
компоненты клеточных стенок бактерий
(липополисахарид) и медиаторы воспаления,
выделяемые активированными клетками.
Больше всего ИЛ-1 вырабатывают макрофаги.
На всех клетках организма имеются
рецепторы к ИЛ-1, и это обуславливает
его разнообразные эффекты на организм.
Обладая снотворным действием, этот
цитокин вызывает снижение работоспособности,
гиподинамию; стимулирует продукцию
кортикотропина и кортикостероидов,
подавляет гипоталамическую секрецию
соматолиберина и стимулирует выработку
соматостатина, что вызывает ослабление
анаболизма, протеолиз и освобождение
аминокислот из скелетных мышц, усиление
секреции синовиальной жидкости и
резорбтивные изменения в костях и
хрящах, что проявляется костно-мышечно-суставными
болями, а также снижение продукции
инсулина.
Фактор
некроза опухолей, образуется в виде
двух фракций. ФНО-а (кахектин) вырабатывается
макрофагами, лимфоцитами, тучными
клетками и микроглией. ФНО-в (лимфокин)
образуется лимфоцитами. Кахектин
является мощным пирогеном, тормозит
активность центра голода и стимулирует
центр насыщения в гипоталамусе, что
ведет к потере веса, обладает сильным
контринсулярным эффектом, стимулирует
синтез белков острой фазы печени,
индуцирует апоптоз гепатоцитов и клеток
желудочно-кишечного тракта.
ФНО
и ИЛ-1 особенно токсичны при совместном
действии, они способны блокировать
мембранное пищеварение и перистальтику
кишечника, провоцировать рвоту, понос,
вызывать дисфункцию гепатоцитов,
гиперкалиемию и ацидоз, а при массированном
освобождении приводить к летальности,
способствуя развитию ДВС-синдрома. Они
стимулируют эндотелий к продукции
прокоагулянтов, окиси азота и
миокардиального депрессорного фактора,
который вызывает снижение сократимости
миокарда.
ИЛ-6
– важнейший индуктор синтеза белков
острой фазы. Мишенью его действия служат
гепатоциты, тимоциты и лимфоциты. Он
также стимулирует гемопоэз, вызывая
продукцию гранулоцитов, моноцитов,
тромбоцитов, эритроцитов.
ИЛ-8
– это семейство пептидов, которые
вырабатываются макрофагами и клетками
кожи по сигналу ИЛ-6. Он усиливает
хемотаксис и краевое стояние лейкоцитов,
стимулирует освобождение дефензинов
из нейтрофилов.
В
ряде случаев системных проявлений
острого воспалительного процесса может
не быть, хотя различные органы организма
реагируют на повреждение. Это наблюдается
при достаточно быстрой активизации
антимедиаторной системы.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
Воспаление (лат. inflammatio) – это сложный процесс реакции организма на внешний или внутренний повреждающий (болезненный) фактор. Воспаление направлено на устранение этого фактора, восстановление поврежденных тканей и защиту от развития заболеваний.
Таким образом, воспаление выполняет защитную функцию в организме, но только тогда, когда оно острое. Хроническое воспаление перестает быть физиологическим фактором и становится патогеном, ведущим к аутоиммунным заболеваниям и раку.
Воспаление – это естественный процесс, который происходит на определенных этапах. Без воспалительной реакции, которая активирует иммунную систему для борьбы с патогеном, например, вирусом, бактериями, травмированными участками, мы не смогли бы пережить даже самую маленькую инфекцию.
Сложность воспалительного процесса отражается в часто используемых терминах – состояние, процесс или воспалительная реакция.
Симптомы воспаления
Симптомы острого воспаления были впервые описаны римским ученым и энциклопедистом Аврелием Цельсом (25 г. до н.э. – 50 г. н.э.). в единственной работе «Медицина», которая сохранилась до наших дней, он описал четыре основных симптома острого воспаления, которые иногда называют тетрадой Цельса:
- боль (лат. dolor);
- повышенная температура (лат. calor);
- покраснение (лат. rubor);
- отек (лат. tumor).
Пятый признак воспаления – потеря функции и повреждение органов (лат. Functiolaesa) был добавлен немного позже, возможно, греческим врачом и философом Галеном (129-200 н.э).
Покраснение кожи является результатом увеличения кровотока в области, пораженной патогенными микроорганизмами, отек – это результат проникновения белка и клеток из сосудов в ткани – все это вызывает боль. Температура также является следствием увеличения кровотока. В свою очередь, «потеря функции» означает, что орган не функционирует должным образом.
В развитии воспалительной реакции участвуют многие физиологические механизмы, связанные как с клетками – гранулоцитами, моноцитами, тромбоцитами, лимфоцитами Т и В, тучными клетками, эндотелиальными клетками кровеносных сосудов, макрофагами, фибробластами, так и с веществами, выделяемыми ими – медиаторами воспаления. Со временем могут быть поражены целые органы и могут возникнуть системные симптомы – повышение температуры тела, потеря веса, мышечная атрофия, чувство общей слабости.
Воспаление при ларингите
Как возникает воспаление?
Чаще всего повреждающий фактор, который инициирует воспалительный процесс, приходит извне. Это может быть:
- физическое повреждение – химическое, тепло или холод, механическая травма;
- биологический агент – бактерии, вирус, чужеродный белок.
Также бывает, что причиной воспаления является процесс, происходящий внутри организма – эмболия артерии, сердечный приступ или развитие рака.
Изменения в кровеносных сосудах всегда являются корнем воспалительной реакции. Сосуды расширяются, и их проницаемость увеличивается. Это приводит к проникновению медиаторов и воспалительных клеток в окружающие ткани.
Составляющие воспаления
Острое воспаление выполняет важную защитную функцию – оно удаляет возбудителя и восстанавливает нормальную функцию органа. Переход острой фазы в хроническую фазу часто связан с потерей контроля организма над воспалительными механизмами и, следовательно, с функциональными нарушениями и даже повреждением пораженной ткани. Этот процесс можно сравнить с превращением острой боли (защитной функции) в хроническую боль, которая становится самой болезнью.
Патогенез воспалительного процесса
Воспалительная реакция неразрывно связана с иммунным ответом. Начинается с контакта патогена со специализированными клетками иммунной системы, так называемыми антигенпрезентирующие клетки. Когда клетки стимулируются, они продуцируют и высвобождают медиаторы воспаления, которые имеют решающее значение для инициации и поддержания воспалительного процесса.
Медиаторы оказывают про-и противовоспалительное действие на клетки-мишени, модулируя течение воспаления. Со временем адаптивная иммунная система (специфическая реакция) также участвует в борьбе с повреждающим фактором. Работа этой системы чрезвычайно точна – взаимодействие лимфоцитов Т и В приводит к выработке специфических антител, которые селективно нейтрализуют возбудителя.
Правильно функционирующая иммунная система эффективно распознает патогены и эффективно уничтожает их, не повреждая свои собственные клетки и ткани. Однако в определенных ситуациях иммунорегуляторные механизмы могут работать с дефектом – возникает воспалительная реакция на аутоантигены.
Это состояние встречается при многих аутоиммунных заболеваниях (диабет 1 типа, ревматоидный артрит, красная волчанка, целиакия, болезнь Хашимото).
Поделиться ссылкой:
Источник
Каждый, кто болел тяжелой ангиной или респираторной инфекцией, имеет представление о системных симптомах острого воспаления.
Комплекс системных изменений, сопровождающих острое воспаление, называют ответом острой фазы или синдромом системного воспалительного ответа.
Эти изменения связаны с реакциями цитокинов, продукция которых стимулируется бактериальными продуктами, такими как липополисахарид, и другими раздражителями воспаления.
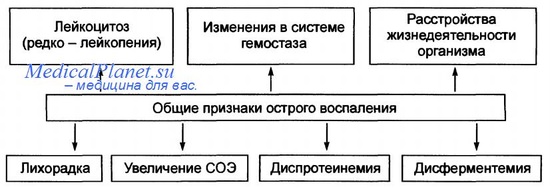
Ответ острой фазы включает несколько клинических и патологических изменений:
– лихорадка (повышение температуры тела на 1-4°С, одно из наиболее частых проявлений ответа острой фазы, особенно когда воспаление вызвано инфекцией) является ответом организма на действие особых веществ — пирогенов, которые путем стимулирования синтеза простагландинов действуют на клетки сосудов и периваскулярных пространств гипоталамуса.
Такие бактериальные продукты, как липополисахарид (экзогенный пироген), стимулируют высвобождение лейкоцитами цитокинов, например IL-1 и TNF (эндогенных пирогенов), что повышает уровни СОХ, конвертирующих арахидоновую кислоту в простагландины. В гипоталамусе простагландины, особенно PGE2, стимулируют образование нейротрансмиттеров, например циклического аденозинмонофосфата, функция которых заключается в регуляции температуры тела.
Нестероидные противовоспалительные средства, включая аспирин, снижают явления лихорадки путем ингибирования синтеза простагландинов. Было показано, что повышенная температура тела помогает амфибиям бороться с микробными инфекциями, и предполагают, что лихорадка имеет то же значение для млекопитающих, хотя ее механизм неясен. Одна из гипотез заключается в том, что повышение температуры тела может индуцировать белки теплового шока, усиливающие реакцию лимфоцитов на микробные агенты;
– белки острой фазы — это белки, синтезированные преимущественно в печени, концентрации которых в плазме крови могут повышаться в несколько сот раз при реакции на воспалительный стимул. Самые известные белки острой фазы: С-реактивный белок, фибриноген и сывороточный амилоид А. Синтез этих молекул гепатоцитами регулируют цитокины, особенно IL-6 (для С-реактивного белка и фибриногена) и IL-1 или TNF (для сывороточного амилоида А).
Многие белки острой фазы, например С-реактивный белок и сывороточный амилоид А, связываются со стенками микробных клеток, где могут выполнять функцию опсонинов и связывать компоненты системы комплемента. Они также связывают хроматин, возможно помогая в удалении ядер некротических клеток. Во время ответа острой фазы сывороточный амилоид А заменяет аполипопротеин А, компонент частиц липопротеинов высокой плотности (ЛПВП), что может нарушить передачу ЛПВП клетками печени макрофагам, которые могут использовать эти частицы как ресурс для продуцирующих энергию липидов. Фибриноген связывается с эритроцитами, и формируются «монетные столбики», которые быстрее выпадают в осадок, чем отдельные эритроциты.
Именно скорость оседания эритроцитов является основным показателем наличия системного воспалительного ответа, вызванного любым стимулом. Белки острой фазы оказывают благоприятные эффекты при остром воспалении, но длительная продукция этих белков (особенно сывороточного амилоида А) при хроническом воспалении приводит к развитию вторичного амилоидоза. Повышенные уровни С-реактивного белка в сыворотке крови предлагается использовать в качестве маркера повышенного риска развития инфаркта миокарда у пациентов с болезнью коронарных артерий, поскольку С-реактивный белок продуцируется при воспалении, а гипотетически воспаление в атеросклеротической бляшке коронарной артерии предрасполагает к тромбозу и последующему инфаркту. Другой пептид, продукция которого повышается во время ответа острой фазы, — железорегулирующий пептид гепсидин.
Постоянно повышенные концентрации гепсидина в плазме при хроническом воспалении снижают биодоступность железа и приводят к развитию анемии;
– лейкоцитоз — характерный признак воспалительных реакций, особенно индуцированных бактериальными инфекциями. Количество лейкоцитов обычно повышается до 15-20 тыс. клеток/мкл, но иногда может достигать необычайно высоких уровней — до 40-100 тыс. клеток/мкл. Такие экстремальные повышения называют лейкемоидной реакцией, поскольку подобный уровень лейкоцитов наблюдается при лейкемии. В таких случаях необходима дифференциальная диагностика.
Лейкоцитоз первично появляется в результате усиленного высвобождения клеток, вызванного цитокинами, включая TNF и IL-1, из постмитотического пула костного мозга. Таким образом, лейкоцитоз ассоциирован с увеличением количества преимущественно незрелых нейтрофилов в крови (сдвиг влево). Длительные инфекции тоже индуцируют пролиферацию кле-ток-предшественников в костном мозге, вызывая повышение продукции колониестимулирующего фактора. Следовательно, в костном мозге повышается продукция лейкоцитов для компенсации их потерь при воспалительной реакции. Большинство бактериальных инфекций приводят к абсолютному повышению в крови числа нейтрофилов (нейтрофилии).
Вирусные инфекции, например мононуклеоз, инфекционный паротит и краснуха, вызывают абсолютное повышение количества лимфоцитов (лимфоцитоз). При бронхиальной астме, аллергии и паразитарных инфекциях обнаруживается абсолютное повышение количества эозинофилов (эозинофилия). Ряд инфекций (брюшной тиф и инфекции, вызываемые определенными вирусами, риккетсиями и некоторыми простейшими) сопровождаются уменьшением количества лейкоцитов в крови (лейкопенией). Лейкопения также появляется при инфекциях, поражающих пациентов, ослабленных диссеминированной злокачественной опухолью, активным туберкулезом или тяжелым алкоголизмом;
– увеличение частоты сердечных сокращений, повышение артериального давления, снижение потоотделения (главным образом из-за перераспределения кровотока с поверхностных на глубокие кровеносные русла для минимизации теплопотерь через кожу), озноб, зябкость, анорексия, сонливость и недомогание, вероятно из-за воздействий цитокинов на клетки мозга;
– септический шок. При тяжелых бактериальных инфекциях (сепсисе) высокие концентрации микроорганизмов и липополисахаридов в крови или во внесосудистых тканях стимулируют продукцию некоторых цитокинов, особенно TNF, а также IL-12 и IL-1 в огромных количествах. В результате изменяется характер реакции организма и появляется триада клинических признаков септического шока: диссеминированная внутрисосудистая коагуляция, гипогликемия и гипотензивный шок.
– Рекомендуем ознакомиться со следующей статьей “Варианты воспалительной реакции и ее последствия”
Оглавление темы “Патофизиология”:
- Клетки участвующие в хроническом воспалении – макрофаги и другие клетки
- Причины и механизмы гранулематозного воспаления. Что такое гранулема?
- Влияние воспаления на организм в целом (системные симптомы воспаления)
- Варианты воспалительной реакции и ее последствия
- Пути заживления и обновления тканей – репарация, регенерация
- Регуляция деления и пролиферации клеток в тканях
- Виды стволовых клеток и их характеристика
- Эмбриональные стволовые клетки и их характеристика
- Индуцированные плюрипотентные стволовые клетки (ИПСК) и их характеристика
- Где присутствуют стволовые клетки у взрослых?
Источник
