Воспаление местные и общие признаки воспаления их механизмы развития
Билет
172. Местные и общие клинические проявления воспаления, их патогенез.
Местные (кардиальные) признаки воспаления
Жар
(calor)– связан с притоком теплой
артериальной крови в очаг воспаления,
изменение обмена веществ в самом очаге
воспаления, в связи с повреждением
мембраны разобщается окислительно
фосфорилировани и преобладание
катаболических реакций.Краснота
(rubor)– гиперемия как артериальная
так и венозная. При артериальной – с
красным оттенком, при венозной –
синюшный.
Она связано с расширением артериол,
развитием артериальной гиперемии и
“артериализацией” венозной крови в
очаге воспаления.Отек,
припухлость (tumor)– повышение
гидростатического давления в сосудах;
повышение проницаемости сосудистой
стенки под действием медиаторов и
кислых окислителей; рост коллидо-осмотического
давления; выход лейкоцитов под действием
хемоаттрактанта.Боль
(dolor)– обусловлена действием
медиаторов, медиаторы разделяются на:
альгогенные (сами вызывают боль, действуя
на болевые рецепторы; например:
брадикинин, гистамин, серотонин, кислые
продукты обмена, внеклеточный калий)
и гиперальгического действия (это
простагландины, повышают чувствительность
болевых рецепторов). Боль обусловливает
сдавление нервных окончаний экссудатом.Нарушение
функции (functio laesa).Общие признаки воспаления
ПРИЗНАК
ПАТОГЕНЕЗ
Интоксикация
Токсины
микроорганизмов, продукты альтерации,
продукты нарушенного метаболизма
Лихорадка
Пирогены:
ИЛ-1, ФНО, ИЛ-6, интерферон
Лейкоцитоз,
активация фагоцитоза
Лейкотриены,
ИЛ-1, ИЛ-6, ИЛ-8
Активация
иммунитета
Активация
макрофагов, реакции клеточной
кооперации, антителообразования
Увеличение
СОЭ
Увеличение
концентрации белков «острой фазы»
и иммуноглобулинов
Увеличение
продукции интерферона
Активация
макрофагов и Т-лимфоцитов
Гломерулонефрит
– поражение клубочкового аппарата.Это
группа заболеваний, которая характеризуется
диффузным поражением почечной ткани,
воспалительного и/или иммунопатологического
генеза с вовлечением в патологический
процесс всех отделов нефронов
(преимущественно клубочков), а также
интерстициальной ткани и сосудов почек.Острый гломерулонефрит
Этиология
I.НАСЛЕДСТВЕННЫЙ
II.ТОКСИЧЕСКИЙ
III.ИММУНОПАТОЛОГИЧЕСКИЙ
ДЕЙСТВИЕ
ИММУННЫХ КОМПЛЕКСОВ (ГЕТЕРОЛОГИЧНЫХ
И АУТОЛОГИЧНЫХ)ДЕЙСТВИЕ
АНТИПОЧЕЧНЫХ АУТОАНТИТЕЛ
Патогенез иммунопатологического гломерулонефрита
I.
МЕХАНИЗМЫ ИММУНОПАТОЛОГИЧЕСКИХ
РЕАКЦИЙ
ВОЗНИКНОВЕНИЕ
ПОСЛЕ ИНФЕКЦИОННОГО ПРОЦЕССА В
ОРГАНИЗМЕ (-ГЕМОЛИТИЧЕСКИЙ
СТРЕПТОКОКК А, СТАФИЛОКОКК, ПНЕВМОКОКК,
ВИРУСЫ, ПЛАЗМОДИЙ МАЛЯРИИ)СИЛЬНОЕ
ПЕРЕОХЛАЖДЕНИЕ, ВАКЦИНАЦИЯОБРАЗОВАНИЕ
АНТИТЕЛ К АНТИГЕНАМ БАЗАЛЬНОЙ
МЕМБРАНЫ КЛУБОЧКОВ (5%)ФИКСАЦИЯ
КОМПЛЕКСОВ АНТИГЕН-АНТИТЕЛО НА
БАЗАЛЬНОЙ МЕМБРАНЕ КЛУБОЧКОВ (80%)ФИКСАЦИЯ
КОМПЛЕМЕНТА НА БАЗАЛЬНОЙ МЕМБРАНЕ
КЛУБОЧКОВ (5%)
II.ВОСПАЛЕНИЕ КЛУБОЧКОВ
ПОВЫШЕНИЕ
ПРОНИЦАЕМОСТИ КАПИЛЛЯРОВТРОМБОЗ
КАПИЛЛЯРОВНЕКРОЗ
КАПИЛЛЯРОВ И АРТЕРИОЛСДАВЛЕНИЕ
КЛУБОЧКОВСКЛЕРОЗ,
ГИАЛИНОЗ КЛУБОЧКОВАТРОФИЯ
КАНАЛЬЦЕВ
II
А.ГИПОПЕРФУЗИЯ КЛУБОЧКОВ
СНИЖЕНИЕ
ФИЛЬТРАЦИИ (ОЛИГО-, АНУРИЯ)СТИМУЛЯЦИЯ
ЮГА (НИКТУРИЯ)АКТИВАЦИЯ
АНГИОТЕНЗИН-АЛЬДОСТЕРОНОВОЙ СИСТЕМЫ
(АРТЕРИАЛЬНАЯ ГИПЕРТОНИЯ)ГИПЕРНАТРИЕМИЯ,
ГИПЕРВОЛЕМИЯ (ГИПЕРГИДРАТАЦИЯ,
АРТЕРИАЛЬНАЯ ГИПЕРТЕНЗИЯ, ГИПЕРТРОФИЯ
ЛЕВОГО ЖЕЛУДОЧКА, РЕТИНОПАТИЯ –
НАРУШЕНИЕ ЗРЕНИЯ)ПРОГРЕССИРУЮЩАЯ
ИШЕМИЯ ПОЧЕКВЫДЕЛИТЕЛЬНЫЙ
МЕТАБОЛИЧЕСКИЙ АЦИДОЗГИПЕРАЗОТЕМИЯ,
УРЕМИЯ
II
В.ПОВЫШЕНИЕ ПРОНИЦАЕМОСТИ КАПИЛЛЯРОВ
КЛУБОЧКОВ
АЛЬБУМИНУРИЯ
В ПРЕДЕЛАХ
1-3
г/сут
ГЕМАТУРИЯ
ГИПО-,
ДИСПРОТЕИНЕМИЯ (ГИПООНКИЯ)ЦИЛИНДРУРИЯ
ЛЕЙКОЦИТУРИЯ
Проявления:
Ренальные
(мочевой синдром):
Ишемия
клубочков – нарушается их фильтрационная
способность
снижение клиренса эндогенного креатинина,
олиго- анурия, никтурия.Повышение
проницаемости мембран клубочков
гематурия, протеинурия (ведет к
цилиндрурии), лейкоцитурия.
Экстраренальные
проявления:
отечный
синдром (на лице, под глазами, по утрам,
в рыхлой клетчатке).Гипотензивный
синдром – в основе активация РААС.Нефросклероз
– Уменьшение выработки вазодепрессоров
– ренопривная артерильная гипертензия.Анемический
синдром (анемия брайтика) – вследствие
уменьшения продукции эритропоэтина.
Билет
182. Причины, механизмы развития, изменения газового состава артериальной и венозной крови при экзогенной, дыхательной, сердечно-сосудистой, кровяной и тканевой гипоксии. Смешанная гипоксия.
Гипоксия– состояние, возникающее в результате
недостаточного обеспечения тканей
организма кислородом и /или нарушения
его усвоения в ходе биологического
окисления.Гипоксия
– типовой патологические процесс,
развивающийся в результате недостаточности
биологического окисления, приводящий
к нарушению энергетического обеспечения
функций и пластических процессов в
организме.Гипоксемия
– снижение, по сравнению с должным,
уровней напряжения и содержания
кислорода крови.Типы
гипоксии по этиологии:
Экзогенная
– снижение кислорода в окружающем
воздухе. Может быть гипобарической
снижение атмосферного давления и
снижение рО2
(высотная болезнь и горная болезнь).
Горная болезнь развивается в разных
горах на разной высоте: на Кавказе,
Альпах развитие горной болезни будет
определяться 3 тысячами. Факторы,
влияющие на возникновение горной
болезни: ветер, солнечная радиация,
влажность воздуха, наличие снега,
высокий перепад ночных и дневных
температур + индивидуальная
чувствительность: пол, возраст, тип
конституции, тренированность, прошлый
высотный опыт, физическое и психическое
состояние. Тяжелая физическая работа.
Скорость набора высоты:
Нормобарическая;
Гипобарическая;
Эндогенная:
Дыхательная;
Циркуляторная;
Гемическая;
Тканевая
(гистотоксическая);Смешанная.
Местная
(регионарная):
Циркуляторная;
Тканевая
(гистотоксическая);Смешанная.
Нормобарическая
гипоксия развивается при нормальном
атмосферном давлении:
Замкнутое
или плохо вентилируемое пространство;Гиповентиляция
при ИВЛ.
Критерии
экзогенной гипоксии:
Снижение
Нb O2
(артериальной крови) – артериальная
гипоксемия;Снижение
раСО2
(гипокапния) – при гипобарической
гипоксии;Повышение
раСО2
(гиперкапния) в замкнутом пространстве.
Эндогенная
Дыхательная
гипоксия – нарушение вентиляции,
диффузии, перфузии – дыхательная
недостаточность.Критерии
дыхательной гипоксии: артериальная
гипоксемия, раСО2в норме
или гиперкапния.Циркуляторная
гипоксия:
Сердечная
недостаточность – снижение скорости
кровотока, увеличение времени контакта
крови с окружающими тканями, у пациента
венозная гипоксемия, а также увеличение
артериовенозной разницы по кислороду;Сосудистая
недостаточность – снижение скорости
кровотока, увеличение времени контакта
крови с окружающими тканями, у пациента
венозная гипоксемия, а также увеличение
артериовенозной разницы по кислороду;Сердечно-сосудистая
недостаточность.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
Воспаление
– типовой патологический процесс,
возникающий на воздействие патогенных
факторов, проявляется альтерацией,
экссудацией и пролиферацией.
Этиология
воспаления:
1)Экзогенные
факторы
-инфекционные
(бактерии, вирусы, простейшие, грибы)
-неинфекционные
(физические, химические, биологические)
2)Эндогенные
факторы
-продукты
тканевого распада (очаги некроза, распад
тканей, гематомы, тромбы)
-мочевая
кислота и её соли
-УПМ
-иммунные
комплексы Аг-Ат.
Местные
признаки воспаления:
-покраснение
связано с развитием артериальной
гиперемии в очаге воспаления.
-жар
обусловлен увеличением притока тёплой
крови, активацией метаболизма, разобщением
процессов биологического окисления.
-отёк
вследствие развития экссудации и отека,
набухания тканевых элементов, увеличение
суммарного диаметра сосудистого русла
в очаге воспаления.
-боль
в рез-те раздражения нервных окончаний
различными БАВ, сдвига активной реакции
среды в кислую сторону, повышение
осмотического давления и механического
растяжения или сдавления тканей.
-нарушение
функции воспалённого органа связано с
расстройством его нейроэндокринной
регуляции, развитием боли, структурными
повреждениями.
Общие
признаки воспаления:
-лейкоцитоз
– увеличение количества лейкоцитов.
Изменение лейкоцитарной формулы чаще
в виде увеличения % содержания нейтрофилов,
в т.ч. п/я и юных, т.е. ядерного сдвига
влево.
-лихорадка
под влиянием поступающих из очага
воспаления пирогенных факторов. (ИЛ-8,1,6
и ФНО).
-увеличение
в крови содержания альфа и гамма-глобулинов.
-изменение
ферментного состава крови выражается
в увеличении активности трансаминазы.
-увеличение
СОЭ.
-симптомы
интоксикации.
Всякое
повреждение сопровождается нарушением
гомеостаза, вызывает наряду с местными
воспалительными реакциями ряд сложных
системных реакций, обуславливающих
вовлечение важнейших защитных и
регуляторных систем организма. Эти
реакции получили название ООФ.
Проявления
ООФ: лихорадка, анорексия, миалгия,
артралгия, гипергаммаглобулинемия,
гипоальбуминемия, появление в крови
белков острой фазы, повышение СОЭ,
нейтрофильный лейкоцитоз, активация
клеток ИС.
Системные
реакции организма (ООФ) обусловлены
появлением в организме медиаторов. Эти
медиаторы секретируются клетками,
участвующими в воспалительном ответе,
развивающемся в месте первичного
повреждения, моноцитами, макрофагами,
нейтрофилами.
Медиаторы
попадают в кровоток и воздействуют на
клетки мишени, имеющие на своей поверхности
соответствующие рецепторы. Такие клетки
имеются на поверхности всех клеток
органов.
К
числу важнейших медиаторов ООФ относятся
ИЛ-1,6, ФНО-альфа.
20 вопрос.
Альтерация, ее виды и значение. Изменения
обмена веществ, физико-химических
свойств тканей и их структуры в очаге
воспаления. Медиаторы воспаления. Их
происхождение и действие на органы и
ткани.
Альтерация или
дистрофия, повреждение ткани, нарушение
в ней питания (трофики) и обмена веществ,
ее структуры и функции. Различают
первичную и вторичную альтерацию.
Первичная
альтерация является
результатом повреждающего воздействия
самого воспалительного агента, поэтому
ее выраженность при прочих равных
условиях (реактивность организма,
локализация) зависит от свойств флогогена.
Вторичная
альтерация является
следствием воздействия на соединительную
ткань, микрососуды и кровь высвободившихся
внеклеточно лизосомальных ферментов
и активных метаболитов кислорода.
Вторичная
альтерация не зависит от воспалительного
агента, для ее развития необязательно
дальнейшее присутствие флогогена в
очаге. Она является реакцией организма
на уже вызванное вредным началом
повреждение. Это целесообразный и
необходимый компонент воспаления как
защитно-приспособительной реакции,
направленный на скорейшее отграничение
(локализацию) флогогена и (или) поврежденной
под его воздействием ткани от остального
организма. Ценой повреждения достигаются
и другие важные защитные явления: более
выраженный микробицидный и литический
эффект лизосомальных ферментов и
активных метаболитов кислорода, поскольку
он осуществляется не только в фагоцитах,
но и внеклеточно; вовлечение других
медиаторов воспаления и клеток, усиленная
экссудация, эмиграция и фагоцитоз. В
результате воспалительный процесс
завершается быстрее. Однако альтерация
целесообразна лишь в известных пределах.
Так, например, при дисбалансе в системе
лизосомальные протеиназы –
их
ингибиторы возникают избыточные
проявления альтерации с преобладанием
некроза.
Альтеративные
явления при воспалении включают тканевой
распад и усиленный
обмен веществ
(«пожар обмена»), приводящие к ряду
физико-химических изменений в воспаленной
ткани: накоплению кислых
продуктов (ацидоз, или Н+-гипериония), увеличению
осмотического давления (осмотическая
гипертензия, или гиперосмия), повышению
коллоидно-осмотического, или онкотического,
давления (гиперонкия).
В
зависимости от силы повреждающего
агента, интенсивности и локализации
воспаления морфологические проявления
альтерации широко варьируют: от едва
заметных структурно-функциональных
изменений до полной деструкции(некробиоз) и
гибели (некроз) тканей
и клеток. Обнаруживаются мутное набухание
цитоплазмы клеток, явления белковой,
жировой и других видов их дистрофии.
Резко повышается проницаемость мембран
клеток и клеточных органелл. Изменяются
и субклеточные структуры – митохондрии,
лизосомы, рибосомы, эндоплазматическая
сеть. Митохондрии набухают или
сморщиваются, кристы их разрушаются.
Повышение проницаемости и повреждение
мембран лизосом сопровождаются выходом
разнообразных ферментов, играющих роль
в разрушении субклеточных структур.
Изменяются форма и величина цистерн
эндоплазматического ретикулума, в
цитоплазме появляются везикулы,
концентрические структуры и др. Отмечаются
краевое расположение хроматина,
повреждение мембраны ядра. В строме
наблюдаются мукоидное и фибриноидное
набухание вплоть до некроза, растворение
коллагеновых и эластических волокон.
Повышение
обмена веществ при воспалении происходит
преимущественно за счет углеводов.
Первоначально усиливается как их
окисление, так и гликолиз. В основе этого
явления лежит активация соответствующих
тканевых ферментов. Заметно увеличивается
потребление кислорода воспаленной
тканью. По мере накопления в очаге
лейкоцитов, лизосомальные ферменты
которых расщепляют углеводы анаэробным
путем, а также повреждения и снижения
количества митохондрий в ходе альтерации,
реакции окисления заметно ослабевают,
а гликолиза – нарастают. Соответственно
расщепление углеводов не всегда доходит
до конечных продуктов – углекислого
газа и воды. Дыхательный коэффициент
снижается. В ткани накапливаются
недоокисленные продукты углеводного
обмена – молочная и трикарбоновые
кислоты.
Кроме
того, вследствие нарушения обмена жиров,
белков и распада нуклеиновых кислот в
очаге нарастает содержание жирных
кислот, кетоновых тел, полипептидов,
аминокислот, нуклеотидов (АТФ, адениловая
кислота), нуклеозидов (аденозин). В
результате развивается ацидоз.
Первоначально он компенсируется
тканевыми буферными системами и
ускоренным крово- и лимфотоком. По мере
истощения буферных систем и замедления
крово- и лимфотока ацидоз нарастает и
становится некомпенсированным. Если в
норме концентрация водородных ионов в
ткани составляет 0,5?10-7,
т.е. рН равен 7,34, то при воспалении может
быть, соответственно, 25?10-7 и
5,6 и ниже. Чем острее протекает
воспалительный процесс, тем более
выражен ацидоз. Так, при остром гнойном
воспалении рН составляет 6,5-5,39, а при
хроническом – 7,1-6,6. Ацидоз принимает
участие в повышении проницаемости
сосудов. Он создает благоприятные
условия для реализации разрушительных
эффектов лизосомальных ферментов, в
частности гликозидаз, расщепляющих
углеводные компоненты матрикса
соединительной ткани.
Наряду
с Н+-гиперионией в очаге нарастает
содержание и других ионов – ионов калия,
натрия, кальция. Это обусловлено
разрушением клеток и усиленной
диссоциацией в кислой среде солей.
Вследствие опережающего повышения
уровня внеклеточного калия нарушается
соотношение ионов калия и
кальция (дизиония). Изменения
в гомеостазе ионов Са2+
могут лежать в основе гибели клеток в
очаге воспаления. Са2+
является одним из вторичных мессенджеров
между мембраной и клеточными ферментными
системами, а также генным аппаратом.
Повышение уровня внутриклеточного Са2+
приводит к абсорбции его митохондриальными
мембранами и последующим блокированием
дыхательной цепи электронов. Повышенное
внутриклеточное содержание Са2+
активирует нелизосомальные протеазы,
приводя к лизису цитоскелета, деградации
энзимов, мембрано-ассоциированных
белков (ионных каналов, переносчиков,
рецепторов, молекул адгезии). Отмечено,
что хотя снижение внеклеточного Са2+
важно для выживания клеток, это может
быть препятствием к их новому росту. В
очаге воспаления нарастает молекулярная
концентрация, поскольку в процессе
тканевого распада и усиленного обмена
веществ происходит расщепление крупных
молекул до множества мелких. Вследствие
повышения ионной и молекулярной
концентрации развивается гиперосмия.
Так, если в норме депрессия межклеточной
жидкости
составляет
0,62°, т.е. осмотическое давление равно 8
атм, то при гнойном воспалении –
соответственно 0,80° и 19 атм (рис. 10-4).
В
результате физико-химических изменений
воспаленной ткани, расщепления белков
до полипептидов и аминокислот с
увеличением концентрации последних
происходит увеличение дисперсности
коллоидов, их способности притягивать
и задерживать воду. Развивается
гиперонкия. Изменения осмотического и
онкотического давления являются важным
фактором экссудации и, соответственно,
воспалительного отека.
Медиаторы
воспаления




Эффект
медиатора может быть добавочным
(аддитивным), потенцирующим (синергистическим)
и ослабляющим (антагонистическим), а
взаимодействие медиаторов возможно на
уровне их синтеза, секреции или эффектов.
Медиаторное звено является основным в
патогенезе воспаления. Оно координирует
взаимодействие множества клеток –
эффекторов воспаления, смену клеточных
фаз в очаге воспаления.
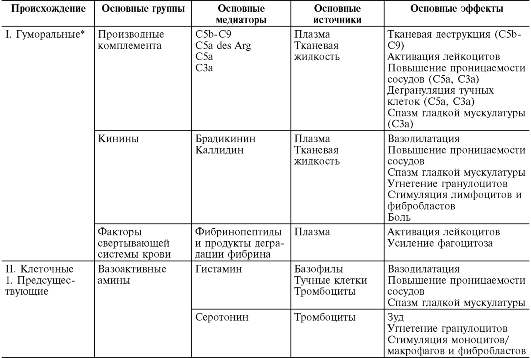
Медиаторы воспаления
по происхождению делятся
на гуморальные (образующиеся
в жидких средах – плазме крови и тканевой
жидкости) и клеточные. Все гуморальные
медиаторы являются предсуществующими, т.е.
имеются в виде предшественников до
активации последних; к ним относятся
производные комплемента, кинины и
факторы свертывающей системы крови. Среди
клеточных медиаторов выделяют
предсуществующие (депонированные
в клетках в неактивном состоянии) –
вазоактивные амины, лизосомальные
ферменты, нейропептиды, и вновь
образующиеся (т.е.
продуцируемые клетками при стимуляции)
– эйкозаноиды, цитокины, лимфокины,
активные метаболиты кислорода.
Основными
источниками клеточных медиаторов
являются:
1. Нейтрофилы, которые
выделяют катионные белки, стимулируют
высвобождение биогенных аминов из
тромбоцитов и тучных клеток, содержат
ингибитор высвобождения гистамина и
гистаминазу. Протеазы нейтрофилов
участвуют в образовании кининов и
активных фрагментов комплемента (С3а,
С3Ь). Нейтрофилы образуют простагландин
(PG) E2 и
другие эйкозаноиды. Ферменты нейтрофилов
активируют как свертывание крови, так
и фибринолиз.
2. Макрофаги выделяют
ангиотензин-конвертазу, которая
инактивирует брадикинин, превращает
ангиотензин-I в ангиотензин-П. Они
синтезируют PGE2,
а также тромбоксаны и лей-
котриены
(LT). Поскольку PGE2 препятствует
высвобождению клеточных медиаторов
воспаления и подавляет агрегацию
тромбоцитов, макрофаги, помимо
провоспалительной, обладают и
противовоспалительной функцией.
Макрофаги синтезируют различные
компоненты комплемента, обладают
свертывающей и фибринолитической
активностью.
3. Эозинофилы служат
отрицательными модуляторами воспаления.
Они содержат гистаминазу, кининазу,
ферменты, расщепляющие лейкотриены С
и D (лизофосфалипазу, арилсульфатазу В,
фосфолипазу D), главный щелочной белок,
осуществляющий цитотоксическую функцию
и нейтрализующий гепарин.
4. Тучные
клетки и базофилы выделяют
гистамин и серотонин, гепарин, факторы
хемотаксиса нейтрофилов и эозинофилов,
фактор активации тромбоцитов,
протеолитические ферменты, они продуцируют
пероксидазу, супероксид и пероксид
водорода, а также протеазу, превращающую
кининоген в кинин.
5. Тромбоциты секретируют
факторы роста и свертывания, вазоактивные
амины и липиды, нейтральные и кислые
гидролазы.
Производные
комплемента
являются наиболее важными из гуморальных
медиаторов воспаления.
Кинины –
вазоактивные пептиды, образующиеся из
кининогенов (а2-глобулинов)
под влиянием калликреинов в плазме
(брадикинин) и в тканевой жидкости
(каллидин). Пусковым фактором активации
калликреин-кининовой системы является
активация при повреждении ткани фактора
Хагемана (XII), превращающего прекалликреины
в калликреины
Эйкозаноиды являются
важным медиаторным звеном воспалительной
реакции, о чем свидетельствуют их
продолжительная продукция в очаге и
тесная связь с ключевым событием
воспаления – лейкоцитарной инфильтрацией,
а также мощный противовоспалительный
эффект ингибиторов их синтеза.
Преобладающими эйкозаноидами в очаге
воспаления
оказываются простагландины (PGE2), лейкотриены(LTB4)
и 5-гидропероксиэйкозатетраеновая
кислота (5-HPETE).
Простагландины сами
не повышают сосудистую проницаемость,
но, будучи сильными вазодилататорами,
усиливают гиперемию и, следовательно,
экссудацию.
Лейкотриены (синтезируются
во всех клетках крови, кроме эритроцитов,
а также в адвентиции сосудов, тучных
клетках, легких) способствуют сокращению
гладкой мускулатуры желудочнокишечного
тракта, оказывают сосудосуживающее
действие (в том числе коронарных артерий.
Тромбоксаны (образуются
в ткани мозга, селезенки, легких и в
тромбоцитах, клетках воспалительной
гранулемы) вызывают адгезию и агрегацию
тромбоцитов, способствуют развитию
тромбоза при ишемической болезни сердца,
оказывают вазоспастическое действие.
Биогенные
амины – гистамин и серотонин считаются
основными медиаторами первоначальных
микроциркуляторных нарушений в очаге
острого воспаления и немедленной фазы
повышения проницаемости сосудов.
Незначительное
количество нейромедиатора серотонина содержится
в тучных и энтерохромаффинных клетках,
но главным его источником являются
тромбоциты.
Гистамин действует
двояко в отношении сосудов и клеток.
Через Н1-рецепторы
он расширяет артериолы и угнетает
эмиграцию и дегрануляцию лейкоцитов,
а через H1-рецепторы
суживает венулы, повышая таким образом
внутрикапиллярное давление, и стимулирует
эмиграцию и дегрануляцию лейкоцитов.
Лизосомальные
ферменты высвобождаются
в очаге воспаления из гранулоцитов и
моноцитов-макрофагов в ходе их
хемотаксической стимуляции, миграции,
фагоцитоза, повреждения, гибели.
Неферментные
кат ионные белки, содержащиеся
в азурофильных и в специфических гранулах
нейтрофилов, обладают таким важным
свойством, как высокая микробицидность.
Цитокины при
воспалении продуцируются главным
образом стимулированными моноцитами
и макрофагами (монокины), а также
нейтрофилами, лимфоцитами, эндотелиальными
и другими клетками. Цитокины повышают
сосудистую проницаемость (нейтрофилзависимым
путем), адгезию и эмиграцию лейкоцитов.
К
медиаторам воспаления (цитокинам)
относится также ряд лимфокинов –
полипептидов, продуцируемых стимулированными
лимфоцитами. Лимфокины координируют
взаимодействие нейтрофилов, макрофагов
и лимфоцитов, регулируя воспалительную
реакцию в целом.
Активные
метаболиты кислорода, прежде
всего свободные радикалы – супероксидный
анион-радикал (О*-)
, гидроксильный радикал (НО*), гидроперекисный
радикал (НО*,), вследствие наличия на их
внешней орбите одного или нескольких
непарных электронов обладают повышенной
реактивностью с другими молекулами и,
следовательно, значительным деструктивным
потенциалом, который имеет значение в
патогенезе воспаления.
К
медиаторам и модуляторам воспаления
относят также нейропептиды –
вещества, высвобождаемые С-волокнами
в результате активации воспалительным
агентом полимодальных ноцицепторов,
играющих важную роль в возникновении
аксон-рефлексов в конечных разветвлениях
первичных афферентных (чувствительных)
нейронов. Наиболее изученными являются
вещество Р, кальцитонин-генсвязанный
пептид, нейрокинин А. Кроме вышеперечисленных
веществ, к медиаторам воспаления
относятся также ацетилхолин
и катехоламины,высвобождающиеся
при возбуждении холин- и адренергических
структур. Ацетилхолин вызывает расширение
сосудов и играет роль в аксон-рефлекторном
механизме артериальной гиперемии при
воспалении. Норадреналин и адреналин
тормозят рост сосудистой проницаемости,
выступая главным образом как модуляторы
воспаления.
Соседние файлы в предмете Патологическая физиология
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
