Воспаление вилочковой железы фото
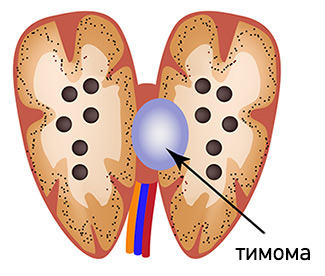
Тимома – это общее название для группы опухолей вилочковой железы (тимуса). Чаще всего они носят доброкачественный характер. На долю злокачественных опухолей приходится около 30% тимом. Выраженность клинической картины может быть самой разной, от бессимптомного течения до выраженной миастении и симптомов компрессии органов средостения.
Вилочковая железа частично находится в нижней части шеи, частично – в верхней части средостения. В органе выделяют два типа тканей – эпителиальную (железистую), которая отвечает за синтез тимических гормонов, и лимфоидную, которая представлена Т-лимфоцитами различной степени зрелости.
Таким образом, тимус является уникальным органом, который с одной стороны является железой внутренней секреции, а с другой – органом иммунной системы. В норме вилочковая железа проявляет активность в детском возрасте, играет роль депо Т-лимфоцитов и координирует работу эндокринной и иммунной систем. По мере взросления, тимус замещается жировой тканью. И у людей старше 50 лет сохраняется только 10% активных клеток.
Причины возникновения тимомы
Причины возникновения тимомы неизвестны. Предполагается, что в этом процессе могут принимать участие следующие факторы:
- Нарушения в эмбриональном периоде развития.
- Нарушение синтеза тимопоэтина.
- Нарушение иммунных механизмов.
- Инфекционные заболевания.
- Воздействие ионизирующего излучения.
- Травматические повреждения органов средостения.
- Некоторые аутоиммунные и эндокринные патологии: синдром Иценко-Кушинга, диффузный токсический зоб, миастения и др.
Виды тимомы
Единой классификации тимом на сегодняшний день нет, ввиду большого разнообразия опухолей, развивающихся в вилочковой железе. В 1999 году ВОЗ предложила морфологическую классификацию, в основе которой лежит соотношение лимфоцитарных и эпителиальных клеток. По этой классификации выделяют 6 видов опухоли:
- Тимома типа А – опухолевая ткань представлена дифференцированными клетками без признаков атипии, практически всегда отграничена от окружающих тканей капсулой. Клетки веретенообразные или овальные. Это благоприятный, доброкачественный вариант тимомы, 15-летняя выживаемость при которой составляет 100%.
- Тимома типа АВ морфологически схожа с типом А, но имеются единичные очаги патологических лимфоцитов.
- Тимома типа В – в опухолевой ткани преобладают дендритные и эпителиоидные клетки. Тип В будет разделяться в зависимости от соотношения эпителиальных и лимфоидных клеток, а также от выраженности их атипизма.
- Тимома типа В1 (преимущественно кортикальный тип). По структуре напоминает кортикальный слой вилочковой железы, очаговыми вкраплениями медуллярных клеток.
- Тимома типа В2 (кортикальный тип). В ткани опухоли имеются эпителиальные клетки с признаками атипии и везикулами в ядре.
- Тимома типа В 3 (эпителиальный тип). Опухоль представлена атипичными эпителиальными клетками. Некоторые авторы расценивают ее как высокодифференцированный рак вилочковой железы.
- Тимома типа С – рак тимуса. Представлен разнообразными гистологическими типами рака – светлоклеточный, плоскоклеточный, веретеноклеточный и др. Склонен к агрессивному течению, прорастает в соседние органы, дает метастазы в печень, кости и лимфатические узлы.
Тимомы типа А, АВ и В1 относят к доброкачественным новообразованиям тимуса, тип В2 и В3 – это злокачественные тимомы с относительно благоприятным течением, когда при своевременном обращении возможно полное излечение и 20-летняя продолжительность жизни составляет 40-60%. Тип С называют карциномой тимуса 2-го типа. Как мы уже говорили, это агрессивная опухоль, склонная к быстрому росту и метастазированию.
Стадии тимомы
Для характеристики распространения тимомы применяется классификация Masaoka-Koga. В ее основу положена оценка вовлеченности тканей и органов средостения, а также наличие лимфогенных и гематогенных метастазов.
- 1-2 стадия тимомы – опухоль прорастает за пределы своей капсулы, затрагивает плевру и клетчатку средостения.
- 3 стадия тимомы – опухоль прорастает в перикард, затрагивает легкое или магистральные сосуды, находящиеся в средостении.
- 4А стадия – имеется опухолевая диссеминация по плевре или перикарду.
- 4В стадия – имеются лимфогенные или гематогенные метастазы.
Диагностика тимомы
Заподозрить наличие опухоли можно по характерным клиническим симптомам, после чего пациент направляется на диагностические исследования. Рентген грудной клетки является неспецифическим методом диагностики и позволяет только увидеть расширение тени средостения.
 Компьютерная томография с контрастированием – более информативный метод. Он позволяет получить информацию о наличии новообразования, определить его злокачественность, и даже дифференцировать его природу – отличить тимому от лимфомы и др. МРТ не является рутинным методом диагностики тимом, но может использоваться по показаниям, например, при наличии у пациента аллергии на йодсодержащий контраст, применяемый при КТ.
Компьютерная томография с контрастированием – более информативный метод. Он позволяет получить информацию о наличии новообразования, определить его злокачественность, и даже дифференцировать его природу – отличить тимому от лимфомы и др. МРТ не является рутинным методом диагностики тимом, но может использоваться по показаниям, например, при наличии у пациента аллергии на йодсодержащий контраст, применяемый при КТ.
Окончательный диагноз выставляется после морфологического изучения опухолевой ткани. Как правило, ее получают после радикальной операции. Если это невозможно, рассматривают вариант проведения биопсии. Для этого может использоваться толстоигольная или хирургическая биопсия, которая проводится во время лапароскопических операций. Морфологическая верификация необходима для подбора оптимального метода лечения.
Симптомы злокачественного новообразования вилочковой железы
Какое-то время злокачественная опухоль вилочковой железы может протекать бессимптомно. На данном этапе обнаруживается случайно, при проведении обзорной рентгенографии грудной клетки или флюорографии. По мере развития процесса, будет возникать и нарастать неспецифическая симптоматика, которая связана с локальным воздействием опухоли на органы груди и средостения:
- Кашель.
- Боль в области груди.
- Одышка. Она может быть результатом компрессии органов дыхания, или миастенического синдрома, при котором наблюдается слабость мышц из-за нарушений нейромышечных связей.
- Синдром верхней полой вены – нарушение венозного оттока от головы и плечевого пояса из-за компрессии верхней полой вены. Проявляется цианозом кожи и отечностью верхней половины тела, а также расширением вен.
- Нарушение иммунной системы. Тимус является органом, в котором проходят определенные стадии своего развития Т-лимфоциты. При опухолевых процессах происходит нарушение их дифференцировки, что чревато развитием иммунодефицитов или аутоиммунных заболеваний. Самым частым из них является миастения – нарушение нервно-мышечной проводимости, развивающейся из-за воздействия антител на рецепторы ацетилхолина. При этом возникает мышечная слабость и патологическая утомляемость. Миастения характерна для типа лимфом В1-В3 и С.
- Аплазия костного мозга.
- Повышение температуры тела и ночные поты. Эти симптомы затрудняют дифдиагностику, поскольку более характерны для лимфом.
- На поздних стадиях присоединяется канцерогенная интоксикация: общая слабость, потеря аппетита, снижение массы тела.
Лечение тимомы
Лечение доброкачественной тимомы и злокачественной тимомы 1-2 стадии подразумевает хирургическое удаление вилочковой железы. Операция может быть выполнена в следующем объеме:
- Тотальное удаление тимуса вместе с окружающей жировой клетчаткой и лимфатическими узлами.
- Расширенное удаление тимуса – помимо вышеперечисленного объема, проводится еще резекция плевры и полное удаление переднестернальной жировой клетчатки.
При местно-распространенных злокачественных тимомах есть вероятность невозможности проведения радикального вмешательства, поэтому лечение рекомендуют начинать с адъювантной терапии. Обычно используется индукционная химиолучевая терапия с препаратами: циклофосфамидом, доксорубицином и цисплатином.
Объем операции будет зависеть от того, какие органы вовлечены в процесс. Может потребоваться резекция легочной ткани, перикарда, протезирование крупных кровеносных сосудов. Такие операции проводятся только на базе специализированных центров, в которых созданы условия для обширных вмешательств на органах грудной клетки. Для уменьшения развития рецидивов проводят послеоперационную лучевую терапию. При неоперабельных опухолях, ключевым методом лечения является химиолучевая терапия.
Последствия удаления тимомы
У пациентов, перенесших удаление вилочковой железы, есть риск развития миастенического криза – грозного состояния, при котором нарушается нервно-мышечная проводимость, из-за чего развивается сильная слабость мышц, сопровождающаяся параличами, нарушением дыхания и глотания. В тяжелых случаях возможен летальный исход. Для лечения пациентов применяется искусственная вентиляция легких и антихолинэстеразные препараты длительными курсами.
Прогнозы выживаемости
Прогнозы зависят от гистологического вида тимомы. При доброкачественных тимомах результаты лечения благоприятны, например, при типе В1 20-летняя выживаемость составляет около 90%. У пациентов со злокачественными вариантами тимомы прогноз будет зависеть от стадии распространения опухоли. При 2 стадии 5-летний рубеж переживают около 90% больных, при 3 стадии до 70% и при неоперабельных опухолях только 10%.
Источник
В. Л. Маневич, В. Д. Стоногин, Т. Н. Ширшова, И. В. Шуплов, С. В. Момотюк
II кафедра клинической хирургии (заведующий – профессор Тимофей Павлович Макаренко) Центрального института усовершенствования врачей на базе Центральной клинической больницы № 1МПС.
Публикация посвящается памяти Василия Дмитриевича Стоногина (1933-2005)
Заболевания вилочковой железы изучаются врачами различных специальностей: невропатологами, эндокринологами, иммунологами, гемато¬логами, хирургами, патогистологами и др. Проблема миастении является относительно изученной; в последние годы установлено участие вилочковой железы в таком жизненно важном процессе, как выработка (регулировка) иммунитета.
Опухоли и кисты вилочковой железы, миастения и некоторые аутоиммунные заболевания требуют хирургического лечения. Значительный вклад в этот сложный раздел внесли отечественные и зарубежные хирурги (А. Н. Бакулев и Р. С. Колесникова; В. Р. Брайцев; Б. К. Осипов; Б. В. Петровский; М. И. Кузин и соавт.; С. А. Гаджиев и В. Васильев; Viets, и др.).
С 1966 по 1973 год мы наблюдали 105 больных с различными заболеваниями переднего средостения, из них 66 с различными заболеваниями вилочковой железы. Эти больные были разделены на следующие клинические группы: 1-я – 30 больных с гиперплазией вилочковой железы и явлениями миастении; 2-я – 23 больных с опухолями вилочковой железы (тимомами), из них с доброкачественными 15, в том числе с явлениями миастении 9; со злокачественными 8, в том числе с явлениями миастении 5; 3-я – 4 больных с кистами вилочковой железы, все без миастении; 4-я – 3 больных с тератоидными образованиями; 13-я – 2 больных – лимфогранулематоз с изолированным поражением вилочковой железы; 6-я – 4 больных с апластической анемией на фоне аутоиммунной агрессии вилочковой железы.
Из 66 больных 65 были оперированы: 62 произведена радикальная и 3 эксплоративная операция.
С явлениями миастении под нашим наблюдением было 44 больных, из которых 43 (13 мужчин и 30 женщин) оперированы; возраст оперированных был от 14 до 55 лет, причем возраст большинства (25 больных) – от 15 до 30 лет. Среди больных с опухолями вилочковой железы преобладали 30-40-летние (13 больных).
Миастения – сложное нейроэндокринное заболевание, основным проявлением которого является слабость и особенно быстрая, патологическая мышечная утомляемость после физической нагрузки. Наряду с этим, согласно исследованиям ряда авторов (М. И. Кузин и соавт., и др.), при ми¬астении нарушается функция многих органов и систем (сердечно-сосудистой, дыхательной, пищеварительной, обмена веществ и т. д.).
Клиника миастении хорошо известна, однако правильный диагноз больному с миастенией нередко ставят после продолжительного наблюдения. У 32 из 44 наших больных правильный диагноз был поставлен только через 6-8 месяцев после появления первых признаков заболевания. Это объяс¬няется малой выраженностью клинической картины миастении в начальной стадии и плохой осведомленностью практических врачей, к которым впервые обращаются за помощью больные миастенией (невропатологи, окулисты, отоларингологи, терапевты).
При выраженной генерализованной форме миастении диагноз не труден. В начальной стадии и в случаях, когда миастения носит локализован¬ный характер (бульбарная, глазная, скелетно-мышечная, глоточно-лицевая), у наших больных предполагались самые разнообразные диагнозы, вплоть до подозрения на симуляцию. Считаем необходимым подчеркнуть особую важность прозериновой пробы, имеющей дифференциально-диагностическое значение. У больных миастенией внутримышечная инъекция 1-2 мл 0,05% раствора прозерина устраняет мышечную слабость и быструю утомляемость, в то время как при миопатиях и мышечной слабости, вызванных другими причинами, инъекция прозерина не дает эффекта. Имеют значение динамометрия, эргометрия и электромиография.
Общепризнано, что лечение миастении должно проводиться комплексно с участием 3-4 специалистов: невропатолога, терапевта-эндокринолога, анестезиолога-реаниматолога и хирурга. На основании большого клинического материала (сотни оперированных и наблюдаемых в отдаленном периоде) авторы подчеркивают преимущество оперативного лечения миастении перед консервативным (М. И. Кузин; А. С. Гаджиев и соавт., и др.). Результаты оперативного лечения лучше, если операцию производят впервые 2-2,5 года от начала заболевания. В более поздние сроки операция оказывается менее эффективной. Отсюда вытекает особая важность ранней диагностики миастении.
Из 43 оперированных нами больных в первый год заболевания миастенией поступили лишь 12, в сроки от 1 года до 3 лет – 23 и после 3 лет – 8 больных. Следовательно, больные поступали в клинику для оперативного лечения поздно.
Специальным методом исследования вилочковой железы является рентгеноконтрастный – пневмомедиастинография, которая позволяет судить о степени увеличения вилочковой железы, её структуре – отдель¬ный узел с четко ограниченными контурами или опухоль с инфильтрирую¬щим ростом и т. д.
Наличие у больного выраженной клинической картины прогрессирующей миастении является показанием к операции, так как все консервативные методы лечения, включая и рентгенотерапию, дают лишь временное улучшение.
У больных миастенией необходима специальная предоперационная подготовка, цель которой – снижение проявлений миастении путем индивидуального подбора дозы лекарственных препаратов. Дозировки препаратов подбирают строго индивидуально, с таким расчетом, чтобы в течение суток не наблюдалось периодов миастенического истощения, не наступало миастенического криза. Предоперационная подготовка, являясь симптоматической терапией, оказывает некоторое лечебное действие, что имеет положительное значение для предстоящей операции. Однако не у всех больных предоперационная подготовка, несмотря на ее комплексность и интенсивность, оказывается эффективной.
Вопрос о необходимости предоперационной рентгенотерапии нельзя считать окончательно решенным. Только 5 из наших больных перед операцией получали рентгеновское облучение, причем каких-либо улучшений в течении послеоперационного периода мы у них не отметили. У больных, оперированных по поводу злокачественной тимомы с явлениями миастении, предоперационное облучение играет важную роль в ближайшем исходе операции и в какой-то степени влияет на сроки наступления рецидива заболевания (М. И. Кузин и соавт.).
Большинство операций по поводу миастении нами выполнено из переднего доступа путем полной срединной продольной стернотомии. Наиболее ответственным моментом операции является отделение железы от левой плечеголовной вены. Ранение этого сосуда опасно из-за массивного кровотечения и возможной воздушной эмболии. В одном случае произошло ранение этой вены, закончившееся благополучно (был наложен боковой сосудистый шов). При операции следует избегать наложения зажимов на железистую ткань, раздавливания её.
У 3 наших больных было сочетание миастении и загрудинного зоба. Произведены тимэктомия и субтотальная струмэктомия.
У 26 больных во время операции была повреждена медиастинальная плевра, в том числе у 8 больных с обеих сторон. Осложнений, связанных с операционным пневмотораксом, не было. Если во время операции плевра не повреждена, переднее средостение дренируется одной резиновой трубкой, конец которой выводят в нижний угол раны или через отдельный прокол ниже мечевидного отростка и соединяют с отсосом. Вслед за тимэктомией трахеостома (превентивно) была наложена 5 больным.
Если сама операция тимэктомии по сравнению с другими торакальными операциями не представляет особой сложности, то течение послеоперационного периода у ряда больных сопровождается осложнениями, на 1-м месте среди которых стоит миастенический криз. Поэтому операции по поводу миастении возможны только в тех учреждениях, где можно обеспечить круглосуточное наблюдение анестезиолога-реаниматолога, а также многодневную аппаратную вентиляцию лёгких.
Вопрос о назначении антихолинэстеразных препаратов в послеоперационном периоде окончательно не решен. С целью уменьшения гиперсекреции бронхов лучше назначать прозерин с небольшими дозами атропина.
Тяжелый миастенический криз с расстройством дыхания, сердечной деятельности, глотания и т. д. наблюдали в первые дни после операции у 26 больных. Вывести из криза консервативными мероприятиями удалось 7 больных; 19 больным была наложена трахеостома с переводом их на аппаратное дыхание, длительность которого составляла от 3 до 40 суток. Через трахеостому систематически круглосуточно аспирируют слизь из трахеобронхиального дерева. Питание больных, находящихся на аппаратном дыхании, осуществляется через зонд. Помимо медикаментозного лече¬ния, применения кислорода, использования дыхательной гимнастики, в последние годы всем больным миастенией в послеоперационном периоде проводится лечебный массаж всего тела, повторяемый несколько раз в день.
Трахеостомическую трубку удаляют после того, как у больного стойко восстанавливается самостоятельное дыхание.
Из 43 оперированных по поводу миастении в первые дни после операции умерли 3 больных. Это относится к периоду, когда в клинике только осваивались эти операции. Все больные оперированы в тяжелом состоянии. Отдаленные результаты прослежены у 26 больных: выздоровление наступило у 17 и улучшение (больные принимают антихолинэстеразные препараты) – у 8 больных; состояние осталось без изменений у 3 больных. Двое оперированных умерли от рецидива злокачественной тимомы (один – с явлениями миастении через 3 года, другой – с инфарктом миокарда).
Доброкачественные опухоли вилочковой железы (тимомы) представля¬ют собой узлы округленной формы с плотной капсулой. При гистологическом исследовании в этих опухолях наряду с соединительнотканными клетками обнаруживаются фибробласты и концентрически расположенные вытянутые эпителиальные клетки, напоминающие тельца Гассаля. Эти опухоли по строению напоминают склерозирующую ангиому, еще их называют ретикулярной перителиомой (Pope и Osgood). Особое место занимают липотимомы. Одни авторы относят их к доброкачественным опухолям, другие – к злокачественным (Andrus и Foot). Опухоли эти нередко достигают боль¬ших размеров и состоят из жировой дольчатой ткани, содержащей скопления тимоцитов и гассалевых телец. Если в опухоли преобладает жировая ткань, её рекомендуют называть липотимомой, если преобладают элементы вилочковой железы – тимолипомой.
Среди наших больных мы наблюдали 3 (2 мужчин и 1 женщину, все старше 40 лет) с липотимомой. У них опухоль была небольших размеров, с ровными четкими границами; опухоль была расценена нами как доброкачественная. Заболевание сопровождалось умеренно выраженными явлениями миастении. Один из этих больных поступил с жалобами на слабость и быструю утомляемость; при дальнейшем обследовании у него была выявлена тяжелая гипопластическая анемия. Больной оперирован; в ближайшем послеоперационном периоде отмечены благоприятные результаты.
Из 15 наших больных с доброкачественными тимомами у 9 (4 мужчин и 5 женщин) были явления миастении, у остальных опухоль ничем себя не проявляла и была выявлена случайно.
Злокачественные тимомы – плотные, различных размеров бугристые опухоли, нередко прорастающие капсулу. У больных с этими новообразованиями из-за быстрого роста опухоли, прорастания соседних органов или сдавления их рано развивается синдром медиастинальной компрессии. Больные жалуются на боли за грудиной, чувство давления в грудной клетке и др. Нередко злокачественные тимомы протекают с явлениями миастении, отмеченной нами у 5 из 8 больных. Злокачественная тимома может протекать и совершенно бессимптомно. Приводим пример.
Больной М., 19 лет, поступил 17.III.1966 года. Жалоб нет. После окончания средней школы при прохождении медицинского обследования для поступления в учебное заведение у него рентгенологически было выявлено опухолевое образование в переднем средостении. Признаков миастении нет. Пневмомедиастинография: в переднем средостении со всех сторон окутанное газом образование продолговатой формы размером 15*5 см, с участками просветления в центре; заключение: опухоль вилочковой железы, возможно, с участками распада. Произведена тимэктомия. Гистологически: злокачественная тимома ретинулоклеточного типа. Проведена послеоперационная рентгенотерапия. Осмотрен через 4 года после операции:, жалоб нет, состояние хорошее, признаков рецидива нет.
Дифференциальный диагноз доброкачественных и злокачественных тимом нередко бывает трудным. Злокачественная тимома по рентгенологическим признакам напоминает лимфогранулематоз и лимфосаркому. В отличие от этих образований тимома располагается непосредственно за грудиной, обычно бывает овально-сплющенной или конусовидной формы. Всякая тимома, протекает она с явлениями миастении или без них, подлежит удалению, В литературе имеются указания, что каждую тимому следует рассматривать как потенциально злокачественную опухоль (Б. В. Петровский; Seybold и соавт., и др.).
Кисты вилочковой железы встречаются довольно редко. Обычно это тонкостенные образования различных размеров, расположенные в толще железы, выполненные желтоватой или коричневатой жидкостью. Из-за эла¬стичности этих образований признаков сдавления окружающих органов не наблюдается. Клиническая картина кист, если они протекают без миастении, бедна. Как правило их обнаруживают случайно, при профилактическом осмотре. Все наши 4 больных (3 женщины и 1 мужчина) были старше 40 лет (41 год – 48 лет). Ни у одного больного не было признаков миастении, хотя описаны сочетания кисты вилочковой железы и миастении. Все были оперированы (тимэктомия) с благоприятным результатом.
У 3 оперированных нами больных опухоль переднего средостения по гистологическому строению была тератомой. Учитывая тесную связь образования с остатками вилочковой железы и наличие в самом образовании ткани вилочковой железы, мы расценили опухоль как тератому вилочковой железы. У 2 больных на основании признаков (появление в мокроте сальных масс, волос у одной больной, а также обнаружение органоидных включений на рентгенограмме у другой) диагноз был поставлен до операции, у третьей больной – лишь во время операции. Из 3 оперированных больных у 2 при¬шлось удалить не только тератоидное образование, но и долю лёгкого из-за вовлечения последнего в процесс (прорыв нагноившейся тератомы в верхнедолевой бронх). Высокая степень злокачественного превращения тератоидных образований, возможность нагноения и другие осложнения убеждают в необходимости раннего и радикального хирургического удаления этих новообразований.
Вопрос о возможности изолированного поражения вилочковой железы лимфогранулематозом представляется спорным. Мы наблюдали 2 больных, у которых до операции был установлен диагноз “опухоль вилочковой железы”. После операции, при гистологическом исследовании препаратов, диагноз был изменен: изолированное поражение лимфогранулематозом вилочковой железы. Принимая во внимание указания о возможности изолированного поражения вилочковой железы на ранних стадиях заболевания (С. А. Гаджиев и В. В. Васильев), оба эти наблюдения мы отнесли к патологии вилочковой железы. После операции за больными ведётся наблюдение в течение 5 лет. Признаков рецидива и генерализации процесса нет.
Заболевание, заключающееся в сочетании патологии вилочковой желе¬зы и гипопластической анемии, которая возникает вследствие избирательного поражения костного мозга без изменения продукции лейкоцитов и тромбоцитов, впервые описано Кацнельсоном в 1922 году. Позже было предположено, что вилочковая железа влияет на гемопоэтическую функцию костного мозга, регуляцию состава белковых фракций, состояние лимфоидной системы и т. д. (Soutter и соавт.). С тех пор опубликованы данные некоторых авторов об отдельных операциях на вилочковой железе при различных болезнях крови (А. Н. Бакулев, 1958; Chaemers и Boheimer, и др.). К настоящему времени нами произведены 4 операции тимэктомии у больных гипопластической анемией. О результатах этих операций говорить пока рано, так как после них прошел небольшой срок. Ближайшие результаты удовлетворительные у 3 больных.
Выводы
- В вилочковой железе возникает ряд патологических процессов, которые требуют оперативного лечения.
- Оперативное лечение по поводу миастении оправдано как при наличии рентгенологически и клинически определяемой опухоли, так и лишь при гиперплазии вилочковой железы.
- Операцию рекомендуется производить в ближайшее время после установления диагноза. Лучевое лечение целесообразно проводить после удаления злокачественной опухоли или если произвести радикальную операцию невозможно.
ЛИТЕРАТУРА.
1) Бакулев А. Н., Колесникова Р. С. Хирургическое лечение опухолей и кист средостения. М., 1967.
2) Брайцев В. Р. Врожденные дизонтогенетические образования средостения и легких. М., 1960.
3) Гаджиев С. А., Догель Л. В., Ваневский В. Л. Диагностика и хирургическое лечение миастении. Л., 1971.
4) Гаджиев С. А., Васильев В. Мед газета, 1973, №15.
5) Кузин М. И. Клин мед, 1969, № 11, с. 6.
6) Кузин М. И., Успенский Л. В., Волков Б. П. Вести, хир., 1972, №7, с.48.
7) Осипов Б. К. Хирургические заболевания легких и средостения. М., 1961.
8) Петровский Б. В. Хирургия средостения. М., 1960.
9) Andгus W., Fооt N., J. thorac. Surg., 1937, v. 6. p. 648.
10) Chaemers G., Boheimer K., Brit. med. J., 1954, v.2, p.1514.
11) Pope R., О s g о о d R., Am. J. Path., 1953, v. 20, p. 85.
12) S е у b о 1 d W., D о n a 1 d М. С., J. thorac. Surg. Clagett C. et al., 1950, v. 20, p.195.
13) Soutter G., Sommers Sh. R e 1 m о n Ch. et al. Ann. Surg., 1957, v. 146, p. 426.
14) Viets H., Brit. med. J., 1950, v. 1, p.139.
Данные об авторах:
Восстановление текста, компьютерная графика – Сергей Васильевич Стоногин.
Любое копирование материала запрещено без письменного разрешения авторов и редактора.
Работа защищена Федеральным законом о защите авторских прав РФ.
Источник
