Значение фагоцитоза при воспалении
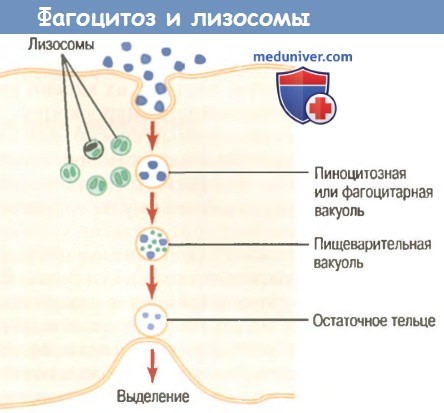
Фагоцитоз – это способность определенных клеток (фагоцитов) удерживать и переваривать плотные частицы. Это явление было открыто И. Мечниковым.
Фагоцитоз осуществляется микрофагами (нейтрофилами) и системой мононуклеарных макрофагов.
Мононуклеарные макрофаги
Система (MMS) включает следующие элементы:
- промоноциты (костный мозг);
- моноциты (кровь);
- тканевые макрофаги;
- гистиоциты соединительной ткани;
- печеночные клетки Куппера;
- легочные альвеолярные макрофаги;
- свободные и фиксированные макрофаги лимфатической ткани;
- плевру и перитонеальные макрофаги.
Клетки мононуклеарной системы объединяет общее происхождение гемопоэтических клеток и саморегуляция.
Моноцитопоэз
Моноцитопоэз – это стимулирующий фактор колонии фибробластов и фактор роста макрофагов, но он же подавляет (отрицательная саморегуляция) интерферон фибробластов и лейкоцитов и т. д.
Процесс фагоцитоза делится на четыре стадии:
- Приближение.
- Адгезия.
- Оседание;
- Стадия пищеварения.
Фаза приближения
Фагоцит приближается к объекту – бактериям, мервому клеточному элементу, инородному объекту. При движении под действием хемотаксиса цитоплазма фагоцита образует удлинения (псевдоподии).
Адгезия
Способствует образованию аминополисахаридов на поверхности фагоцитов и перекрытию фагоцитарного объекта белками сыворотки, особенно иммуноглобулинами. Последний механизм по сути является опсонизацией – бактерии и поврежденные клетки перекрываются с IgM, IgG и компонентами комплемента (C3, C5 и др.), что облегчает адгезию к фагоциту.
Адгезия
Поверхность фагоцита заряжена отрицательно, поэтому адгезия лучше, если объект, подлежащий фагоцитозу, заряжен положительно. Менее фагоцитарны отрицательно заряженные объекты, такие как опухолевые клетки.
Оседание
Этап фагоцитации объекта – путь инвагинации. Сначала фагоцит образует углубление, а затем фагосому – вакуоль, содержащую объект, подлежащий фагоцитозу. НАДН-зависимая оксидаза в мембране фагоцитов активируется до образования фагосом; в результате O2 превращается в O 2 ~ (супероксид-анион) и образуется H 2 O 2.
Эти продукты обладают бактерицидным действием, а также вызывают образование свободных радикалов. Под действием пероксидаз и каталаз H 2 O 2 расщепляется и высвобождается молекулярный O 2. Свободные радикалы и активный молекулярный O 2 действуют на мембрану фагоцита и объект, подлежащий фагоцитозу, активируя перекисное окисление липидов.
Липопероксиды и свободные радикалы неустойчивы к лизосомным мембранам и способствуют высвобождению лизосомальных ферментов.
Стадия пищеварения
Лизосомы присоединяются к фагосоме, содержащей фагоцитарный объект. Эти органеллы содержат все ферменты, необходимые для расщепления углеводов, белков, жиров и нуклеиновых кислот. В еще неактивной форме они попадают в вакуоль фагоцитов.
Пищеварительная вакуоль образуется при pH около 5,0, близком к оптимальному для лизосомальных ферментов. Активируются лизосомальные ферменты, и фагоцитарный объект постепенно переваривается. Во время стадии пищеварения проницаемость мембраны фагосомы увеличивается, содержимое фагосомы ускользает в цитоплазму, и микрофаг умирает (этому процессу способствует ацидоз). В этом случае фагоцитарный микроорганизм также может сохранять жизнеспособность.
Роль макрофагов в воспалительном процессе
Макрофаги начинают участвовать в фагоцитозе позже микрофагов. Макрофаги также более устойчивы к гипоксии и ацидозу, например, моноциты жизнеспособны даже при pH 5,5.
В очаге воспаления макрофаги выполняют несколько функций:
- Фагоцитируют бактериальные остатки, оставшиеся после эвакуации гноя и продуктов распада тканей – очищающая функция;
- Высвобождают лизосомальные ферменты – гиалуронидазу, аминопептидазу и др;
- Синтезируют компоненты системы комплемента и простагландины.
Взаимодействие макрофагов и лимфоцитов при хроническом воспалении
В то же время воспаленная тканевая среда также стимулирует образование фибробластов и фиброцитов. Постепенно появляется новая, богатая сосудами грануляционная ткань.
Фагоцитоз стимулируется продуктами повреждения тканей – внутриклеточные белки, ферменты, полипептиды, аминокислоты, электролиты и т. д., биологически активными веществами, половыми гормонами, тироксином, адреналином, лихорадкой. Но подавляется недостатком стимулирующих факторов, глюкокортикоидов, гликолортикоидов, ацетилхолина, ацетилхолина.
Фагоцитоз
Считается, что клетки плаценты и злокачественные опухоли способны секретировать вещество, которое подавляет функцию макрофагов, иммунологические реакции лимфоцитов и эмиграцию лейкоцитов, что приводит к значительному ослаблению или даже прекращению воспаления.
Объекты, которые фагоциты не могут переваривать, остаются в этих клетках в течение длительного времени и покрываются тонкой пленкой аминополисахаридов. После гибели фагоцитов они повторно фагоцитируются или выводятся из организма. Процесс, при котором фагоцит после переваривания высвобождает часть продуктов своего фагоцитоза в окружающую среду, называется экструзией.
Фагоцитоз – не единственный в организме механизм борьбы с воспалением. Большинство микроорганизмов погибают в условиях ацидоза, а также от ферментов, высвобождаемых во время гибели клеток и функционирования иммунокомпетентной системы.
Нейтрофилы во внеклеточном пространстве секретируют катионные белки, которые могут убивать ферменты без ферментов и фагоцитоза. Таким образом, воспалительные очаги постепенно избавляются от микроорганизмов и мертвых клеток.
Асептическое и острое воспаление
Дальнейшее течение воспаления зависит от того, является ли воспаление асептическим или бактериальным.
В асептических воспалительных условиях, например, вокруг хирургического шва, инородного тела, стенка микрофагов (нейтрофилов) начинает формироваться в течение нескольких часов, достигая максимума в течение дня.
Позже появляется следующий вал макрофагов, который достигает максимума через 2-3 раза. в день. Эмигрировавшие лейкоциты постепенно становятся неподвижными, больше не могут делиться и погибают в течение 3-5 дней. 2-3. на 5 сутки начинает формироваться стенка фибробластов, а на 5 сутки – соединительнотканная капсула.
Таким образом, в случае острого воспаления патогенный агент в организме преобразует белки, которые участвуют в реакции антиген-антитело, медиаторы и модуляторы воспаления, систему фагоцитов и миграцию клеток. В результате заканчивается острое воспаление. Однако, если инфекционные агенты попадают в участок асептического воспаления, например, в результате травмы, это воспаление становится септическим (бактериальным) воспалением.
Бактериальные воспалительные состояния бактерий и токсинов, не вызывающие гиперемии, экссудации и эмиграции лейкоцитов. Между клетками воспаленных тканей и особенно вокруг кровеносных сосудов накапливается все больше и больше микрофагов. Лизосомы микрофагов содержат множество активных ферментов, и эти клетки также начинают процесс фагоцитоза. При пальпации воспаленная ткань в это время кажется плотной, поэтому это называется стадией воспалительной инфильтрации.
По мере прогрессирования воспаления лейкоциты и те тканевые клетки, которые претерпели необратимые изменения во время воспаления, погибают. В этих клетках высвобождаются лизосомальные ферменты, которые расщепляют тканевые белки, белковые и липидные комплексы и другие структуры. Это стадия гнойного размягчения воспаления.
Эти стадии наблюдаются, например, у пациентов с гнойным воспалением перикарда (фурункул), гнойным воспалением апокринных потовых желез (гидраденит) и гнойным воспалением соединительной ткани (флегмона). При вдыхании воспаленная ткань выглядит мягкой, с характерным раскачиванием – флюктуацией. Образуется замкнутое скопление гноя – абсцесс.
Гнойное воспаление перикарда
Гной разрывается в направлении наименьшего сопротивления (либо наружу, либо внутри тела). Если гной попадает в кровоток (пемия), в организме может развиться множество очагов гноя, но под действием микроорганизмов и токсических веществ – угрожающее общее заболевание (сепсис, септикопиемия). Поэтому важно диагностировать накопление гноя и обеспечить хирургический дренаж гноя наружу.
Продолжение статьи
- Часть 1. Этиология и патогенез воспаления. Классификация.
- Часть 2. Особенности обмена веществ при воспалении.
- Часть 3. Физико – химические изменения. Роль нервной и эндокринной систем в развитии воспаления.
- Часть 4. Изменения в периферическом кровообращении при воспалении.
- Часть 5. Экссудация. Экссудат и транссудат.
- Часть 6. Эмиграция лейкоцитов. Хемотаксис.
- Часть 7. Фагоцитоз. Асептическое и острое воспаление.
- Часть 8. Распространение. Последствия. Принципы лечения воспаления.
Поделиться ссылкой:
Источник
Эмигрировавшие
в
очаг
воспаления
лейкоциты
имеют
большое
значение.
Они
участвуют
в
выработке
антител,
доставляют
в
очаг
воспаления
энергетические
вещества
(в
частности,
гликоген),
богаты
ферментами,
способствующими
эмиграции
и
пролиферации
ткани
(т.н.
трефонами),
отграничивают
здоровые
ткани
(т.н.
«лейкоцитарный
вал»),
являются
источниками
пирогенов
и,
основная
их
роль,
участвуют
в
процессе
фагоцитоза.
Фагоцитоз –
эволюционно
выработанная
защитно-приспособительная
реакция
организма,
заключающаяся
в
узнавании,
активном
захвате
(поглощении)
и
переваривании
микроорганизмов,
разрушенных
клеток
и
инородных
частиц
специализированными
клетками-фагоцитами.
К
ним
относятся
ПЯЛ
(в
основном
нейтрофилы),
клетки
системы
фагоцитирующих
мононуклеаров
(моноциты,
тканевые
макрофаги),
а
также
клетки
Купфера
в
печени,
мезангиальные
клетки
почек,
глиальные
клетки
в
ЦНС,
альвеолярные
фагоциты
в
легких,
свободные
и
частично
фиксированные
макрофаги
в
лимфоузлах
и
селезенке,
перитонеальные
и
плевральные
макрофаги
и
др.
Различают
4 стадии
фагоцитоза.
1
стадия
-приближение
фагоцита
к
инородному
предмету.
Основу
этого
движения
составляют
описанные
выше
явления
хемотаксиса
лейкоцитов.
2
стадия
-прилипания
фагоцита
к
объекту.
Она
объясняется
способностью
фагоцитов
образовывать
такие
цитоплазматические
выпячивания,
которые
выбрасываются
по
направлению
к
объекту
фагоцитоза
и
с
помощью
которых
осуществляется
прилипание.
Определенное
значение
при
этом
имеет
поверхностный
заряд
лейкоцитов.
Имея
отрицательный
заряд,
лейкоциты
лучше
прилипают
к
объекту
с
положительным
зарядом.
Прилипанию
предшествует
опсонизация,
т.е.
покрытие
иммуноглобулинами
М
и
J и
фрагментами
СЗ,
С5,
С6,
С7
бактерий
и
поврежденных
частиц
клеток,
благодаря
ему
они
приобретают
способность
прилипать
к
фагоциту.
Процесс
прилипания
сопровождается
усилением
метаболической
активности
лейкоцита,
его
аэробного
и
анаэробного
гликолиза
и
повышением
2-3 раза
поглощения.
3
стадия
– поглощение
объекта
лейкоцитами
(обволакивание)
может
происходить
двумя
способами.
Контактирующий
с
объектом
участок
цитоплазмы
втягивается
внутрь
клетки,
а
вместе
с
ним
втягивается
и
объект.
Второй
способ
заключается
в
том,
что
фагоцит
присасывается
к
объекту
своими
длинными
и
тонкими
псевдоподиями,
а
потом
всем
телом
подтягивается
в
сторону
объекта
и
обволакивает
его.
И
в
том
и
в
другом
случае
инородная
частица
окружена
цитоплазматической
мембраной
и
вовлечена
внутрь
клетки.
В
итоге
образуется
свободный
мешочек
с
инородным
телом
(фагосома).
Образованию
фагосомы
предшествует
повышение
метаболизма
с
активацией
НАДН-зависимой
оксидазы,
что
обеспечивает
синтез
перекиси
водорода.
В
результате
дегрануляции
лейкоцитов
выделяются
лизосомальные
ферменты
и
бактерицидные
белки.
Перекись
водорода
распадается
под
влиянием
оксидаз
с
образованием
активной
молекулы
кислорода,
которая
взаимодействует
с
компонентами
мембраны
клетки,
разрушая
ее
путем
перекидного
окисления.
4
стадия
– внутриклеточного
расщепления
и
переваривания
фагоцитированных
микробов
и
остатков
поврежденных
клеток.
Лизосома
приближается
к
фагосоме,
их
мембраны
сливаются,
образуя
единую
вакуоль,
в
которой
находится
поглощенная
частица
и
лизосомальные
ферменты
(фаголизосома).
В
фаголизосомах
устанавливается
оптимальная
для
действия
ферментов
реакция
(рН
около
5) и
начинается
переваривание
поглащенного
объекта.
В
лизосомах
содержатся
ферменты
(протеазы,
карбогидразы,
липазы
и
пр.),
обеспечивающие
гидролиз
веществ,
содержащихся
в
клетках,
в
том
числе
и
микробных,
но
их
бактерицидное
действие,
обусловлено,
в
основном,
наличием
миелопероксидазы.
Миелопероксидаза
железосодержащий
основной
фермент,
который
содержится
в
азурофильных
гранулах
нейтрофильных
гранулоцитов,
и
бактерицидное
действие
его
заключается
в
том,
что
в
присутствии
перекиси
водорода
и
йода
он
галогенизирует
белки
микроорганизмов.
Наряду
с
перевариванием
инородных
объектов
и
поврежденных
клеток
под
влиянием
гидролитических
ферментов,
выделившихся
в
фагосому,
гибнут
и
сами
фагоциты,
являясь
источником
образования
гноя,
а
продукты
разрушения
стимулируют
процессы
пролиферации
в
очаге
воспаления.
Особенно
отчетливо
значение
фагоцитоза
в
патогенезе
воспаления
выявляется
при
его
нарушении,
когда
даже
слабовирулентные
микроорганизмы
могут
вызвать
сепсис.
Фагоцитоз
в
этом
случае
носит
характер
незавершенного,
и
микробы,
поступая
с
лейкоцитами
из
очага
воспаления
в
различные
органы,
обеспечивают
явление
сепсиса.
Покраснение
(rubor) –
обусловлено
развитием
артериальной
гиперемии,
увеличением
притока
крови
с
повышенным
содержанием
О2,
увеличением
количества
функционирующих
капилляров.
Припухлость
(tumor) –
объясняется
артериальной
и
венознозной
гиперемией,
экссудацией,
эмиграцией
лейкоцитов.
Жар
(саlог) –
обусловлен
усилением
обмена
веществ
на
ранних
стадиях
воспаления,
притоком
крови
с
более
высокой
t°
(особенно
при
воспалении
кожи
и
слизистых),
усилением
теплоотдачи
за
счет
гиперемии.
Боль
(dо1ог) –
вызывается
раздражением
рецепторов
в
очаге
воспаления
медиаторами
воспаления
(особенно
кининами
и
простагландинами),
изменением
рН,
осмотического
давления,
механическим
раздражением
рецепторов
в
результате
припухлости
в
очаге
воспаления.
Нарушение функции (function laesa) является
следствием
повреждения
клеток,
нарушения
обмена
веществ,
кровообращения,
накопления
медиаторов
воспаления,
изменения
электролитного
баланса,
рН,
осмотического
и
онкотического
давления,
процессов
пролиферации.
В
этих
условиях
осуществления
функции
компонентами
функционального
элемента
(А.М.Чернух),
а
следовательно,
и
органа
невозможно.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
Фагоцитоз. Механизмы и значение фагоцитозаНаиболее важной функцией нейтрофилов и макрофагов является фагоцитоз — поглощение клеткой вредоносного агента. Фагоциты избирательны в отношении материала, который они фагоцитируют; иначе они могли бы фагоцитировать нормальные клетки и структуры организма. Осуществление фагоцитоза зависит главным образом от трех специфических условий. Во-первых, большинство естественных структур имеют гладкую поверхность, которая препятствует фагоцитозу. Но если поверхность неровная, возможность фагоцитирования возрастает. Во-вторых, большинство естественных поверхностей имеют защитные белковые оболочки, отталкивающие фагоциты. С другой стороны, большинство погибших тканей и инородных частиц лишены защитных оболочек, что делает их объектом фагоцитоза. В-третьих, иммунная система организма образует антитела против инфекционных агентов, например бактерий. Антитела прикрепляются к мембранам бактерий, и бактерии становятся особенно чувствительными к фагоцитозу. Для осуществления этой функции молекула антитела также соединяется с продуктом С3 каскада комплемента — дополнительной частью иммунной системы, обсуждаемой в отдельной статье на сайте (просим вас пользоваться формой поиска выше). Молекулы С3, в свою очередь, прикрепляются к рецепторам на мембране фагоцитов, инициируя фагоцитоз. Этот процесс выбора и фагоцитоза называют опсонизацией.
Стадии фагоцитоза а) Фагоцитоз, осуществляемый нейтрофилами. Нейтрофилы, входящие в ткани, являются уже зрелыми клетками, способными к немедленному фагоцитозу. При встрече с частицей, которая должна быть фагоцитирована, нейтрофил сначала прикрепляется к ней, а затем выпускает псевдоподии во всех направлениях вокруг частицы. На противоположной стороне частицы псевдоподии встречаются и сливаются друг с другом. При этом образуется замкнутая камера, содержащая фагоцитируемую частицу. Затем камера погружается в цитоплазматическую полость и отрывается от наружной стороны клеточной мембраны, формируя свободно плавающий фагоцитарный пузырек (также называемый фагосомои) внутри цитоплазмы. Один нейтрофил обычно может фагоцитировать от 3 до 20 бактерий, прежде чем он сам инактивируется или погибает. б) Фагоцитоз, осуществляемый макрофагами. Макрофаги представляют собой конечную стадию развития моноцитов, входящих в ткани из крови. При активации иммунной системой они становятся гораздо более мощными фагоцитами, чем нейтрофилы, и часто могут фагоцитировать до 100 бактерий. Макрофаги также способны поглощать гораздо более крупные частицы, даже целые эритроциты и иногда малярийных паразитов, тогда как нейтрофилы не могут фагоцитировать частички, размер которых значительно превышает размер бактерии. Кроме того, макрофаги могут выталкивать конечные продукты и часто живут и функционируют в течение многих месяцев. в) Сразу после фагоцитирования большинство частиц перевариваются внутриклеточными ферментами. После фагоцитирования инородной частицы лизосомы и другие цитоплазматические гранулы нейтрофила или макрофага немедленно вступают в контакт с фагоцитарным пузырьком, их мембраны сливаются, в результате в пузырек вбрасываются многие переваривающие ферменты и бактерицидные вещества. Таким образом, фагоцитарный пузырек теперь становится переваривающим пузырьком, и сразу начинается расщепление фагоцитированной частицы. И нейтрофилы, и макрофаги содержат громадное количество лизосом, наполненных протеолитическими ферментами, особенно приспособленными для переваривания бактерий и других чужеродных белковых веществ. Лизосомы макрофагов (но не нейтрофилов) содержат также большое количество липаз, которые разрушают толстые липидные мембраны, покрывающие некоторые бактерии, например туберкулезную палочку. г) И нейтрофилы, и макрофаги могут уничтожать бактерии. Кроме переваривания поглощенных бактерий в фагосомах нейтрофилы и макрофаги содержат бактерицидные агенты, уничтожающие большинство бактерий, даже если лизосомальные ферменты не могут их переварить. Это особенно важно, поскольку некоторые бактерии имеют защитные оболочки или другие факторы, предупреждающие их разрушение пищеварительными ферментами. Основная часть «убивающего» эффекта связана с действием некоторых мощных окислителей, образуемых в больших количествах ферментами мембраны фагосомы, или специфической органеллой, называемой пероксисомой. К этим окислителям относятся супероксид (О2-), пероксид водорода (Н2О2) и гидроксилъные ионы (-ОН), каждый из них даже в небольших количествах смертелен для большинства бактерий. Кроме того, один из лизосомальных ферментов — миелопероксидаза — катализирует реакцию между Н2О2 и ионами Cl с образованием гипохлорита — мощного бактерицидного агента. Однако некоторые бактерии, особенно туберкулезная палочка, имеют оболочки, устойчивые к лизосомальному перевариванию, и к тому же секретируют вещества, отчасти препятствующие «убивающим» эффектам нейтрофилов и макрофагов. Такие бактерии ответственны за многие хронические болезни, например туберкулез. – Также рекомендуем “Ретикулоэндотелиальная система. Макрофаги в лимфатических узлах” – Вернуться в оглавление раздела “Физиология человека.” Оглавление темы “Эритропоэз. Белые клетки крови”: |
Источник
